遺傳性耳聾能治了,又發論文的基因編輯真的能在人體實驗上成功嗎?_風聞
没有故事-还没写完的风闻小编2017-12-21 08:09
澎湃今天發了個新聞,説是基因編輯可以治療遺傳性耳聾。
雖然,目前很多案例顯示耳聾實際都和遺傳DNA突變有關,而目前已知的和耳聾相關的基因有近100個。**但迄今為止,幾乎沒有任何治療方法可以減緩或者逆轉耳聾。**而現在,阻止遺傳因素導致耳聾的技術離實現臨牀已越來越近。
北京時間12月21日,哈佛大學醫學院耳鼻喉科副教授Zheng-Yi Chen和哈佛大學化學與化學生物學教授、美國博德研究所核心成員David R. Liu共同主導的一項研究在線發表在在國際著名期刊《自然》(Nature),該團隊用基因編輯技術治療TCM1突變“貝多芬小鼠”的遺傳性耳聾,並取得良好效果。
內耳是聲音感知的最重要部位,其中內耳毛細胞又是人類聽到聲音的關鍵。其中,TCM1是內耳毛細胞中機械力傳導的重要組成部分,TCM1蛋白在內耳毛細胞的纖毛上形成通道,當聲波引起纖毛運動時這種通道就會打開,隨後鈣離子進入細胞生成電信號,電信號傳遞到大腦後形成聽覺。
TCM1發生了一種顯性負性錯義突變後,會導致內耳毛細胞單通道電流水平和鈣滲透率降低,進一步導致感音神經性語後聾(語言形成後出現耳聾)。通常,TCM1顯性突變患者在10-15歲時會開始逐漸變聾。
TCM1顯性突變即意味着,一對等位基因中只有一個發生突變就會導致功能喪失,從而致聾。這也就使得修復顯性突變成了一項精細的任務:**必須使突變基因失活,同時還要保留野生型基因。**這一對基因的差別只在於其中一個核苷酸的不同。突變的TCM1在原本野生型一個胸腺嘧啶核苷酸T的位置變成了腺嘌呤核苷酸A。
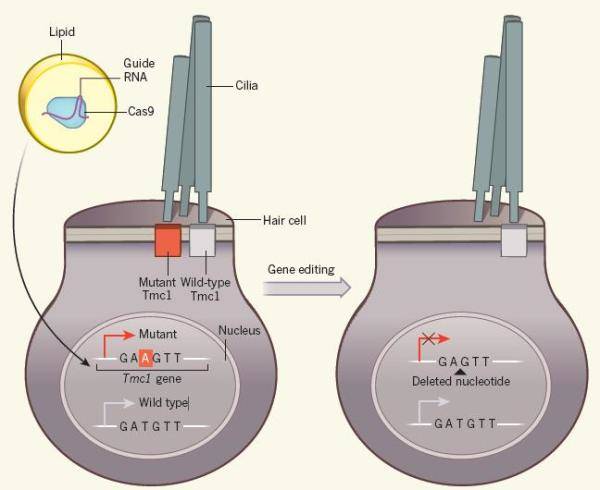
基因編輯過程示意圖
Chen和Liu團隊啓用的是熱門的CRISPR–Cas基因編輯技術。研究團隊將含有Cas9和RNA的脂滴注入新生TCM1貝多芬小鼠的內耳,這種脂滴能和細胞隨後融合。基因編輯後突變基因中腺嘌呤核苷酸A被敲除,從而使該基因失活。但同時保留了野生型基因,保證正常聽力功能實現。
研究團隊評估得出,基因編輯過的小鼠中內耳毛細胞的存活率更高、聽腦幹反應閾值更低。此外,聽覺反射也出現改善,基因編輯過的成年貝多芬小鼠在聽到突發噪音時會表現出驚嚇,然而未經基因編輯的小鼠對此毫無反應。
論文最後指出,這一治療途徑在治療和內耳毛細胞功能障礙有關的常染色體顯性遺傳耳聾方面具備潛力,也為反義寡核苷酸療法和RNA干擾療法提供了補充策略。
基因組編輯技術CRISPR/Cas9在2013年被《科學》雜誌列為年度十大科技進展之一,一直以來都受到學界的高度重視。
CRISPR是規律間隔性成簇短迴文重複序列的簡稱,Cas是CRISPR相關蛋白的簡稱。CRISPR/Cas最初是在細菌體內發現的,是細菌用來識別和摧毀抗噬菌體和其他病原體入侵的防禦系統。
雖然學界認為基於CRISPR/Cas9的基因編輯技術已經相對成熟,但是,人體實驗才剛剛開始。
2016年7月《自然》報道,**中國將進行世界首個在人體上的CRISPR–Cas9基因編輯試驗,**把通過CRISPR-Cas9基因編輯技術修飾的細胞,注入人體。由四川大學華西醫院的腫瘤學家盧鈾領導的團隊計劃於2016年8月在肺癌患者身上使用此項基因編輯技術。該臨牀試驗已在同年7月6日獲得了華西醫院倫理委員會的批准。但是,實驗結果如何目前還未有消息。
而且基於CRISPR的基因編輯技術並非沒有質疑。
2017年5月30日,《Nature Methods(自然方法)》期刊在線發表了一篇名為《體內使用CRISPR Cas9編輯後意想不到的突變》的文章。來美國哥倫比亞大學醫學中心的研究人員表示,通過全基因組測序結果的對比,研究人員發現經過CRISPR基因修飾的小鼠發生了上千個單核苷酸突變、100多個位點的大片段缺失或插入。這些突變都是目前實驗室常用的計算機模擬程序所無法檢測到的。
不知道基因編輯何時才能真正取得臨牀進展。