當FDA遇到傳統藥材,免不了又是一頓口水啊_風聞
岑少宇-观察者网专栏作者-观察者网专栏作者,演化之眼看世界2018-06-15 06:45
12日,雲南省藥物研究所暨雲南白藥集團創新研發中心(注)負責人披露,民族藥“痛舒膠囊”最近獲得美國食品藥品監督管理局(FDA)批覆,獲准在美國開展Ⅱ期臨牀研究。
本來,只是一條普通的醫藥新聞,但因為有FDA和傳統藥材這樣的元素,所以還是有點眼球。筆者認識不少關心傳統醫藥的人士,不管是“粉”是“黑”,他們的言論值得説道説道,剖析後或許可以讓我們更好地理解這件事。
1. 為什麼非要找FDA?
有些人覺得,中國的傳統醫藥別人不信拉倒,在國內用用就好。這些人一般都是樸素的“信徒”式愛好者,遠離醫藥行業,估計不知道藥物如果能在FDA獲批,將在全球市場上帶來多大的好處。
對於上市企業而言,哪怕沒有獲批,每一次試驗進展,都是利好消息,有可能帶動股價上揚——而云南白藥正是一家上市企業。
從理論上來説,很多人希望根據傳統醫學的辯證來設計臨牀試驗,這點在FDA確實不大可能做到,即使在國內也會在試驗對象的選擇上帶來許多額外的要求,增加大量人力物力財力投入。但藥企在成本與收益上肯定有自己的盤算,外人操心也沒用。
另一些人則樂見傳統醫藥去美國碰個頭破血流,到時候便可以用“孔乙己,你又偷了東西”的口吻嘲笑一番。
誠然,到目前為止,傳統藥材在FDA面前的成績是完敗。之前通過II期臨牀試驗的藥有好幾個,複方丹蔘滴丸還完成了III期臨牀試驗,可最終還是沒有通過。
但傳統藥材去FDA還是值得鼓勵。這也可以視作是傳統醫學現代化的嘗試之一,是中外交流的形式之一,哪怕背後的主要動因是商業考量,走出去也總比閉門的好。
不管是不是“粉”,如果連走出去都不鼓勵,那恐怕就是真“黑”了。
2. 區別看待“民族藥”與“中醫”,甚至貶低前者
這一點在普通人看來,可能匪夷所思,本來也分不大清什麼漢醫、蒙醫、藏醫,只在“保健品”廣告裏才聽説些。但在一些資深“中醫粉”裏,這種言論還頗有市場。
需要嚴正指出,《中醫藥法》裏明確規定了,“本法所稱中醫藥,是包括漢族和少數民族醫藥在內的我國各民族醫藥的統稱。”法律層面對各民族的傳統醫藥是一視同仁的。
不僅是傳統醫藥,整個農牧交界地區的文化傳統,本來就是現代中國繼承的一部分,硬要分個高低,實在沒有必要。
漢族的傳統醫學確實更為體系化,但這種博大精深,恐怕更多的來自於文化未斷絕、長期存續演變的優勢。世界各地都有傳統醫藥,只不過大部分都隨着文明消亡而失傳,或因文明式微而得不到良好的發展。
有人認為,文明傳承本身也有傳統醫學的功勞,但不得不指出的是,無論是一般的歷史學家還是專門研究中醫史的,對於中國傳統醫學在治癒率、整個人口的死亡率等方面,是否優於其他傳統醫學,都沒有形成可靠、明確的公論。
換言之,傳統醫學作為中華文明的一部分,在更大程度上可能是“搭便車”的,而不是“開便車”的,與書同文、車同軌等相比,恐怕沒有起到關鍵的作用。貶低世界上其他傳統醫學,缺乏依據,貶低少數民族醫學更是不可理喻。
3. 如何看待藥企宣傳與“割韭菜”?
很多人用天士力的複方丹蔘滴丸作為例子,認為從1997年在美國FDA申請註冊,搞了20年,最終還是失敗,教訓慘痛。而工程院院士李連達曾就此事寫道:“失敗並不可怕,可怕的是不肯認真總結教訓,不講真話,繼續用謊言愚弄羣眾。吹牛在前,失敗在後,始於謊言,毀於欺騙。”
在一些關心股市的人看來,藥企藉着FDA申請流程,可以製造股價波動,“明目張膽”地收割韭菜。所以對類似的藥企宣傳,都心存疑慮。
這麼想也情有可原,因為這幾年圍繞複方丹蔘滴丸的爭論,在相關人士中確實影響不小,堪稱“經典”。
天士力在公告裏對試驗結果避重就輕,挑有利的説。業內人士在匿名接受中國網等主流媒體採訪時,雖然不像李連達那樣言辭激烈,但也認為天士力“確實吹了很多年的牛”。
但另一面也很有故事,比如主要的質疑者之一祝國光,曾長期擔任天士力技術顧問。天士力方面稱,祝國光在合同到期終止後,多次索要不當費用未達到目的,因此攻擊公司產品。
李連達則早在2008年就質疑複方丹蔘滴丸的安全性與有效性,但當時他還是白雲山和黃公司首席科學顧問,是出於競爭關係,還是出於科學,説不清道不明。
更有趣的是,2009年祝國光還舉報過李連達學術論文造假,祝當時偏偏兼任了天士力集團技術顧問……恐怕他們自己也不會想到,十年不到,兩人就會一齊把矛頭指向天士力。
在非傳統醫學領域,也有“重啤”疫苗這樣的“經典”案例,事件影響更大,不過與本文主旨無關,就不再贅述了。
過去的戲固然精彩,但我們也要看到,現在的上市企業,已經越來越“乖巧”,否則被監管部門收拾,日子可不好過。
比如這次披露的信息雖然和雲南白藥集團有密切聯繫,但不是集團正式公告的,而是由研究所出面。
現在人們都知道“酒香也怕巷子深”,都會想盡辦法宣傳,受眾也習以為常,只要不出格,一般都能接受。
這次單就宣傳來説,沒有出現什麼偏差,確實是Ⅱ期臨牀,在少數民族醫藥裏,也確實是首次。負責人也在報道里提到,“創新研究從來都是九死一生的。Ⅱ期臨牀研究只是開始,路還很長,但我們有信心用實力應對挑戰。”
然而,真的要完全避免誤導,恐怕這樣還不到位。用“九死一生”來形容創新研究沒錯,但在中國傳統藥材赴FDA申請這樣的具體問題上,其實是“十死零生”。
至於媒體記者,基本上都是分條線的,負責“大健康”的記者們和醫藥企業低頭不見抬頭見,報道當然要從企業而非“韭菜”的角度出發,標題裏自然只會突出“首次”,而不會強調此前“十死零生”的大背景。
從這一角度來看,涉上市公司的信息管理,也是“路還很長”。
中國股市發展了這麼多年,還是屢屢出現因為與某熱點事件諧音而導致的暴漲暴跌,在這樣的環境下,更應該多從“韭菜”的角度出發,去思考如何管理。
所幸,這次雲南白藥並沒有出現股價的大幅波動,也許是新聞傳播不廣,也許是熟悉醫療版塊的“韭
菜”們已經練就了一身本領吧。
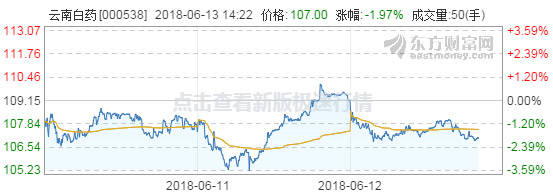
(11日到13日的股價情況,中間略有上揚,但迅速再次轉陰)
注:根據公開信息,雲南省藥物研究所2000年整體轉制進入雲南醫藥集團,2012年與雲南白藥集團雲南白藥研究院、雲南白藥集團無錫新型給藥系統工程技術中心,整合組建成雲南白藥集團創新研發中心,同時保留雲南省藥物研究所牌子和獨立法人地位。
從中也可以看出傳統醫藥企業與地方的密切聯繫,這在此前其他地方的多次事件中也有所體現。