新冠病毒又被“扒掉一層皮”!西湖大學成功解析病毒細胞受體空間結構,助力研發特效藥_風聞
量子位-量子位官方账号-2020-02-19 13:42
郭一璞 乾明 發自 雲凹非寺
量子位 報道 | 公眾號 QbitAI
新冠病毒入侵眾多人類的身體後,一個叫ACE2的結構在學術圈突然火了。
作為一個人類身體細胞中本來就存在的結構,ACE2被紛紛指責:
就是你這個奸細,把新冠病毒帶進了人體細胞!
雖然ACE2本身是人體細胞的正常結構,但它怎麼就被新冠病毒“利用”了呢?
針對ACE2“容易被利用”的特點,要提供怎樣的藥物、怎樣的治療方式,才能拯救更多人呢?
首先,必須摸清ACE2的底細,搞清它的結構,才好對症下藥。
現在,西湖大學把這件事做出來了。
ACE2:被新冠病毒“綁架”的細胞門把手
今天(2月19日)凌晨3點,西湖大學研究團隊在預印版平台bioRxiv上線最新研究成果:利用冷凍電鏡技術,成功解析新冠病毒受體ACE2的全長結構。
這也是全球第一次成功解析ACE2的全長結構。
有什麼用呢?對抗疫特效藥研發大有幫助。
ACE2,全稱Angiotensin-converting enzyme 2,中文名稱血管緊張素轉化酶2。
主要生理作用是促進血管緊張素(一種控制血管收縮和血壓的肽激素)的成熟,在肺、心臟、腎臟和腸道廣泛存在。
只是,當病毒入侵時,ACE2就被病毒“綁架”了。
它是SARS冠狀病毒(SARS-CoV)和人類冠狀病毒NL63的受體,可以説是多數冠狀病毒侵入人體的關鍵。
比如,當它被SARS冠狀病毒“綁架”後,就會變成一個這個樣子,像個大龍蝦:
“龍蝦鉗子”的部分,就是SARS病毒的S蛋白,它和ACE2的PD部分緊緊地結合在了一起,這樣,ACE2就被迫成為了“內奸”,引病毒入細胞。
而且,最近美國得克薩斯大學奧斯汀分校的研究團隊,還成功解析了新冠病毒的S蛋白結構,指出ACE2與新冠病毒的RBD之間的親和力,比其與SARS病毒的RBD的親和力高10-20倍。
也就是説,相比SARS,新冠病毒在“綁架ACE2”這件事兒上更得心應手。
這雖然還不能直接得出“新冠病毒傳染性是SARS 10-20倍”的結論,但“親和力”一項對比,也算為新冠病毒傳染性之強,找到了科學依據。
西湖大學研究團隊稱:“在SARS病毒和‘新冠病毒’侵入人體的過程中,ACE2就像是‘門把手’,病毒抓住它,從而打開了進入細胞的大門。”
ACE2全長結構的解析,對於後續疫苗和抗病毒藥物的研發,無疑提供了重要的結構生物學數據支撐。
“將有助於理解冠狀病毒進入靶細胞的結構基礎和功能特徵,對發現和優化阻斷進入細胞的抑制劑有重要作用“,清華大學全球健康與傳染病研究中心主任張林琦教授解釋。
此外,微博網友“三個大米袋”也給出了一個更形象的比喻:“就和知道鎖孔長啥樣然後照這個配鑰匙。不然就要用無數個鑰匙去試哪個可以開門。”
全球首次解析出ACE2的全長結構
根據西湖大學公佈的資料,ACE2的全貌長這樣:
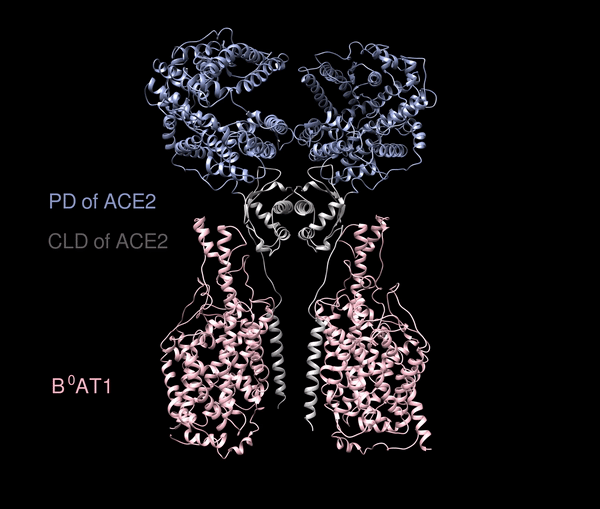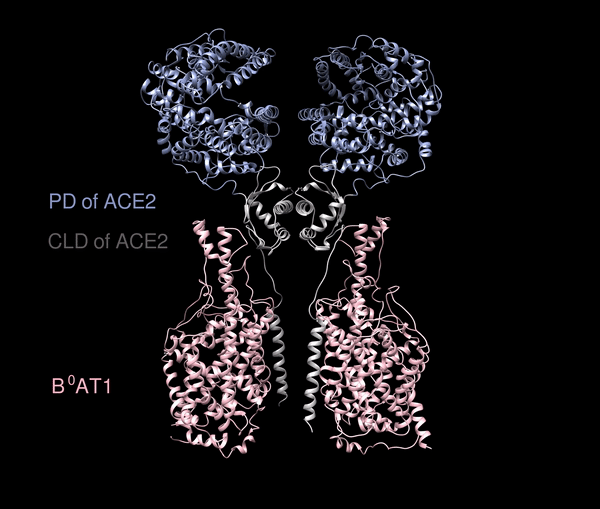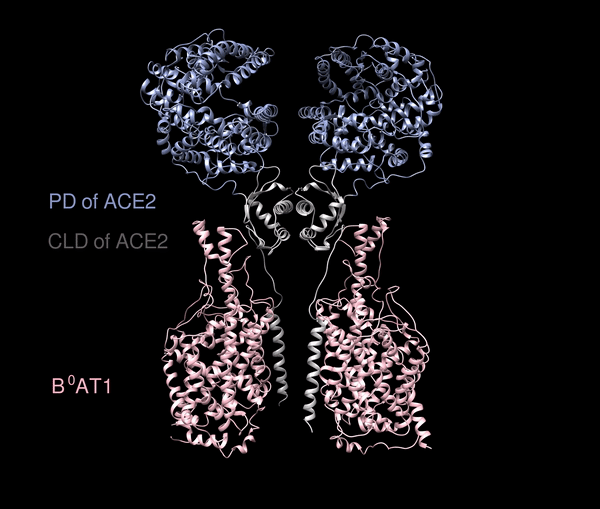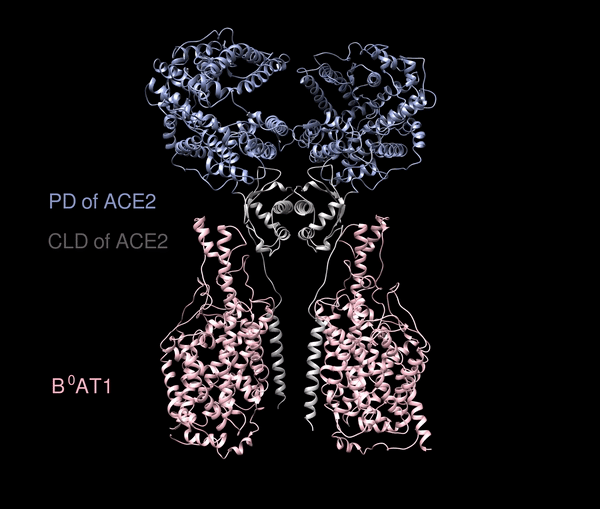
上面的藍色和灰白色部分,是ACE2的兩個結構PD(肽酶結構域,peptidase domains)和CLD(Collectrin樣域,Collectrin-like domain),但ACE2很難在體外穩定獲得,常常是與腸道內的一個氨基酸轉運蛋白B0AT1打包一同出現。
西湖大學研究團隊給出了大膽假設:這個複合物極有可能穩定住ACE2,並通過共表達的方法,能夠獲得優質穩定的複合物,就構成了上面這種X形狀。
在確定了ACE2的這種特殊存在形態後,就在冷凍電鏡下解析了它的三維結構:
圖中的分辨率是2.9埃。“埃”(符號Å)是計量光波長度和分子直徑的單位,一個“埃”是0.1納米。
而整個ACE2的結構,長這樣:
從給出的這些圖片資料可以看出,ACE2以二聚體形式存在,同時具有開放和關閉兩種構象變化,但兩種構象均含有與冠狀病毒的相互識別界面。
當然,ACE2只是新冠病毒感染人體細胞過程中的一部分,其關鍵在於新冠病毒的S蛋白與ACE2蛋白的結合。
因此搞清楚新型冠狀病毒S蛋白的結構,以及它與ACE2之間的相互作用,是需要進一步研究的重要方向。
西湖大學團隊稱,這一研究發現為進一步解析全長ACE2和新冠病毒的S蛋白複合物的三維結構奠定了基礎。
在他們看來,這個工作本身為理解新冠病毒侵染細胞,提供了很多有趣的線索。比如:
ACE2的二聚體與新冠病毒S蛋白的三聚體,是否可以發生更高層級的交聯,從而促進病毒與宿主細胞膜的融合或者內吞?
之前有研究表明ACE2的胞外區如果被切割,將會更有效地促進冠狀病毒的侵染,但是ACE2與B0AT1的複合物結構顯示,B0AT1的存在有可能阻礙蛋白酶靠近這個切割位點,這是否解釋了:病毒侵染症狀主要發生在沒有B0AT1的肺部?
西湖大學團隊成果
這篇論文一共5位作者,第一作者和通訊作者,都來自西湖大學浙江省結構生物學研究重點實驗室,由西湖大學創辦校長施一公擔任主任,而且作者都與現普林斯頓大學教授顏寧有極大淵源——眾所眾知,西湖大學校長施一公與顏寧教授是科學屆的知名師徒。
本次研究中,第一作者是鄢仁鴻(下圖左),是西湖大學生命科學學院博士後。本科就讀於山東大學,博士師從顏寧教授。
畢業之後前往西湖大學從事博士後研究工作。(顏寧教授透露,他畢業博士之後,因為不想異地戀,所以沒出國。)
通訊作者名為周強(上圖右),黑龍江齊齊哈爾人。2000年考入清華大學,攻讀學士學位之後,又師從隋森芳院士攻讀博士學位。
博士畢業後繼續留實驗室從事博士後研究工作,2015年博士後出站後在清華大學醫學院顏寧教授課題組任副研究員。
2019年初加盟西湖大學擔任西湖學者、特聘研究員,開展獨立研究工作。
值得一提的是,這也是西湖大學的首篇疫情相關的研究。
自西湖大學謀篇籌建以來,就明確以小而精的高水平研究型大學為目標,外界也有“中國加州理工”的期望。
西湖大學可追溯至2015年3月,其時施一公、陳十一、潘建偉、饒毅、錢穎一、張輝和王堅7位學術知名人士向國家提出希望申辦一所具有中國特色的、新型機制的國際化高水平研究型大學。
隨後,他們組成了西湖大學籌辦委員會,並註冊成立杭州市西湖教育基金會,作為西湖大學的舉辦方。
2016年12月,浙江西湖高等研究院正式成立,作為西湖大學辦學的依託主體和前身。
2018年4月,西湖大學獲批設立,成為中國第一所社會力量創辦的大學,學校辦學經費來源主要為舉辦者出資、辦學收入、競爭性科研項目經費及人才政策支持經費和政府扶持資金等。
2018年10月20日西湖大學正式成立之時,就已經籌資35億元,建造了66畝校園,聚集了68位科學家和139位博士生。
人才濟濟,也產出了諸多研究成果。
成功解析新冠病毒細胞受體的空間結構,也算是其最新代表,為新冠病毒疫情抗擊,貢獻了關鍵性一擊。
最後,附上論文鏈接:https://www.biorxiv.org/content/10.1101/2020.02.17.951848v1.full.pdf






