新冠疫苗不等18個月:中美開展人體臨牀啦!_風聞
疫苗与科学-疫苗与科学官方账号-2020-03-20 16:04
本週一(3月16日),美國打出全球首支人體臨牀試驗新冠疫苗。可以説,美國在新冠疫苗研發賽道上暫時處於領跑狀態。
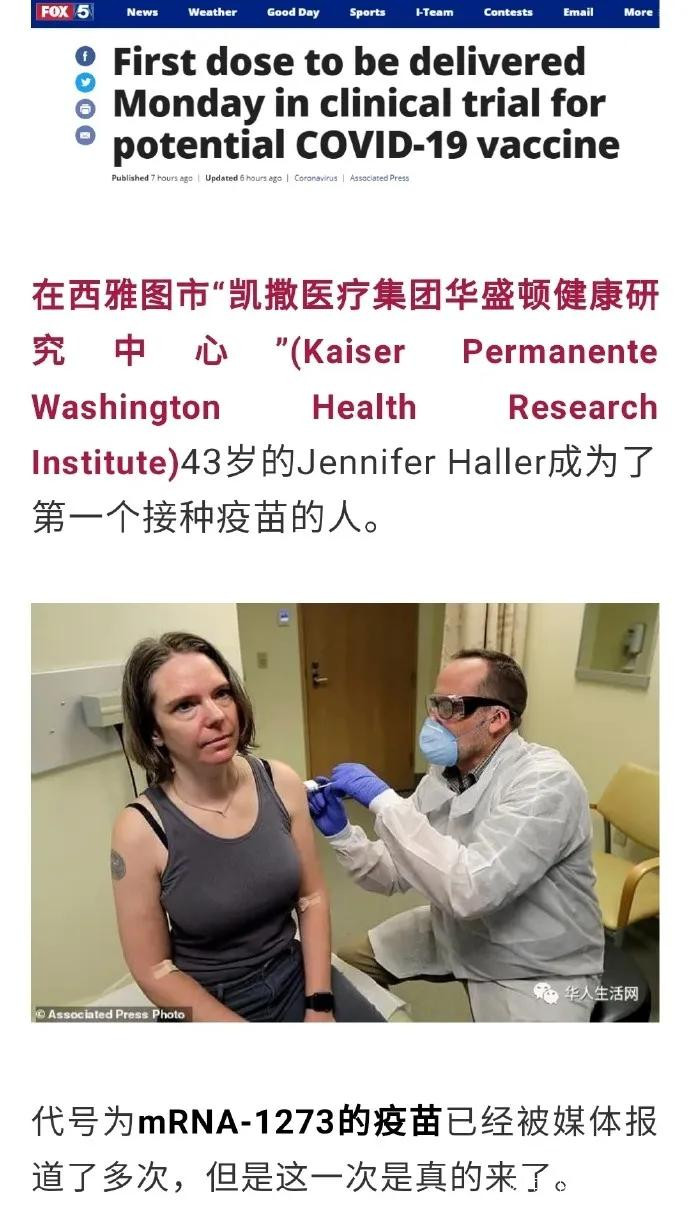
週二晚(3月17日),也就是在美國拋出上面消息後第2天,央視新聞頻道報導重大消息:陳薇院士的腺病毒載體新冠疫苗,也已獲批開展人體臨牀試驗。

在腺病毒載體新冠疫苗獲批人體臨牀消息發佈前,湖北省疾控中心就已經建立起志願者招募系統,需要招募若干18-60歲健康人,並能堅持完成6個月的隨訪。如果陶醫生在湖北當地,一定報名參加。目前,我正在聯繫上海的mRNA新冠疫苗研發企業,爭取能參與4月中旬開始的人體臨牀試驗。
如果要説全球誰最先打出第一支人體臨牀試驗的新冠疫苗,倒還真不好説。美國的16日西雅圖時間比中國的北京時間要晚17小時,目前沒有更詳細的接種時間披露,希望將來可以準確分出第一和第二來。

朱鳳才教授完成我國多項重要的一類新疫苗研發,包括幽門螺桿菌疫苗、四聯疫苗、戊型肝炎疫苗。他在疫苗臨牀試驗領域中發表論文近100篇,是中國疫苗臨牀試驗的首席專家。

2月11日,世衞組織總幹事譚德賽先生表示,新冠疫苗只是【可能在18個月內完成】。然而,譚先生一定沒有想到1個月後,中國的防控形勢一片大好,歐美以及全球的疫情已經幾乎陷入失控狀態,美國股市已經連續熔斷三次,如果沒有特效藥及疫苗,中國以外的其他國家似乎都無法阻止病毒的掃蕩。
在這種危急的形勢下,疫苗幾乎成為救命稻草。所以陶醫生認為,新冠疫苗的研發會進一步壓縮非必要環節,最快有可能從現在起2個月左右完成第1期和第2期人體臨牀,在第3個月就進入大規模的第3期人體臨牀或者直接應用。

新冠疫情發生在武漢,但病毒源頭還沒有查明。世界衞生組織和國際社會明確反對將病毒同特定國家、地區相聯繫,反對搞污名化。然而,美國一些政客把新冠病毒和中國相聯繫,這是對中國搞污名化,連美國總統最近在推特上把新冠病毒説成中國病毒。
既然美國這樣口無遮攔,來而不往非禮也,我們也不妨腦洞大開。基於陶醫生對mRNA疫苗的認識,我提出以下質疑:
美國把人當小白鼠:mRNA疫苗的動物試驗結果都沒有披露,有沒有可能為了趕進度而違反醫學倫理直接上人體試驗呢?
病毒或起源於美國:人用mRNA疫苗之前從未上過人體臨牀,如果美國不是早就拿到病毒並開始秘密研發,怎麼可能那麼快呢?
不是隻有陶醫生有這樣的疑慮,清華大學長庚醫院的急危重症部部長陳旭巖3月17日在接受央視《今日關注》採訪時表示:美國的新冠疫苗上人體臨牀實在太快了,除非很早就做準備。
3月12日晚,外交部發言人趙立堅在推特上,也用中英雙語連發5條推文怒懟美國:美國疾控中心主任被抓了個現行。零號病人是什麼時候在美國出現的?有多少人被感染?醫院的名字是什麼?可能是美軍把疫情帶到了武漢。美國要透明!要公開數據!美國欠我們一個解釋!
以上純屬非科學,大家權當看戲就行。
言歸正傳,美國的技術實力還是非常強大的,這次上人體的mRNA疫苗來自 全球mRNA疫苗巨頭之一的Moderna。2018年2月,該公司成立6年就融資16億美元,市值高達70億美元。其核苷修飾技術能極大提高mRNA的穩定性,且能夠調節mRNA藥物在體內的半衰期。
在 Moderna公開的新冠疫苗研發時間表上我們看到,從1月11日拿到我國分享的病毒序列,到3月16日第1支試驗疫苗接種人體,只用了63天時間。關鍵是,這個時間表裏沒有看到動物試驗的記錄。
陶醫生很難想像,一種疫苗沒有經過動物試驗就直接上人體試驗。不過,如果mRNA疫苗是一種顛覆性的優秀技術,那麼跳過動物試驗大大縮短研發過程也並非不可理解,我隨時準備接受這種新生事物的新遊戲規則。
從 Moderna公佈的資料來看,在過去的四年中,他們已經開展了9項mRNA疫苗的臨牀試驗,有超過1000人接受了該技術的疫苗,針對的病原體有兩種流感病毒、呼吸道合胞病毒、人類偏肺病毒、副流感病毒3。
Moderna此前曾開發了針對MERS冠狀病毒的疫苗,儘管該項目還處於研究階段,但為這次的新冠疫苗研究提供了重要的經驗。
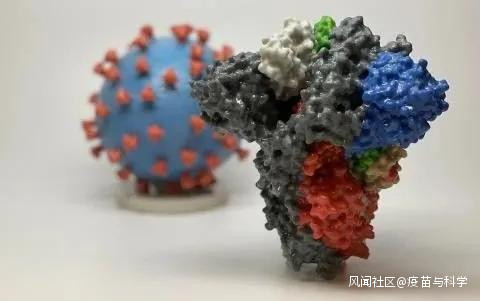
3D打印的新冠病毒(背景)和做疫苗的突觸蛋白(前景)
可見,Moderna在mRNA疫苗研發領域實力確實非常強大,這次新冠疫苗不經過動物試驗直接上人體,陶醫生認為可能的原因是:並不是説不需要動物試驗,而是基於其既往的大量經驗以及與新冠病毒非常相似的MERS病毒的研發經歷,使公司有信心略去動物試驗階段。
不過,陶醫生仔細研究了Moderna的新冠疫苗第1期臨牀方案,發現這種疫苗需要接種2劑間隔28天,且分了3個劑量組(25/100/250微克),每組15人。
Moderna的這種接種方案意味着什麼?
首先,需要間隔1個月接種2劑,無法體現出mRNA疫苗的重大優勢。
mRNA疫苗重大優勢之一是可以在體內表達疫苗成分。這個優勢需要實現可控的持續表達,讓每個人只接種1劑就可以實現長期免疫。如果實現這個優勢,完全可以革任何現役疫苗的命,因為現役疫苗絕大多數需要接種多個劑次。
相比之下,陳薇院士的腺病毒載體疫苗人體臨牀試驗只需接種1劑,比Moderna的疫苗節約1個月。疫苗的人體臨牀試驗分3期,所以理論上我們可以比Moderna快3個月,是不是也有點優勢呢?
其次,分3個劑量組,最高組250微克,是最低組的10倍。
疫苗有效成分的劑量通常為微克級,比如乙肝疫苗通常是10微克,戊肝疫苗是30微克,流感疫苗各組分為15微克,流腦AC多糖疫苗各組分為50微克,宮頸癌4價疫苗各組分為20或40微克。
陶醫生諮詢了業內專家,疫苗人體臨牀1期設計多個劑量組是很常見的,這通常叫做爬坡試驗,是為了確定最合適的劑量,不過最高劑量一般不超過100微克,Moderna的250微克劑量並不常見。陶醫生認為,mRNA疫苗屬於新技術,其合適的人用劑量還需要摸索,所以其劑量尺度比較大。
再説陳薇院士的腺病毒載體疫苗,也分了3個劑量組開展人體臨牀。疫苗液裏腺病毒顆粒含量為1×10^11個/mL,3個劑量組分別接種0.5mL,1mL和1.5mL,最高劑量只是最低劑量的3倍而已。這樣看來,是不是比mRNA疫苗更有把握呢?畢竟基於腺病毒載體的埃博拉疫苗已經成功過了。
疫苗中腺病毒顆粒含量為1×10^11個/mL
另外,腺病毒載體疫苗由於有埃博拉疫苗的經驗,各期臨牀的觀察時間也可能大幅度縮短。而按照美國美國國立衞生研究院的人體臨牀試驗計劃,mRNA疫苗需要在接種後的一年內進行隨訪。
關於腺病毒載體疫苗與mRNA疫苗的PK,陶醫生還諮詢了業內專家,再給大家補充一些專家觀點:
1. 腺病毒疫苗是否會被體內抗體中和?
專家:這種現象存在。腺病毒是一種感冒病毒(不是流感病毒),有多個型別,這次新冠疫苗使用一種很常見的腺病毒型別,所以人體很可能對其有一定的抗體,確實會干擾疫苗的效果。有兩種技術方法可以克服這種干擾:一是提高疫苗劑量;二是採用噴鼻或口服方式。這些都需要在臨牀試驗中去觀察與調整。
2. 腺病毒疫苗為何只需接種1劑?
專家:目前觀察到腺病毒載體進入人體後,可以持續表達S蛋白(即疫苗的關鍵成分)一段時間,能有效刺激人體的免疫系統,所以目前只安排1劑。mRNA疫苗進入人體後容易降解,所以可能需要兩劑。轉基因S蛋白疫苗或滅活疫苗,目前看來都無法做到只接種1劑,活疫苗有可能只需1劑。
目前,美國的新冠疫苗研發技術除了mRNA疫苗,似乎沒有其他技術的報導。中國則是多條技術路線並進,整體進展順利。

科技日報圖 http://t.cn/A6zYclxC
病毒載體疫苗和核酸疫苗(mRNA疫苗和DNA疫苗)都是新技術,即便研發成功,量產可能也會遇到問題。但只要這些新技術能率先證實基於病毒S蛋白的疫苗有預防作用,那麼重組蛋白疫苗的高純度大規模量產技術就能提供強大的產能支持了。所以,我國的新冠疫苗有多種保險機制,成功的概率大多了。
陶醫生總結:新冠疫苗的研發速度,已經不能用常規思維去評價。美國看起來略微領先,但中國緊追其後,我們完全可能實現反超,笑到最後。中國的口罩和疫苗,可以成為挽救世界的利器,成為我們踐行人類命運共同體的最佳方案。