新冠病毒檢測之戰:面對西方壟斷,中國是如何突圍的?_風聞
铁血军事-军事肥宅2020-04-16 11:12
作者:正解局
本文經授權轉載自微信公眾號:正解局(ID:zhengjieclub)。
開篇導語

新冠病毒檢測之戰再次啓示我們,關鍵技術,還是要掌握在自己手裏。
鐵血軍事
早發現、早隔離、早治療——這是中國抗擊新冠病毒的經驗。
早發現是前提,發現要靠檢測,檢測又離不開核酸檢測試劑。
核酸檢測試劑的成功研發與生產,無疑是抗擊病毒的關鍵一戰。
一度被歐美壟斷的核酸檢測,中國是如何成功突圍的?
1. 檢測試劑為何重要?
在武漢戰疫初期,幾乎每天的新聞都在報道武漢核酸檢測試劑數量不夠,不是每個人都能夠得到檢測。
也正因如此,李蘭娟院士説“早發現、早診斷、早隔離、早治療,目前在武漢還做不到,希望全國支持武漢”。
那麼,核酸檢測試劑為何備受矚目?
核酸檢測直接對標新冠病毒RNA的特異片段,利用熒光PCR技術,憑藉指數級的複製,即便病毒載量低,也能成功檢測出病患是否被感染。
核酸檢測,是目前臨牀上進行病例確診的“金標準”。
▲ PCR技術 來源:必應
除了核酸檢測,抗體檢測也是臨牀上普遍使用的檢測方法。但是,與核酸檢測相比,抗體還有一定的侷限性。
這是因為,病患產生IgM抗體一般需要一週的時間;而核酸檢測是直接檢測方法,只要患者體內病毒濃度達到一定範圍就可以檢測到。
所以,國內外的臨牀指南都通過核酸檢測來驗證病患是否已感染新型冠狀病毒。

▲ 核酸檢測試劑 來源:美疾控中心官網
核酸檢驗需要針對新型病毒開發特異性高的檢測試劑,中國高效的檢測試劑研發和生產能力為抗擊疫情提供了強有力的支持。
1月23日10時,武漢封城。
1月26日,之江生物成為國內首個經藥監局批准獲得三類醫療器械證書的新型冠狀病毒核酸試劑生產商。

▲ 之江生物新型冠狀病毒2019-nCoV核酸檢測試劑盒
隨後,其他企業紛紛跟進。3月27日,國家藥監局應急審批通過1個新冠病毒檢測產品。
至此,中國的新冠病毒檢測產品總數已達23個,包括核酸檢測試劑15個和抗體檢測試劑8個。

▲ 藥監局應急批准檢測試劑 來源:國家藥監局官網
聖湘生物新型冠狀病毒核酸檢測試劑日均產能最高可達50萬人份;達安基因3月19日在互動平台表示,公司新冠核酸檢測試劑盒產品向市場累計供應超過500萬人份。
政府官方數據,國內核酸檢測試劑日產能近260萬人份,抗體檢測試劑日產能近100萬人份,核酸試劑供給有力地保障疫情防控需求。
同時,“中國製造”的檢測試劑,走出國門,走向世界。
歐洲疫情肆虐,對病毒檢測的需求大幅度增加,核酸檢測試劑陷入緊缺。在滿足我國病毒檢測需要的基礎上,中國的檢測試劑以各種渠道“走出去”。
▲ 中國向日本捐贈核酸檢測試劑
中國不僅捐贈了一批又一批試劑,也已經向意大利、英國、荷蘭等十餘個國家銷售。
2. 中國突圍之路
核酸檢測是體外診斷(IVD)重要分支,中國的起步很晚。
20世紀70年代末,隨着改革開放的到來,中國體外診斷產業才開始發展。
國內陸續出現體外診斷試劑的生產廠家,但生產規模小而單一,大多數產品也僅限於零星的實驗室研究使用,比如生物樣本檢測等。
相比之下,歐美等發達國家已經對快速發展的體外診斷產業實施制度監管。
國內的檢測試劑市場一直被國外企業壟斷,直到上世紀最後十年,國產的商品化成套試劑盒才逐漸進入臨牀。
進入新世紀後,中國的IVD產業迎來快速發展,又是如何突圍的呢?
其一,國家長期對基礎學科特別是生物研究的投入,為診斷試劑的開發提供了充足的智力支持。
2005-2016年,國家政策大力扶持生物醫藥產業的發展,重視對高端人才的培養,吸引了更多優秀的人才投身生物醫藥研究。研發機構人員數量由1577人增加至11494人。
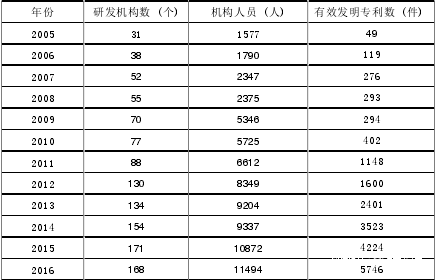
▲ 2005-2016年生物醫藥產業研發機構和專利數量
來源:中國高技術統計年鑑
其二,優厚的人才政策,吸引了大量海外人才歸國,這些海外精英把檢測技術帶回國內。
湖南聖湘生物科技有限公司董事長戴立忠,早年赴美攻讀碩、博學位,畢業後加入美國最大的核酸試劑公司Gen-Probe工作。
2008年,他回國創業,在他的帶領下,團隊研發出高精度乙肝定量PCR檢測試劑,檢測時間比國內同類產品縮短90%以上,靈敏度仍高出50倍至100倍,價格僅是國外同類產品的1/3左右。
在這次的新冠疫情中,聖湘也第一時間開發出熒光PCR法核酸檢測試劑盒,順利通過國家藥監局審批,在臨牀上支援抗擊疫情。

▲ 聖湘獲批通告 圖片來源:國家藥監局官網
其三,國內高速發展的經濟和日益規範的投資市場,為創新企業發展保障了資金支持。
2005-2016年中國生物醫藥產業技術研發經費支出中,技術改造經費支出最大。
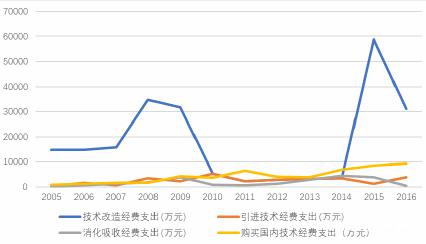
▲ 2005-2016年生物醫藥產業技術研發經費支出
來源:中國高技術統計年鑑
疾風知勁草,時勢造英雄。
新冠病毒突襲而來,無疑給了中國企業一次展現核酸檢測試劑研發能力的機會。
3. 美國先發,為何晚人一步?
作為後入場者,中國雖然奮力追趕,卻還未跑贏歐美國家的醫藥巨頭,IVD的全球市場仍然被歐美巨頭把持。
世界體外檢測產業呈現“4+X”的格局,以羅氏、西門子、雅培、貝克曼等為代表的前十大企業佔據了全球80.7%的市場份額。
美國無疑是檢測試劑的老大,排名前四的雅培、貝克曼等都是美國公司,世界排行前十的製藥企業,也有6家屬於美國。
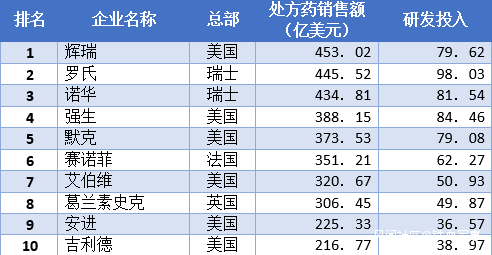
▲ 2019全球TOP10製藥企業
讓人好奇的是,美國為何在這次新冠疫情中落了下風呢?
首先,美國一線檢測人員較少,成為最大短板。
3月5日,美國官方表示,已向全國發放110萬份試劑。
3月11日的國會聽證會上,該數據被打臉,美國疾控中心承認,本部門每天僅能檢測300到350個樣本。美國副總統彭斯也向媒體記者承認:
美國現有檢測試劑不足,無法滿足檢測需求的預期增長。
3月18日,被問及“檢測資源不足,為什麼不少政界名人和社會名流卻能優先接受檢測”,特朗普回答道,“或許這就是人生吧。”

▲ 特朗普:這就是人生
其次,生物製劑的生產要求非常高,美國檢測試劑的製造出現問題。
2月12日,美國疾控中心對媒體表示,部分實驗室在檢測試劑盒有效性的過程中報告了“一些問題”,導致部分實驗室的檢測出現“無效結果”。

▲ 美國試劑短缺
最後,體制僵硬,流程繁瑣,審批過程過於複雜。
1月20日,美國用自行研發的試劑盒,成功檢測出了第一例由武漢入境華盛頓州的輸入型病例。然而,直到2月29日,美國食品藥品監督管理局更新檢測批准流程後,部分實驗室才被允許自行生產檢測試劑。
不可否認,美國的生物技術世界領先。在新冠病毒的檢測卻慘遭滑鐵盧,説到底,還是政府的動員能力出了問題。
面對重大公共緊急事件,考驗的不僅是科技實力,更是隨機應變的動員能力。
新冠病毒檢測之戰再次啓示我們,關鍵技術,還是要掌握在自己手裏。
假設中國無法自主生產檢測試劑,又將如何面對這場疫情?
本文授權轉載自:正解局(ID:zhengjieclub)。正解局,一個有見識、有深度、有誠意的時勢財經大號,華爾街見聞、雪球、螞蟻金服、世界經理人等10多家主流財經社區特邀入駐。每天全網閲讀超過100萬人次,在這裏,穿透信息迷霧,正解中國成長的力量。