2020年諾貝爾化學獎:基因編輯,眾望所歸_風聞
造就-造就官方账号-发现创造力2020-10-07 20:53
 北京時間10月7日傍晚,諾貝爾委員會宣佈,2020年諾貝爾化學獎被授予給Emmanuelle Charpentier和Jennifer a . Doudna,以表彰她們“開發出一種基因組編輯方法”——CRISPR/Cas9基因剪刀。這也是諾貝爾化學獎首次被兩位女性科學家共享。
北京時間10月7日傍晚,諾貝爾委員會宣佈,2020年諾貝爾化學獎被授予給Emmanuelle Charpentier和Jennifer a . Doudna,以表彰她們“開發出一種基因組編輯方法”——CRISPR/Cas9基因剪刀。這也是諾貝爾化學獎首次被兩位女性科學家共享。
利用這項技術,研究人員可以極其精確地改變動物、植物和微生物的DNA。這項技術還對生命科學產生了革命性的影響,正在為新的癌症療法做出貢獻,並可能使治癒遺傳性疾病的夢想成真。
****“這項基因工具藴含着強大的力量,影響着我們所有人。它不僅徹底改變了基礎科學,而且推動了創新作物的誕生,未來還將會為突破性的新醫學療法指明方向,”****諾貝爾化學委員會主席Claes Gustafsson説。
上海農業科學院生物技術研究所研究員唐雪明表示心情很激動:
“祝賀兩位女科學家!過去的3年,我都在期待基因編輯技術能獲得實至名歸的諾貝爾獎,基因編輯技術在過去幾年裏中在多領域的實踐都取得激動人心的成果。今年這個願望終於實現了。
兩位女科學家獲獎是眾望所歸,再加一個張鋒應該也是實至名歸。自從他第一個編輯了哺乳動物細胞以來,對基因編輯技術進步的貢獻真是無人能及!好可惜!我理解委員會還是把這個基因編輯技術的獎給了兩位切第一刀的人,而且解析了怎麼切,在哪切。諾貝爾獎關注的是第一發現者,絕對原創性,比如屠呦呦獲獎,田中耕一獲獎都是這樣。無論如何,祝賀基因編輯技術獲獎!”
眾望所歸的兩位獲獎者

Emmanuelle Charpentier
埃曼紐爾·卡彭蒂耶(Emmanuelle Charpentier),法國微生物學、遺傳學和生物化學教授和研究員,目前在德國柏林馬克斯·普朗克病原學研究所工作。
她的大部分研究都有一個共同對象:致病細菌。它們為什麼這麼好鬥?它們如何發展對抗生素的抵抗力?是否有可能找到可以阻止其進展的新療法?
2002年,卡彭蒂耶在維也納大學成立了自己的研究小組,專注於對人類造成最大傷害的細菌之一:化膿鏈球菌。每年,它感染數以百萬計的人,經常引起扁桃體炎和膿皰瘡等可治癒的疾病。但是,它也可能導致危及生命的敗血症並破壞體內的軟組織,被冠有“食肉者”的可怕稱號。
為了更好地瞭解化膿性鏈球菌,夏彭蒂爾首先徹底研究了這種細菌的基因是如何調控的。這項決定是發現基因剪刀的第一步。
卡彭蒂耶以破譯細菌CRISPR / Cas9免疫系統的分子機制並將其重新定位為基因組編輯工具而聞名。她發現了一種非編碼RNA成熟的新機制,該機制在CRISPR / Cas9的功能中至關重要,還證明了一種被稱為tracrRNA的小RNA對於crRNA的成熟至關重要。

Jennifer a . Doudna
詹妮弗·杜德納(Jennifer a . Doudna),美國生物化學家,現任美國加州大學伯克利分校教授,霍華德·休斯醫學研究所研究員。
在2012年,杜德納和她的同事們在鏈球菌細菌“ CRISPR ”免疫系統中發現的一種名為Cas9的蛋白質,該蛋白質與引導RNA協同工作,像剪刀一樣起作用。這種蛋白質會攻擊目標病毒的DNA並將其切成薄片,從而阻止其感染細菌。該發現減少了編輯基因組DNA所需的時間和工作。
杜德納在生物化學和遺傳學方面也做出了重要貢獻,例如她通過對核酶的X射線晶體學研究確定了其結構。
基因剪刀:重寫生活準則的工具
如果研究人員想要了解生命的內部運作原理,則必須掌握修改細胞中基因的能力。
這曾經是一項費時費力,有時甚至是不可能的工作。但現在有了CRISPR/Cas9這把基因剪刀,研究人員可以在幾周的時間內改變生命密碼。
CRISPR/Cas9技術誕生於2012年,其原理如同用剪刀剪切DNA,然後插入或重新排列基因代碼。

Cas9是一種內切酶,能剪切DNA雙螺旋結構的兩條鏈。有些內切酶會隨機剪切DNA長度的任何位點。其他內切酶會尋找特定的DNA序列,然後剪切那個位點。然而,同樣的序列會在基因組中多次出現,因此無法用限制性內切酶來剪切特定的一個位點。
和限制性內切酶不同,細菌性Cas9能剪切特定的一個位點,被剪切的DNA序列是指定的。Cas9與CRISPR系統關聯起來,後者使用一種小片段RNA來引導Cas9作用於靶位點。
在自然界,這種小片段RNA通常用來抵禦病毒(噬菌體)序列。Cas9尋找病毒序列,然後剪切它,因此CRISPR系統是細菌抗病毒防禦機制的一部分。
不過,這種引導Cas9的小片段RNA可以用研究人員選定的一個序列代替。CRISPR系統的一個好處在於,你可以提供不止一種引導分子,意味着你可以指導系統剪切不止一個位點。CRISPR系統能夠確定它要剪切的DNA序列,但脱靶編輯仍然時有發生,科學家們一直在想辦法解決這個問題。
**就像在科學上經常發生的那樣,CRISPR/Cas9發現純屬偶然。**埃曼紐爾·卡彭蒂耶在化膿性鏈球菌(對人類危害最大的細菌之一)的研究中,她發現了一種之前未知的分子——tracrRNA。她研究發現,tracrRNA是細菌古老免疫系統CRISPR/Cas的一部分,通過裂解病毒的DNA來消滅病毒。
2011年,卡彭蒂耶在發表了這一發現。同年,她開始與詹妮弗·杜德納合作。杜德納是一位經驗豐富的生物化學家,對RNA有深刻的瞭解。她們的最初想法是開發一種新形式的抗生素,最後卻成功地在試管中再造了細菌的基因剪刀,並簡化了剪刀的分子組成,使其更容易使用。
在一個劃時代的實驗中,兩人對基因剪刀重新編程,使其在自然形態下可以從病毒中識別DNA,在一個預定的位置切斷任何DNA分子。在DNA被切斷的地方,就很容易改寫生命密碼。
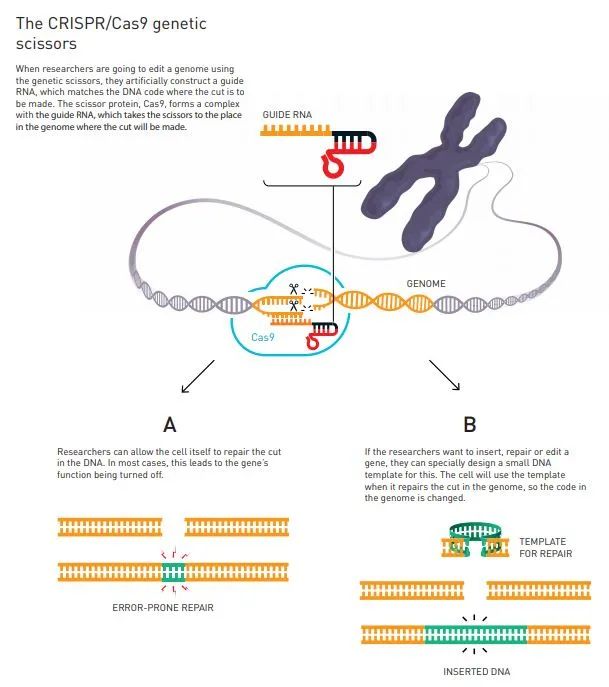
自CRISPR/Cas9基因剪刀2012年被發現後,這項技術被廣泛應用於各項領域。
現在,生物化學家和細胞生物學家可以輕鬆地研究不同基因的功能及其在疾病進展中的可能作用;
在植物育種中,研究人員可以賦予植物特定的特徵,例如在温暖的氣候下抵抗乾旱的能力;
在醫學上,該基因編輯器為新的癌症療法和試圖治癒遺傳性疾病的首批研究做出了貢獻。
除了上述優點之外,這把基因剪刀也很可能被濫用。例如,該工具可用於創建轉基因胚胎。但是,多年來,有控制基因工程應用的法律和法規,其中包括禁止以允許遺傳改變的方式修改人類基因組。另外,涉及人畜的實驗必須在進行之前得到倫理委員會的審查和批准。
可以肯定的是,這種新工具可能有助於解決人類目前面臨的許多挑戰,也將帶來新的道德問題,把生命科學帶入了一個新時代。
“數説”諾貝爾化學獎
111次頒獎
1901年以來,諾貝爾物理學獎共頒發過113次。其中有六個年份沒有頒發過諾貝爾物理學獎,分別是1916、1931、1934、1940、1941和1942年。
根據組委會的章程,在1901年至2019年之間,共頒發了111項諾貝爾化學獎。
自1901年以來,諾貝爾物理學獎共頒發過111次,其中有8個年份沒有頒發過諾貝爾化學獎,分別是1816年、1917年、1919年、1924年、1924年、1933年、1940年、1941年和1942年。
為什麼那些年沒有授予化學獎?根據諾貝爾組委會的章程規定,如果候選人的研究沒有達到一定要求,那麼獎金將被留至下一年。如果第二年仍然沒有合適人選,獎金將被加入到基金會的初始資金中。
在兩次世界大戰期間,因為戰爭關係,化學方面的突破較少,所以諾貝爾化學獎經常缺席。
183位獲獎者
自頒佈以來,諾貝爾化學獎被授予給184位在化學領域做出卓越貢獻的獲獎者。因為弗雷德裏克•桑格曾兩次獲得諾貝爾化學獎,所以全世界共有183人獲得過諾貝爾化學獎。
其中,諾貝爾獎有63次是個人單獨獲得,23次是兩人共享,25次是三人共享。
沒有過,也不會出現三人以上共享諾貝爾化學獎的場景。因為諾貝爾基金會章程規定:“獎金數額可以在兩件作品之間平均分配,每件作品都應被視為獲獎。如果獎勵作品是由兩個或三個人制作的,則應共同獎勵。在任何情況下,獎金數額均不得超過三人。”
97歲與35歲
在諾貝爾化學獎的獲獎者中,所有的獲獎者都不算太年輕。
年齡最大的諾貝爾化學獎獲得者是約翰·B·古德諾,是一位著名的固體物理學家,鋰離子電池的奠基人之一,通過研究化學、結構以及固體電子/離子性質之間的關係,設計新材料解決材料科學問題,被業界稱為“鋰電池之父”,他在2019年獲得化學獎時已經97歲。

最年輕的諾貝爾化學獎得主是弗雷德裏克·喬里奧特, 1935年他和妻子因發現人造放射性而被授予了諾貝爾化學獎,時年35歲,在一眾諾貝爾獎得主中算得上青年才俊。

喬里奧特與妻子伊雷娜·約里奧-居里
5位女性獲獎者
除今年之外,在獲得諾貝爾化學獎的183人中,僅有5位女性。
1911年,瑪麗·居里因發現元素釙和鐳獲獎(1903年獲得了諾貝爾物理學獎)。
1935年,伊雷娜·約里奧-居里(瑪麗·居里的女兒和最年輕的諾貝爾化學獎得主弗雷德裏克·喬里奧特的妻子)因發現人工放射性物質獲獎。
1964年,多蘿西·克勞福特霍奇金因通過X射線分析出分子構造獲獎。
2009年:阿達·約納特因核糖體的結構和功能研究獲獎。
2018 年:弗朗西斯·阿諾德因實現了酶的定向轉化獲獎。
百年諾貝爾:化學?物理?生理?傻傻分不清
1901年,諾貝爾獎首次被頒發。
第一位諾貝爾化學獎的得主是雅各布斯·亨裏克斯·範托夫,因發現了溶液中的化學動力學法則和滲透壓規律,以及對立體化學和化學平衡理論作出的貢獻而獲獎。

荷蘭化學家雅各布斯·亨裏克斯·範托夫
而這個世紀之交的節點,也恰巧是化學史上的轉折點。
處在科學中心的化學學科,既與物理學接壤,從物理學學科中獲取了理論基礎,又與生物學接壤,因為生物體擁有着世界上最複雜的化學系統。
因此,20世紀化學領域的初蓬勃發展,很大程度上要歸功於物理學的發展,同時又與生物學有着脱不開的關係。
1897年,劍橋大學的約瑟夫·約翰·湯姆森爵士宣佈發現電子,這些帶負電荷的“微粒”,質量比氫原子小1000倍,並因此獲得了1906年的諾貝爾物理學獎。

約瑟夫·約翰·湯姆森
19世紀90年代,曾在湯姆森實驗室工作的歐內斯特•盧瑟福,在湯姆森發現的基礎上,於1911年制提出了一種原子模型:原子的全部正電荷和幾乎全部質量都集中在原子核裏,帶負電的電子在核外空間裏繞着核旋轉。這一模型也被稱為“行星模型”。
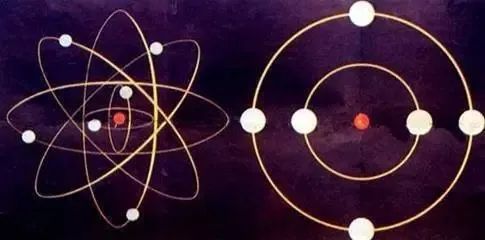
盧瑟福提出的原子模型
但是,人們很快發現,在盧瑟福的原子模型中,電子會以電磁輻射的形式失去能量,最終落入原子核,不符合經典物理定律。
1913年,哥本哈根的尼爾斯·玻爾提出了另一種原子模型。在這個模型中,當電子從一個軌道轉移到另一個軌道時,光被髮射(或吸收)。玻爾因其在原子結構方面的研究而獲得1922年的諾貝爾物理學獎。

1912 年玻爾寄給盧瑟福的“曼徹斯特備忘錄”中關於構造成簡單分子的原子可能的構型圖
1916年,上述物理學理論開始被應用到化學領域。吉爾伯特·牛頓·路易士提出,原子間的強(共價)鍵涉及到原子間共享兩個電子(電子對鍵)。但路易士並未因這一發現獲得諾貝爾化學獎。事實上,他曾41次獲得諾貝爾化學獎提名,但從未真正摘得桂冠,這也成為諾貝爾獎歷史上的巨大爭議之一。

19世紀90年代,在化學與物理交界的地帶,湧現了很多重大發現。
實際上,在最初的十年中,三位諾貝爾化學獎的獲獎者,雅各布斯·亨裏克斯·範托夫,斯萬特·奧古斯特·阿累尼烏斯和威廉·奧斯特瓦爾德,通常被認為是化學的新分支——物理化學的奠基人。
此外,委員會還對化學的另一邊界,展現出極大的開放性和遠見。1907年,生物學家愛德華·比希納因為發現無細胞發酵,被授予了諾貝爾化學獎。

因為化學與物理、生物的密切關係,經常會出現同一名候選人同時獲得化學獎、物理學獎、生理學或醫學獎的提名。
這個問題早在1903年就出現了,當時阿累尼烏斯既被提名了化學獎,也被提名了物理學獎。
化學委員會提議授予他每個獎項的一半,但這個想法被物理學委員會否決了。
由於這種邊界問題,當今的化學委員會與物理學,生理學或醫學委員會需要舉行聯席會議。然而,正如韋斯特格倫所説:“重要的是,那些可以被視為化學、物理和生理和醫學領域的工作,實際上是否值得一個諾貝爾獎。”