多發性骨髓瘤患者在接受細胞治療後出現BCMA基因缺失_風聞
推医汇-汇聚健康行业资讯,推动学术交流。2021-04-29 11:58
B細胞成熟抗原(BCMA)是多種免疫療法的靶點,也是多發性骨髓瘤(MM)的生物標誌物。在最近發表的一項研究中,來自德國維爾茨堡大學的Leo Rasche團隊報道了參與KarMMa臨牀試驗(NCT03361748),並在抗BCMA CAR T細胞療法治療後出現惡化的MM患者中不可逆BCMA丟失的情況,相關結果發表在《Nature Medicine》雜誌上。

(圖片來源:www.nature.com)
在這項研究中,作者對正在進行的KarMMa II期臨牀試驗(NCT03361748)的71歲男性免疫球蛋白G(IgG)-κMM患者的BCMA丟失情況進行了深入分析。磁共振成像(MRI)顯示了患者在接受治療之前位於骨盆和脊柱的多個病灶以及左腋窩區域的EMD。用氟達拉濱和環磷酰胺進行淋巴清除後,向患者體內輸入450×106 CAR + T細胞,患者經歷了I級細胞因子釋放綜合徵。1個月後,M蛋白從4.2μg/dl下降至0.8μg/dl。此外, MRI顯示局灶性病變和EMD完全消失。經過3個月的隨訪,根據國際骨髓瘤工作組的指導方針,M蛋白進一步降低至0.2μg/dl,並且仍未檢出MRD,這與非常好的療後反應相符。
但是,MRI檢測發現一名患者左腋窩區域存在一個大小為0.8 cm的單個淋巴結,懷疑為早期局部復發。CAR-T細胞輸入後五個月,部分患者出現明顯復發,M蛋白水平為3.8 g dl-1,骨髓漿細胞浸潤(BMPC)達到90%,廣泛的EMD影響淋巴結,肝臟和脾臟。細胞動力學分析顯示CAR T細胞的大量擴增,患者在兩週後因難治性疾病死亡。
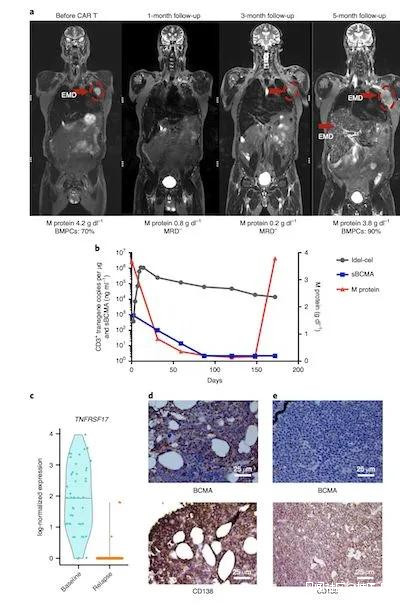
MM患者治療初期到復發後的臨牀特徵
為了闡明抗BCMA CAR T細胞療法復發的潛在機制,作者使用單細胞RNA測序調查了試驗早期和進展後收集的骨髓樣本。結果顯示:TNFRSF17在基線時在骨髓瘤細胞中高水平表達,但在進展時幾乎無法檢測到。使用免疫組織化學在蛋白水平上證實了基因表達結果。其他漿細胞標誌物和潛在的免疫治療靶標,例如CD38和SLAMF7,在進展過程中仍穩定表達。儘管所有出現惡化的細胞均為TNFRSF17隱形,但作者仍注意到這些細胞轉錄組水平的異質性,並將其進一步分為八類,例如高度增殖性細胞(MKI67)或CD27 +細胞。此外,作者注意到與治療初期相比,復發時骨髓浸潤性T細胞中的耗竭標誌物表達增加。
進一步,作者研究了導致TNFRSF17基因表達完全喪失的分子機制,對此,作者對疾病進展過程中的MM細胞進行了全基因組測序(WGS),進而揭示了許多基因組畸變,包括1q擴增,1p缺失,TP53的雙等位基因失活和p53的雙等位基因失活。複雜的IGH-MYC重排等。研究結果表明:16號染色體存在21.3 2megabases(Mb)的雜合性缺失和91 kilobases(kb)的純合缺失,導致TNFRSF17基因在16p13.13丟失雙等位基因。這些數據表明在CAR T細胞治療後觀察到的BCMA-進展的基因組機制。
綜上,作者確定了TNFRSF17(BCMA)純合缺失的克隆的選擇作為免疫逃逸的潛在機制。此外,作者還在168例MM患者中的37例中發現了雜合性TNFRSF17缺失,在33例先前未接受過BCMA靶向治療的高單倍體MM患者中存在28例,這表明:從理論上講,雜合性TNFRSF17缺失可能是免疫治療後BCMA抗原丟失的危險因素。
原始出處:Da Vià, M.C., Dietrich, O., Truger, M. et al. Homozygous BCMA gene deletion in response to anti-BCMA CAR T cells in a patient with multiple myeloma. Nat Med 27, 616–619 (2021). https://doi.org/10.1038/s41591-021-01245-5