“基因編輯嬰兒”醜聞曝光兩年後,WHO終於出手了_風聞
推医汇-汇聚健康行业资讯,推动学术交流。2021-07-26 18:12
2021年7月12日,世界衞生組織(WHO)下屬專家委員會發布《人類基因組編輯管治框架》和《人類基因組編輯建議》,首次提出了將人類基因組編輯作為公共衞生工具的全球建議,並論證了其安全性、有效性和倫理。
 WHO
WHO
人類基因組編輯技術(Human Genome Editing)能夠讓人類對目標基因進行“編輯”,科學家能夠通過改變DNA,就像剪刀一樣,在特定位置切割DNA,也可以移除、添加或替換被切割的DNA,進行基因編輯,從而改變身體特徵,如眼睛顏色和疾病風險,在治療某些遺傳性疾病時具有無可比擬的優勢。
基因編輯,可分為體細胞基因編輯(不可遺傳)和種系基因編輯(可遺傳的)。當前,各界對體細胞基因編輯普遍持支持態度,因為這種改變只會影響自身健康,而不會影響到後代以及種系基因組。
2018年11月,第二人類基因組編輯國際峯會上,與會人員普遍認為體細胞基因編輯對治療血友病、艾滋病、癌症、阿爾茨海默病等顯著有益。
人類基因組編輯的潛在好處包括更快和更準確的診斷,更有針對性的治療和預防遺傳疾病。體細胞基因療法涉及修改患者的DNA以治療或治癒疾病,已成功用於治療艾滋病毒、鐮狀細胞病和甲狀腺素運載蛋白澱粉樣變性。這項技術還可以極大地改善多種癌症的治療。
與其他基因編輯技術相比,2009年發明的CRISPR/Cas9技術更易於操作擴展性也更強,更簡單、更快、更便宜且更準確,因此迅速成為了科研領域的寵兒。
就在上個月,6月26日,NEJM發表了首個人體內CRISPR基因編輯治療 I 期臨牀試驗結果,療法安全有效。在研CRISPR體內基因組編輯療法NTLA-2001在1期臨牀試驗中獲得積極結果,這是首個支持體內CRISPR基因編輯安全性和效果的臨牀數據,是基因編輯技術中一個里程碑式的事件。

可以説,基因編輯技術在推動很多疾病治療方面卓有成效。2015年,倫敦大學學院的研究人員對英國一歲的Layla進行基因編輯治療,採用體細胞基因療法幫助她成功對抗白血病,成為世界上首個接受基因工程免疫細胞治療的病例。
科學家採用的是一種稱為 TALENs 的基因組編輯技術。在此之前,研究人員發現經過修飾的細胞具有抗癌作用,但僅在患有白血病的小鼠身上進行了測試。最終,醫生嘗試了很多治療方法,只有這種療法挽救了Layla的生命。
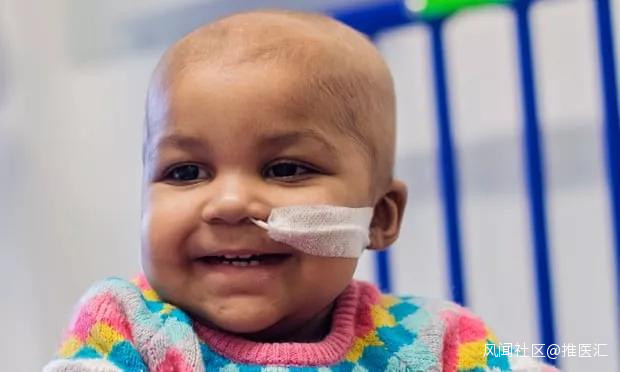 來源:theguardia
來源:theguardia
接受了基因工程免疫細胞治療的侵襲性白血病患兒Layla Richards
像 Layla 接受的那種治療仍然是實驗性的,因為科學界和政策制定者仍然必須解決圍繞基因組編輯的技術障礙和倫理問題。
基因編輯存在一些風險,例如,種系和可遺傳的人類基因組編輯會改變人類胚胎的基因組,並可能傳遞給後代,從而改變後代的特徵。
目前開展的基因治療試驗屬於體細胞基因編輯,2018年震驚世界的基因編輯嬰兒事件則屬於種系基因編輯。相比於體細胞基因編輯,種系基因編輯極具爭議,因為它會導致一系列生物倫理問題。
基因編輯技術為大眾所熟知也是在2018年,時任中國南方科技大學副教授的賀建奎,他的團隊通過基因編輯技術,對一對雙胞胎嬰兒胚胎細胞的基因進行了改造,產下一對具備先天艾滋病免疫能力的“健康”雙胞胎。
此舉在國際社會引起軒然大波,人們普遍對其中所涉及的倫理和醫學所產生的嚴重負面後果表示極大擔憂。
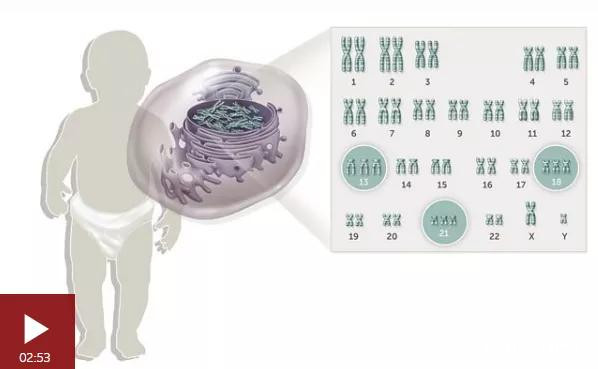 人體基因編輯示意圖 來源:BBC截圖
人體基因編輯示意圖 來源:BBC截圖
最終,於2019年12月30日,深圳市南山區法院一審宣判,裁定被告人賀建奎等人因共同非法實施以生殖為目的的人類胚胎基因編輯和生殖醫療活動,構成非法行醫罪。法院判處賀建奎有期徒刑三年,罰款人民幣300萬元。
中國科學院生物與化學交叉研究中心研究員陳椰林曾表示,賀建奎的實驗引起巨大爭議的原因,是CRISPR技術的“脱靶效應”很明顯(脱靶效應是指未能達到預先設定的目標,有所偏移的現象),導致實驗風險巨大。
CRISPR基因編輯技術開發者之一,美國加利福尼亞大學伯克利分校教授詹妮弗·杜德納(Prof Jennifer Doudna)親自到香港聽取賀建奎的説法後也大表不安,覺得其技術遭賀建奎“玩弄”。由此,國際上要求對基因編輯工作進行全球治理和監管的呼聲日漸強烈。
基因編輯技術原本是一件利器,用得其所可以為很多病患帶來希望,但絕不是可以隨意“玩弄”的技術。
事實上,早在2015年12月舉行的第一屆人類基因組編輯國際峯會上,各國學者就已達成共識:除非安全性、有效性問題已得到解決,除非社會認可,否則不得進行任何基因編輯嬰兒的臨牀應用。賀建奎的做法顯然違背了上述宗旨,為針對人類基因編輯研究的監管提出了挑戰。
此次WHO發佈的報告就九個獨立領域的人類基因組編輯的治理和監督提出了建議,包括人類基因組編輯註冊;國際研究和醫療旅行;非法、未註冊、不道德或不安全的研究;知識產權;以及教育、參與和賦權。這些建議側重於在所有國家建設能力所需的系統層面改進,以確保人類基因組編輯被安全、有效和合乎道德地使用。
這些報告還提供了一個新的治理框架,確定了具體的工具、機構和場景,以説明在實施、監管和監督人類基因組研究方面的實際挑戰。
自2018年的“基因編輯嬰兒”事件以來,圍繞着基因編輯的討論不絕於耳。這項技術的突破,同時也讓大家充滿了期待與擔憂。
基因編輯是劃時代技術,是魔剪,但這個是魔是惡魔,還是祛除惡魔,就看人類往哪裏走了,無論怎麼説,基因編輯都是面向未來的技術,也許有一天,我們會在路上發現很多具有超能力的基因編輯人,也許並不奇怪。
參考資料:
1.CRISPR gene editing in human embryos wreaks chromosomal mayhem.Nature 583, 17-18 (2020).DOI:10.1038/d41586-020-01906-4
2.Quest to use CRISPR against disease gains ground.Nature 577, 156 (2020).DOI:10.1038/d41586-019-03919-0
3.CRISPR-Cas9 In Vivo Gene Editing for Transthyretin Amyloidosis.NEJM.June 26, 2021
DOI: 10.1056/NEJMoa2107454
4.https://www.who.int/publications/i/item/9789240030404
5.https://www.who.int/publications/i/item/9789240030060
6.https://news.un.org/zh/story/2019/11/1045341
7.https://www.who.int/zh/news/item/12-07-2021-who-issues-new-recommendations-on-human-genome-editing-for-the-advancement-of-public-health
8.https://www.genome.gov/about-genomics/policy-issues/what-is-Genome-Editing
9.http://www.siis.org.cn/Research/Info/4687
10.https://www.timedoo.com/5845.html