安全性和有效性數據不夠?美國第3針要推遲!白宮和聯邦衞生官員再現爭端_風聞
大眼联盟-2021-09-05 22:50
繼美國食藥監局FDA多位高級官員因在加強針方面存在分歧而離職後,美國聯邦政府與其衞生官員之間針對新冠疫苗加強針的問題再現爭端。
據多家媒體援引知情人士稱,美國疾病控制與預防中心(CDC)主任Rochelle Walensky和美國食品藥品管理局(FDA)代理局長Janet Woodcock週四告知白宮聯絡官員,建議暫時縮減新冠疫苗加強針在全國範圍內接種的計劃,因需要更多時間來收集、評估有關安全性和有效性的數據。

這可能代表,大部分美國人將無法按照白宮的原計劃,從9月20日當週開始注射新冠疫苗加強針。
FDA週五表示,將要求莫德納公司就新冠加強針上市申請提交更多有力數據,審核過程會排在審核輝瑞加強針的數週之後,目前沒有足夠多的數據為任何人推薦接種加強針。
白宮隨即回應稱,正在等待FDA對新冠疫苗加強針的全面審查和批准,以及CDC專家小組的相關建議。一旦獲得批准和建議,將準備好實施遵循科學的加強針計劃,有助於更快遏制疫情傳播。
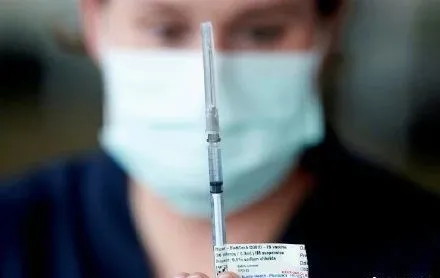 上述報道援引一位官員稱,對輝瑞/BioNTech新冠疫苗的加強針接種仍在按計劃推進,如果真的在9月20日當週開始接種,也可能需要僅限於高風險人羣,例如養老院居民、醫護人員和65歲以上的人。
上述報道援引一位官員稱,對輝瑞/BioNTech新冠疫苗的加強針接種仍在按計劃推進,如果真的在9月20日當週開始接種,也可能需要僅限於高風險人羣,例如養老院居民、醫護人員和65歲以上的人。
與此同時,兩家聯邦機構最早在10月才能對Moderna和強生疫苗的加強針給出建議。
據悉,FDA的顧問團隊將於9月17日開會討論兩個關鍵問題,以考慮是否在今年秋天開展新冠疫苗加強針推廣活動,第一個問題是初始疫苗的保護力是否減弱,第二個是加強針能否有所幫助。當天會議重點是輝瑞疫苗,也不排除討論其他議題。
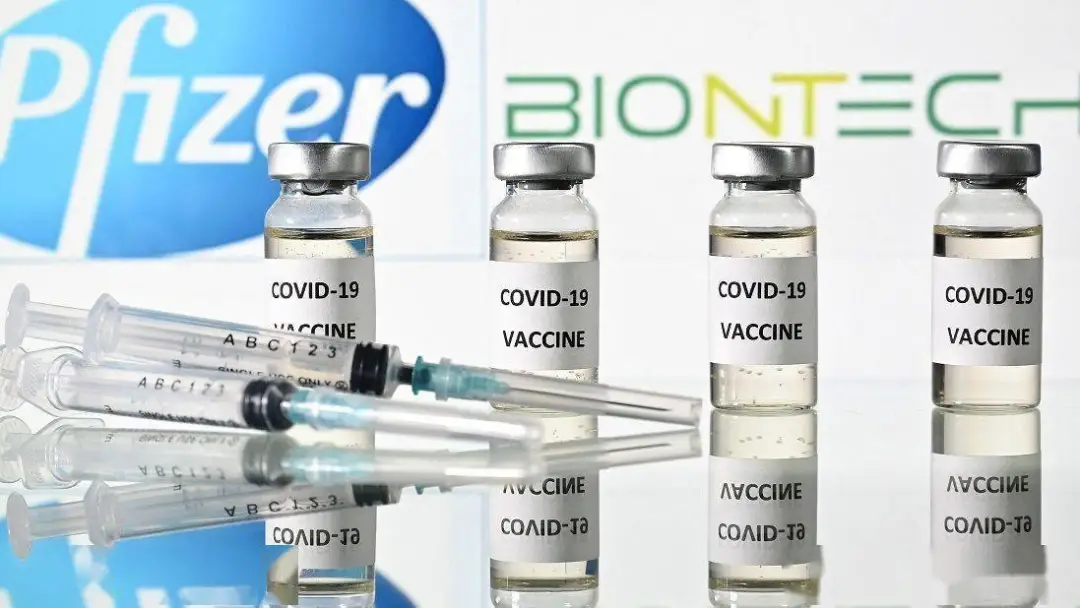 知情人士稱,白宮與聯邦衞生官員們的分歧存在於幾大方面。首先是莫德納疫苗的加強針應該是50微克劑量還是前兩次注射使用的100微克劑量。
知情人士稱,白宮與聯邦衞生官員們的分歧存在於幾大方面。首先是莫德納疫苗的加強針應該是50微克劑量還是前兩次注射使用的100微克劑量。
莫德納公司提倡使用50微克,而一些政府官員出於對耐用性的不確定而支持繼續使用100微克。此外,專家們還試圖確定單劑量的強生疫苗與加強針之間正確間隔時長是多久。
據CDC統計,美國目前有9460萬人完成了輝瑞新冠疫苗的兩針注射,6580萬人完全接種了莫德納疫苗,另有1420萬人接種了強生疫苗。
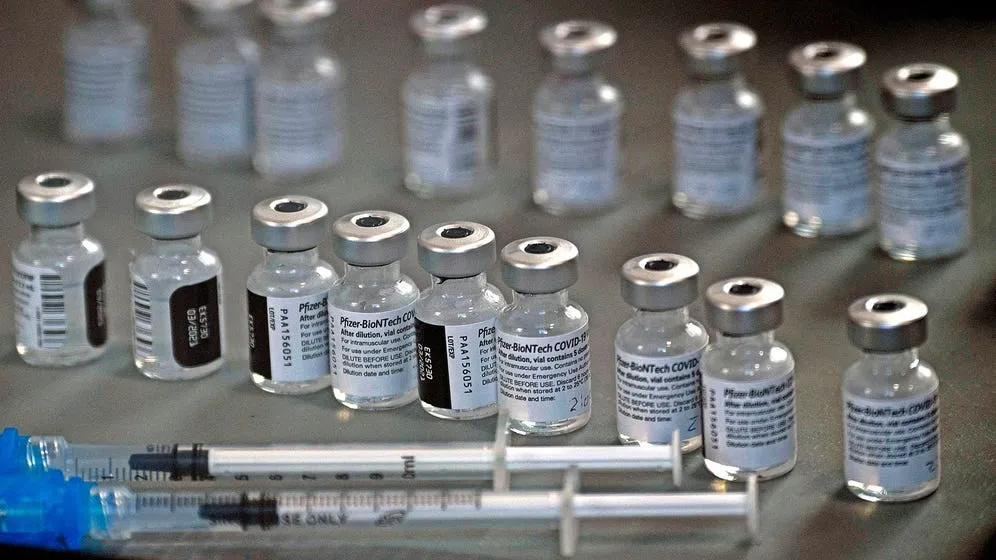
今年8月13日獲得特殊批准以來,約有95.5萬人接種了輝瑞和Moderna的新冠疫苗加強針,他們主要是免疫功能低下或有缺陷的病患。
8月24日,美國疾病預防與控制中心的一項針對疫苗有效性的研究結果提前發佈在其網絡版MMWR網站上。
該研究對美國6個州8個測試點的首次接種了mRNA新冠疫苗的醫護人員、救護人員和其他數千名一線工人進行每週一次的測試,並在出現新冠感染後立即進行測試,使研究人員能夠估計疫苗對有症狀和無症狀感染的影響。

研究發現,在2020年12月14日至2021年4月10日期間,輝瑞和莫德納新冠疫苗在預防有症狀的感染方面的有效性約為91%。
而當傳染性較強的Delta變種病毒佔據主導地位時(佔病毒序列的50%以上),這兩種疫苗的有效性下降到66%。
在研究中,4217名參與者有3483人(83%)接種了疫苗:2278人(65%)接種了輝瑞-疫苗,1138人(33%)接種了莫德納疫苗和,67人(2%)接種了強生疫苗。488名受試者未接種疫苗。

研究人員解釋説,疫苗有效性下降的原因可能有多種解釋,包括疫苗的保護作用可能隨着時間的推移而減弱。66%的估計是基於一個相對較短的研究期。
研究人員認為,雖然這些中期發現表明輝瑞-BioNTech和Moderna mRNA新冠疫苗在預防感染方面的有效性有所降低,但感染風險持續降低了三分之二。
同時,今年早些時候,一項美國疾病預防與控制中心在洛杉磯的研究表明,未接種疫苗的人患新冠住院的風險大約是接種疫苗者的29倍。
來源:綜合華爾街見聞、21世紀經濟報道