做到超500億淨利潤要多久?科興答:6個月_風聞
锐公司-中文财经期刊《商界》官方账号-全球发行量最大的中文财经期刊之一《商界》旗下平台2021-09-17 10:14
鋭公司(ID:shangjiezz)報道
作者/ 崔小花
編輯/ 周春林
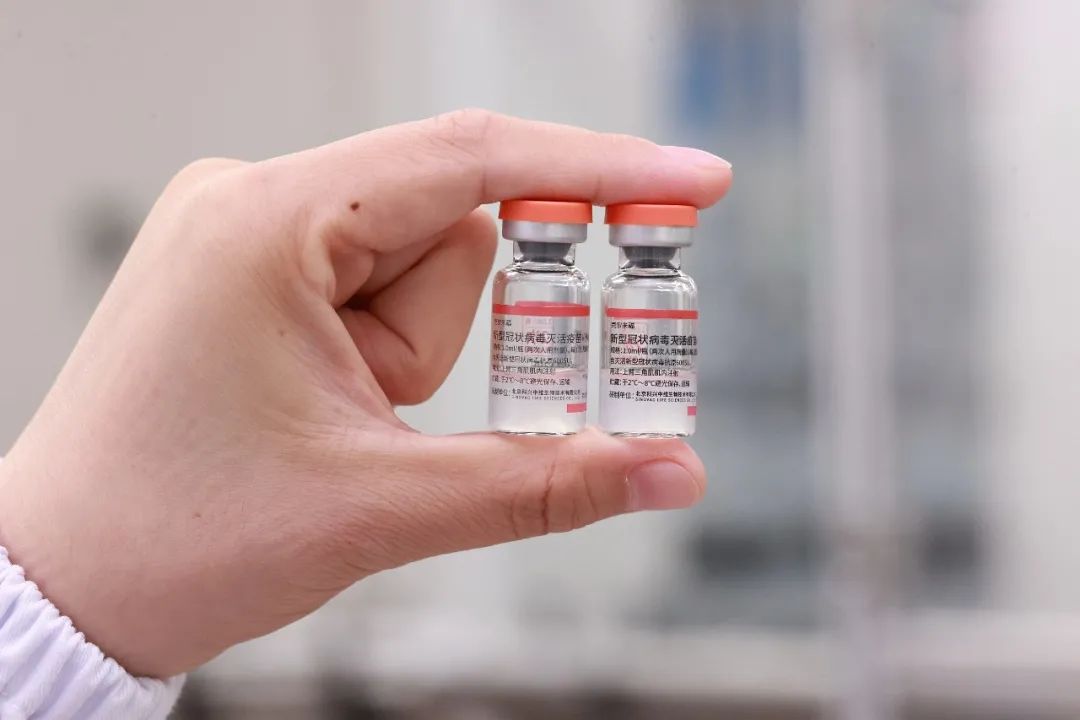
圖片/ 視覺中國
近日,中國生物製藥發佈公告:今年上半年,中國生物製藥歸屬於母公司持有者盈利84.8億元,同比增長583.6%,而其中參股公司就貢獻了75.85億元。而在去年同期的財報中,這一項是負4000萬元,2019年也只有700萬元,那麼今年的高速增長源自哪裏?
中國生物製藥最近一筆大規模投資是2020年12月,以5.15億美元拿到科興中維15.3%股權。據此,業內人士推測做滅活新冠疫苗的科興,今年上半年疫苗銷售淨利潤可能超過500億元。
500億元淨利潤是一個怎樣的概念?
從全球範圍來看,上半年利潤超過500億的藥企還有兩家:分別是強生和輝瑞。
500億元佔了2020年整個中國醫藥行業GDP的2.5%,相當於醫藥大龍頭企業恆瑞醫藥過去十年利潤的總和,相當於0.5個A股醫藥板。
如果要用一個更加聳人聽聞的對比:500億在2021年中國城市的財政收入中能夠排進前20名,超過西安、東莞、瀋陽等大城市。
而科興作為一家疫苗企業,僅用6個月就做到了。
天意弄人
很多人説科興是憑着新冠疫苗一戰成名,大概有點低估了這家企業。
這家多少有點“時運不濟”的企業,從研製我國第一支甲肝滅活疫苗開始,到第一支甲乙肝聯合疫苗,再到與全球同步的大流行流感疫苗,一直都戰鬥在防疫的第一線。然而留在人們記憶裏的卻是那三次“天意弄人”的“緊急研發”。
上世紀80年代中國甲肝疫情爆發,那時的科興董事長尹衞東還只是一名基層的流行病醫生,主要工作就是甲肝防治研究。相比於其他出身正統的民營疫苗公司,這個出身多少帶了點草莽氣息。
説起中國的疫苗產業,六大生物製品研究所是個逃不開的話題。
所謂六大所,即北京、成都、長春、武漢、蘭州以及上海生物製品研究所,是新中國成立以後,在國家統籌協調下建起的各地方級疫苗研究機構,一直是中國疾控的中堅力量,為國家培養了一大批生物製藥領域的人才。
改革開放後,大江南北春潮湧動,六大所培養的人才也紛紛投入改革的浪潮:華蘭生物、智飛生物、康華生物、沃森生物等根紅苗正的疫苗企業都有這六大所的影子。
1992年,在新中國的商業史上是至關重要的一年。鄧小平第二次南巡講話後,中國湧現出了一大批踏實勤懇的民營企業家。尹衞東也在這一年開啓了自己的創業生涯。雖然沒有六大所的出身背景,但後來他也獲得了北大未名生物工程集團的支持,實現了甲肝疫苗的批量生產,打破了國外生物醫藥巨頭對於這個市場的壟斷。
2003年非典疫情爆發之後,科興憑藉高度的市場敏鋭度,成為最早參與SARS疫苗研發的企業之一。在經過8個月艱苦卓絕的技術攻關後,科興率先完成了第一期臨牀試驗。就在這個關鍵階段,最後一個非典病人治癒出院,SARS疫情結束,疫苗二期臨牀試驗還沒開始就結束了。
這一次的研發,科興不僅顆粒無收,並且為此停掉了成品疫苗生產線,成了一筆妥妥的“賠本生意“。
2009年H1N1流感和2013年H7N9高致病性禽流感相繼在國內出現,科興拿到分離毒株,並將滅活疫苗推進到了三期臨牀試驗。但歷史總是驚人的相似,疫苗研發出來了,疫情也過去了。
這三次有功無果的研發,讓科興成為了業內人士常常調侃的“倒黴蛋兒”。
一戰成名
經歷了SARS疫苗和禽流感疫苗產品研發出來了,卻沒了用武之地的尷尬,科興雖然沒有得到真金白銀的收益,但那兩次“戰疫”中積累的對突發疫情的應對經驗,在這次新冠疫苗的研發中發揮了重要作用。
2020年的春節,對於中國來説是悲情的,尤其是江城武漢。除夕前夜,武漢封城。
而就在封城的前三天,科興負責研發的副總親自帶着新冠病毒毒株回到了北京。一場與時間的賽跑開始了。
晚上8點毒株被送進實驗室進行純化等工作,8小時後樣本出爐,8天后動物試驗,4月中旬獲批一期臨牀試驗……
幾乎與科興同步,中國疫苗企業向着5種技術路線同時進軍,向攻克新冠病毒發起了總攻。
2020年3月15日,康希諾生物與軍科院陳薇團隊合作研發的腺病毒載體新冠疫苗進入一期臨牀試驗;4月12日,國藥中生武生所的新冠滅活疫苗進入一期臨牀試驗;6月19日,智飛生物與中科院微生物研究所聯合研發的重組新冠疫苗也獲批進入一期臨牀試驗……
單從時間上來看,沒有佔到先發優勢的科興能夠後發制人,除了與之前研發SARS和禽流感疫苗積累的經驗有關,也與這次新冠疫情全球大流行造成的特殊局勢有關。
科興的收益,除了源自國內疫苗的高接種率,更來自大量的出口訂單。
2021年上半年,中國已經向100多個國際和國際組織提供了超過5億劑的疫苗和原液,這相當於全球新冠疫苗總產量的六分之一,出口量是歐洲疫苗出口量的227%,是美國疫苗出口量的84倍。
科興生產的新冠滅活疫苗,在2021年上半年被世界衞生組織WHO列入緊急使用清單,同時被列入清單的除了中國的兩款滅活疫苗,還有美國的兩款mRNA疫苗。本來美國的疫苗應該更具有國際競爭力,然而美國前政府和WHO矛盾不斷,甚至在7月6日宣佈退出WHO。 而WHO寄予厚望的印度,在疫苗研發上卻遲遲沒有突破。
最終,中國接住了這份幸運,科興接住了這份幸運,一戰定江山。
“幸運”不可複製
提起生物製藥產業,人們最容易想到的就是它所謂“三高一長”的特性,即:高投入、高技術、高風險和長週期。僅僅在兩三年前,這個高入門門檻、高行業天花板的產業還是許多資本不願觸碰的領域,而如今一旦沾上“新冠疫苗”的概念,企業估值和融資立馬就能上去。
比如在剛剛過去的8月,國內生物醫藥領域就迎來了最大一筆投融資事件。艾博生物僅依靠兩款與沃森合作的mRNA疫苗作為核心賣點展示便狂吸7億美元(約45.36億元人民幣)C輪融資,刷新了中國生物醫藥公司IPO前單筆融資紀錄。
新冠病毒疫苗,讓投資人見識了創新藥方向的崛起有多快。最近,除了復星醫藥的mRNA疫苗在等待獲批外、兩家mRNA疫苗在進行三期和一期臨牀試驗外,至少還有20家企業扎堆進入新冠疫苗的賽道。
然而,科興的“幸運”是可以複製的嗎?
8月23日,美國FDA首次全面批准了輝瑞的新冠疫苗,使其成為了全世界第一個被正式批准的新冠疫苗。這是一個重要的信號,預示着新冠疫苗這條賽道下半場的遊戲規則變了。
此前,包括輝瑞在內的新冠疫苗都是“緊急使用”狀態,而“緊急獲批”狀態下,只能由政府牽頭購買。
也就是説,科興的新冠疫苗在海外大賣,是在EUA(緊急使用授權)模式下進出口,是由各國政府組織,在獲得進口國政府批准使用後,通過商業協議給各國提供疫苗。
而FDA完全批准了輝瑞疫苗,就意味着輝瑞可以通過正常的出口方式,在每個國家申請進口註冊,然後由當地代理商進口銷售,並且當地政府和醫院也可以直接和代理商採購。這樣一來,整個國際疫苗市場的遊戲規則就發生了本質的變化。
新冠疫情依舊在全球範圍內蔓延,全世界疫苗缺口依然巨大。
然而對於一戰成名天下知的科興和中國生物製藥行業來説,如何用實力將這份“幸運”繼續下去,才是今後需要更多思考的問題。