我們學的化學就這?_風聞
中科院物理所-中科院物理所官方账号-2021-10-19 14:01
原創:中科院物理所
如果只從標準教科書或高中課程中學習化學,很容易一葉障目不見泰山。
當同齡人剛開始用五顏六色的液體搗鼓有趣的化學實驗的時候,十幾歲的我就已經非常熱愛化學這門學科了。當然,所有的孩子都想搞一些能爆炸的東西玩。化學對孩子們有一種天然的吸引力,因為它自帶爆炸、閃光、氣泡以及五彩斑斕的顏色,並且總能用到酷酷的、形狀複雜奇特的玻璃器皿。
此外,我也碰巧是一個歷史愛好者。有時讀到有關金屬加工的古老歷史,或原子能、太陽能電池半導體等更現代的東西時,很難看出它們之間的共同點——因為學校裏教的化學並沒有那麼“接地氣”。這便是此文要做的事情。
混合與分離
簡單來説,應用化學就是混合和分離。我們周圍的世界充滿了不同的元素,但它們通常以我們不想要的方式出現。比如説岩石富含鋁、硅和鐵,但它們結合在礦物裏,沒法直接用。
因此,在實踐中,化學就是把我們需要的物質從無用的東西中分離出來。這樣的途徑紛繁複雜,以至於我們很容易忽略全局,沒有意識到這只是分離兩種或多種化合物的另一種形式。
下面,就讓我們在不同的例子中,更好地瞭解分離和提純化合物的所有方法。
總體思路
在討論細節之前,讓我概述一下總體思路。
把混合在一起的兩個元素分開,有很多有創意的方法。例如,如果一個有磁性而另一個沒磁性,可以用磁鐵;如果一個在加熱時變成氣體,而另一個不變成氣體,則很容易將氣體和固體分離;或者一種化合物比另一種密度大得多,就可以使用人工重力(離心偽力)進行分離,比如使用離心機。
但是如果這些元素是以化學方式結合的,那怎麼把它們分開呢?假設你有原子 X 和 Y ,它們被束縛成化合物 XY 。
加熱通常會使化合物分解。X 元素和 Y 元素從化合物狀態分離開來,但它們仍然混在一起。解決方案通常是加入第三個元素 Z 。如果 Z 可以與 Y 形成比 X 更牢固的鍵,那麼 Y 和 Z 將結合在一起形成 YZ ,這時 X 元素可以被單獨保留。
**化學鍵的強度決定了你需要加熱到什麼程度來將其破壞。**因此,如果加熱到足夠分解 XY ,但不足以分解 YZ 的温度,那麼你能夠逐漸提純出元素 X 。
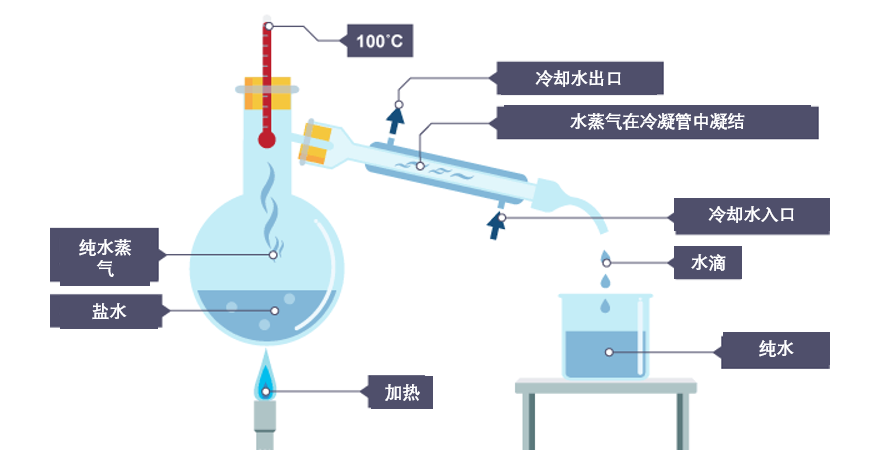
使用温度計,你可以確保温度保持在一個固定值,在這一温度,只有一種特定的化合物變成氣體,而其餘的保持液態或固態。
蒸餾-按物相分離
水中可能混有一些我們不想要的雜質化合物,通過蒸餾的方式可以得到乾淨的水。蒸餾利用的是一種常見的分離技術,即根據不同的相,分離兩種化合物。三種常見相分別是固體、液體和氣體。不同相的化合物更容易分離。
將水加熱到 100°C 以上時,它會從液體變為氣體(水蒸氣)。這時,水從與之混合的東西中分離出來。把水蒸氣引到別處並冷卻,就能得到乾淨的水。我們將水分離了出來,可能剩下某種固體,比如説鹽(由氣體和金屬組成的化合物)。
生產酒精時的做法正好相反。酒精的生產常常伴有水的參與。生產中用酵母和糖最高能得到濃度為 14% 的酒精,那如何讓這個數字變得更高呢?
酒精的沸點比水低。因此,如果將温度保持在 100°C 以下,則只有酒精蒸發。然後將其冷卻以回收濃縮酒精。如果不夠純淨的話,原則上只要重複這個過程就可以了。
冶煉
鐵礦石和銅礦石不只含純金屬,通常以 Fe₃O₄ 和 Fe₂O₃ 的方式存在,其中含有我們不需要的氧。很多情況下岩石裏面混雜着根本不含鐵的礦物,我們就可以粉碎岩石,並按重量分離——重的石頭更有可能含有鐵化合物。
然而,在化合物中分離氧和鐵還需要化學的手段。這時“冶煉”就出場了。任何化合物被加熱時,只要有足夠的熱量,將它們結合在一起的化學鍵就會斷裂。因此,當我們加熱鐵礦物時,我們會得到鐵氧分離的一鍋“熱湯”。
我們不期望的是,一旦“原子湯”冷卻下來,它們就會再次結合在一起。解決辦法是添加一些與氧的結合力更強的物質。例如,氧和碳成鍵生成二氧化碳(CO₂),這一化學鍵非常強,意味着將原子分開將需要大量的熱量。
發現與蒸餾的類同之處了嗎?高温能將部分化合物轉化為氣體。在熔爐中,温度可能足以分解鐵原子和氧原子,但不足以使氧原子和碳原子彼此分離。
因此,當我們通過高温將鐵、氧和碳“燴成一鍋湯”時,碳和氧會結合在一起,再也不會分離。我們現在可以像蒸餾一樣去除碳和氧,因為二氧化碳是氣體,而鐵是液體。
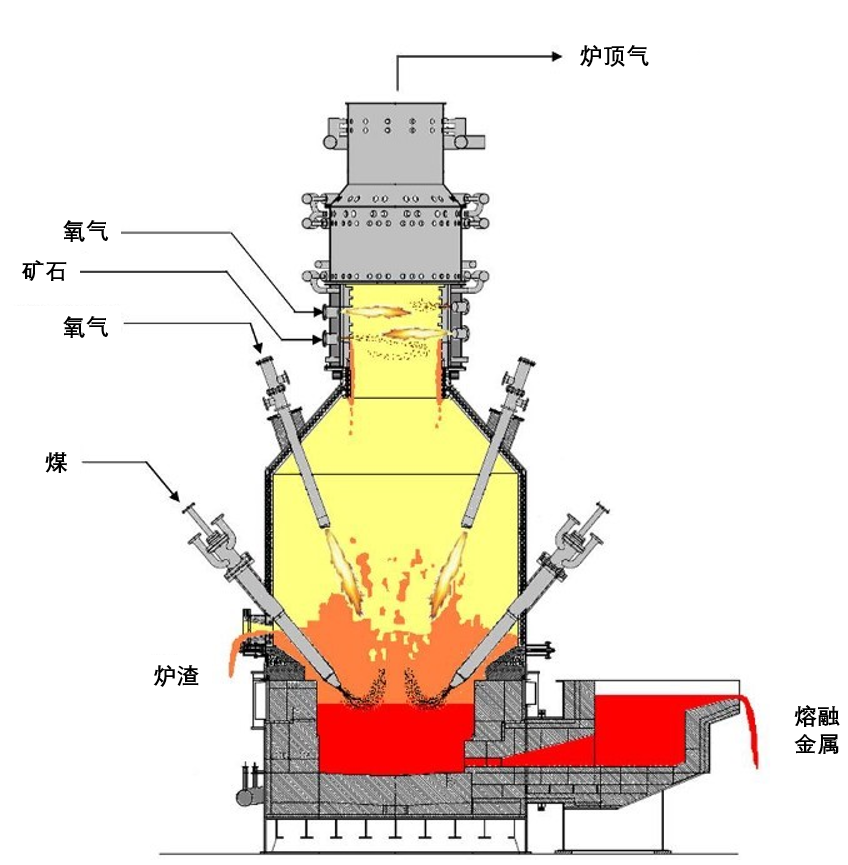
爐渣和金屬就像油和水一樣分層,於是我們很容易就可以將他們分開。爐渣是所有我們不想要的東西的混合物——雜質。
還有另一種形式的分離。你知道油和水是如何分層的嗎?鐵和爐渣也會發生這種情況。爐渣是鐵礦石中我們不需要的所有其他化合物的總稱。我們將碳酸鈣(CaCO₃)扔進去,讓它與鐵礦中我們不需要的二氧化硅(SiO₂)反應,會產生浮在純鐵之上的爐渣,我們稱之為相分離。然後可以將爐渣倒出;因為它比鐵更脆,我們還可以像鐵匠一樣把它敲下來。
即使沒有化學反應,熔鍊也可以用於分離。就像蒸餾一樣,不同的化合物加熱時的反應不同:爐渣通常比氧化鐵更易熔化。因此,如果有足夠的熱量,爐渣會融化並在底部聚集,而氧化鐵則以固體的形式留在頂部。添加一些輔助物質可以也促進這一過程,通常是可以降低爐渣熔點的石灰石(碳酸鈣)碎塊,使其更易熔化。
離心
離心機可以看做是一個飛速旋轉的圓筒,其中最重的化合物被推到底部,以便移除。這是另一種機械分離的形式。
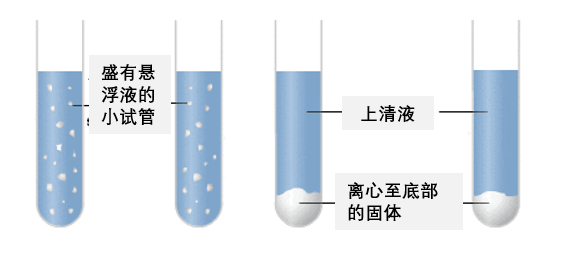
用離心機將固體或較重的元素甩向底部,使其更容易分離。
離心機在核科學中非常重要。
因為質子數相同,鈾的各個同位素具有相同的化學性質,沒法用化學方法分離開。中子的數量決定了它們在核反應中的性質,不同中子數的鈾同位素,具有非常微小的重量差別。
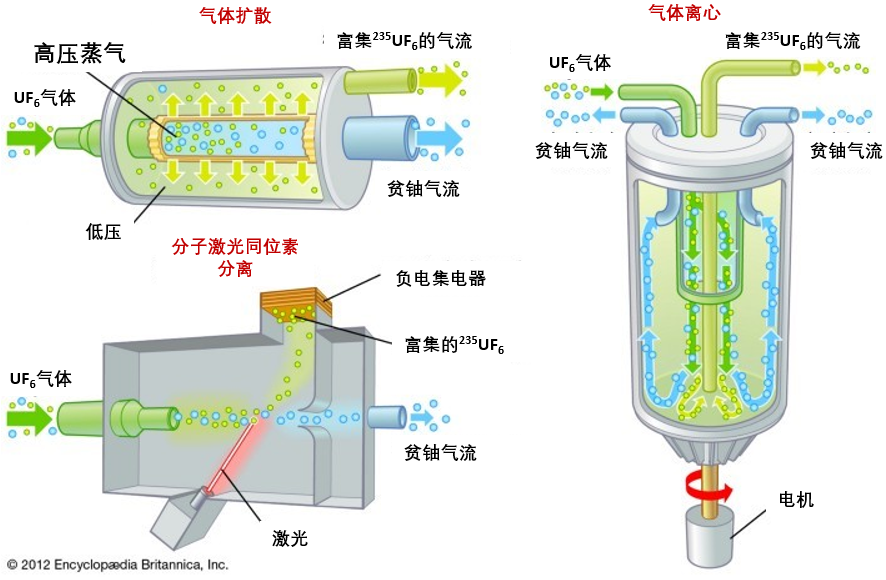
為了更方便提純,利用鈾原料與氟氣反應生成六氟化鈾( UF₆):以氣體形式存在的分子相對容易移動。但是由於質量的差別很小,必須增加離心機的轉速,使較重的氣體聚集起來。
就像許多分離過程一樣,這些操作必須一次又一次地重複。提取出的較重氣體並不是完全純淨的,因此需要把它們放入新的離心機,重複離心過程,才會得到我們需要的越來越高濃度的鈾同位素。
固液氣分離
製造太陽能電池板需要非常純的硅,而常規的冶煉操作無法提供足夠的純度。我們可以參考蒸餾的技巧,以某種方式把我們想要的或不想要的物質轉化為氣體,剩下固體或液體。
通過一些步驟,我們可以將硅 (Si) 轉化為硅烷 (SiH₄) 氣體。其他雜質不一定會在這個過程中變成氣體,我們得以將硅從其他雜質中分離出來。
當然,之後我們需要將混合物中的氫去除掉,這種化合物會在高温下裂解,氫可以被燃燒掉。
浸出
將礦物溶解在酸或其他液體中,可以將其中不同的化合物分離開來。我們想要的化合物可能會溶解,而不感興趣的物質會落到底部被過濾掉。
這就是一些像鈾這種物質的加工方法。我們可以使用浸出法從鈾礦中生產低純度的鈾,俗稱“ 黃餅” (yellow cake)。
雖然具體過程不完全相同,但這與從沙子中分離鹽有一些相似之處。鹽會溶於水,沙子不溶解,只會沉入水底。這樣你就可以過濾掉沙子,然後通過蒸餾來回收鹽。
粉末化、混合和漿料
關於將物質分離,我們已經談了很多,但有時為了分離,首先要混合。例如,如果礦物是大塊固體,那麼它在酸中就會溶解得很慢;再比如鍊鐵時需要石灰石中的碳酸鈣與儘可能多的礦石發生反應。
別忘了,**化學反應只有在原子相互接觸、發生相互作用時才能發生。**內部的岩石不能與外部的酸直接反應,只有岩石表面才可以。
汽油在內燃機中劇烈燃燒也是這個道理。只有液滴表面的汽油分子才可以與氧結合,產生熱量。因此,汽車發動機中的化油器的任務,就是製造霧狀的氧。大量的微小液滴比少數的大液滴具有更大的表面積,為迅速反應提供了機會,從而引發爆炸。就像碎石的表面積比大卵石大一樣,製造火藥時我們也需要將原料磨成粉末,獲得更大的接觸面積來相互反應,創造許多並行反應來引發爆炸。
於是在化學反應中經常會用到漿料(類似泥漿的固液混合物)——粉末與液體充分混合,能夠讓化學反應更容易發生。
如何讓氣體與固體發生反應?只是向一塊石頭噴射某種氣體可沒啥用。
塑料也被稱之為聚合物,塑料的生產就是將相對簡單的分子鏈連接成較長的分子鏈。
將乙烯(C₂H₄) 氣體鼓進通過裝有齊格勒-納塔(Ziegler-Natta)催化劑及其溶劑的容器,乙烯分子可以結合成一條長鏈。你得到了想要的化合物——聚乙烯(一種塑料聚合物),但隨之而來的是混在其中的許多雜質。
因此,接下來等着你的是分離、過濾、溶解、乾燥等一系列步驟。
將分離步驟和混合步驟結合
在實際的化學過程中,**我們很少僅在一個混合步驟或一個分離步驟後,就能得到想要的東西。**無論你使用蒸餾、浸出、熔鍊、過濾、離心還是化學反應,你更容易得到一些不需要的化學物質。要想只留下想要的物質,需要使用許多不同的分離步驟。
複雜之處就在於,通常執行一種特定的分離操作需要先進行某種混合。因此,生產任何東西實際上都是不斷地進行各種各樣的分分合合。
結論
化學過程看起來千頭萬緒、難以理解,但它們基本上都是混合與分離,只是用到的工藝方法不同。一個宏觀上看起來是分離的操作,其實可能是很多細小的混合和分離步驟的總和,而這些小步驟甚至還可以做進一步細分。
讀罷此文,無論是金屬冶煉、釀造、煉油還是聚合(塑料生產),利用上述的框架,您都能對所涉及的化學過程有一個更好的瞭解。
作者:Erik Engheim
翻譯:xux
審校:zhenni
原文鏈接:https://erik-engheim.medium.com/what-they-didnt-teach-you-about-chemistry-e15ac552a0de