陳根:首例豬腎臟移植宣告成功,異種移植未來已來?_風聞
陈根-知名科技作家为你解读科技与生活的方方面面。2021-10-24 07:41
文/陳根
10月19日,世界首例豬腎臟移植人體手術宣告成功,震動全球。實驗成果來自美國紐約大學朗格尼醫學中心移植外科Montgomery教授團隊。
實驗當日,Montgomery教授團隊用手術夾鉗將患者的血液與豬的腎臟分隔,一旦他們鬆開夾鉗,血液就會注入這個新器官**——**Montgomery為這一時刻已經準備了三年。在最壞的情況下,新腎臟將迅速變成藍色,表明免疫系統出現了排斥反應。同時,它也意味着,Montgomery團隊這幾年的工作付諸東流。
幸運的是,移植術後,豬腎沒有出現排異反應,幾乎立即開始正常工作,產生尿液和肌酐,並正常工作了54個小時,直到實驗結束。Montgomery 表示,效果甚至比我們預期的還要好。
此次實驗的成功,可以説是異種移植的一次突破性進展,是數十年來人類尋求使用動物器官異種移植挽救生命的重要一步——異種移植的時代,將要到來了嗎?在異種移植實現臨牀以前,我們又還要面對什麼障礙?
器官移植缺口巨大
之所以要發展異種移植,其根源還在於器官移植的巨大缺口。
1954年12月23日,美國成功進行了世界第一例人體器官移植。此後,器官移植技術快速發展,20世紀70年代以來,器官移植已經成為腎功能衰竭和其他器官疾病患者的切實選擇。然而,由於捐獻的器官數量有限,大量患者需要在長長的隊伍中****等待救命的器官。
據世界衞生組織統計,全世界每年大約有200萬人需要器官移植,而器官供體的嚴重短缺,讓全球平均器官供需比不足1:20。僅在美國,就有超過10萬人正在等待合適的器官,其中超過9萬人在等待腎臟移植。腎臟的等待時間平均為三到五年**,這意味着,平均每天都有超過20人在等待器官的過程中****離開人世**。
全世界的科研人員都在嘗試通過多種途徑解決器官移植短缺問題,異種器官移植無疑是其中比較具有應用前景的手段。人們夢想着異種移植能在某一天實現,即用動物器官來解決可供人類移植的器官短缺問題,但異種移植通常是危險的。
異種移植的最大障礙就是不相容性。人體強烈排斥與自身不完全相似的細胞存在,這使得人與人之間的移植也變得非常棘手。潛在的捐贈者需要儘可能接近受體,無論是在遺傳學還是血型方面,而受體需要服用免疫抑制劑以保持較低的排斥率。然而,當試圖跨越物種障礙時,排斥問題會更加複雜。
事實上,早在17世紀,就有人嘗試用動物血液給人類輸血,當然,結果可想而知。後來,科學家們試圖利用靈長類動物的器官來避免排斥問題。但由於各種原因,並沒有出現成功案例。
1984年,經過多年的研究,美國洛馬林達大學醫療中心的移植外科醫生Leonard Bailey認為他已經克服了免疫系統對外來器官的快速排異反應。隨後,他將一顆狒狒的心臟移植到一個出生僅12天的畸形嬰兒體Fae內。然而,這並未能拯救Fae,她在手術後第21天死於機體排斥和器官衰竭。
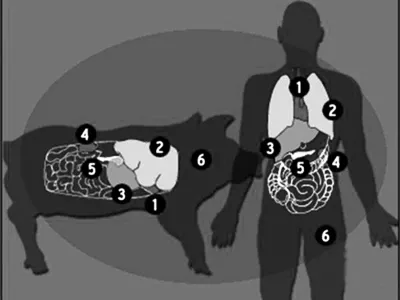
**此後,科學家們將研究重點從靈長類動物轉向了豬,**豬成為解決器官短缺問題的研究重點。因為豬本身就作為人類的食物而被養殖,因此用於器官移植所產生的的倫理問題較少,此外,豬的產仔數量大,妊娠期短。並且,豬和人類還有許多共同點,無論是生理上、解剖上,還是基因上。
實際上,幾十年來,來自豬的心臟瓣膜、來自豬腸的肝素、以及豬皮移植物和豬角膜,已經被成功應用於人類的治療。比如,血液稀釋肝素是從豬腸中提取的;豬的皮膚移植被用於燒傷;中國外科醫生曾用豬的角膜來恢復患者視力。
但是**,將豬的整個器官移植給人類,首先面臨的問題依然是****免疫排斥,這主要是由於豬攜帶的基因產生的α-Gal(α-半乳糖)抗原所致**。事實上,人與豬的不同之處就在於,豬比人多一種蛋白酶,這種蛋白酶可以把α-Gal置於存在於細胞表面的分支糖鏈上,使得人體的免疫系統把α-Gal作為攻擊的信號。
畢竟,此次豬腎臟移植人體手術得以成功的一個關鍵原因,就是用基因技術,敲除了會引起免疫排斥的α-Gal基因。
希望和挑戰並存
此次豬腎臟移植人體手術的實驗來自美國紐約大學朗格尼醫學中心移植外科Montgomery教授團隊。**值得一提的是,Montgomery醫生本人就是心臟移植的接受者,**深知異種移植技術的重要性和迫切性。為了此次實驗,Montgomery已經準備了多年。
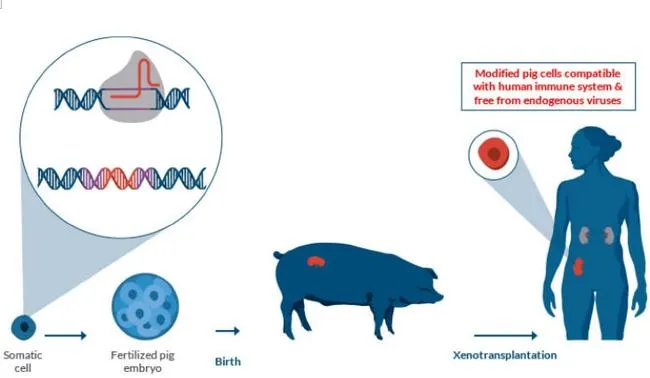
Montgomery醫生團隊用的轉基因豬腎臟,來自於Revivicor公司的GalSafe豬。 如上所述,豬攜帶的基因產生的α-Gal抗原,是使得人體的免疫系統把α-Gal作為攻擊的信號,為了消除這個攻擊信號,Revivicor公司通過CRISPR基因編輯方法,敲除了在豬細胞表面添加α-Gal的蛋白酶,讓豬細胞不再表達α-Gal,從而克服了超急性排斥反應。
轉基因豬由此被賦予了GalSafe豬的名字。2020年12月15日,美國FDA宣佈GalSafe豬獲批上市。這種家豬可能用於食品或人類治療。新聞稿指出,這是 FDA批准的首個可以同時用於人類食物消費和作為潛在療法來源的IGA動物,但尚未評估這些豬用作異種移植產品或植入人類受試者。此次Montgomery教授團隊的實驗就是一次對GalSafe豬的良好試驗。
接受豬腎移植的則是一位腦死亡的女性,且腎功能不全,其家人同意在停止生命跡象前進行該項實驗。因此,Montgomery教授團隊將基因改造過的豬腎臟連接到患者腹部外側的大腿血管上,並對患者的身體情況進行了兩到三天的觀察。
移植手術結束後,器官接受者的身體沒有立即出現排異反應,且豬腎在與患者血管相連後,正常發揮過濾廢物、產生尿液的作用,並正常工作了54個小時**。**同時,患者的肌酐水平也在術後恢復正常,肌酐水平是衡量腎功能是否健全的指標之一。在移植手術後3天,患者生命支持設備按預定日期去除。
Montgomery表示,器官在體外發揮作用的事實,有力地表明它在體內也會發揮作用。“這比我們預期的還要好,”他説,“它看起來就像我做過的任何活體捐贈者的移植手術。很多來自死者的腎臟無法立即工作,需要幾天或幾周的時間才能開始工作。而這次的移植立即就起作用了。”
當然,雖然作為世界首例豬腎臟移植人體手術,Montgomery團隊大獲成功,但從在異種移植的角度來講,離真正的異種移植臨牀又還有很大距離。
一方面,從試驗對象來看,這次試驗的受體是一位腦死亡的女性,在家屬同意後,研究團隊並沒有像正常器官移植那樣將腎臟移植到髂內動靜脈上,而是選擇和受體大腿的血管相連。在接下來的 54 個小時裏,腎臟被放在受體體外保存。
雖然方便了研究人員從外部觀察腎臟的外觀和功能狀態,但也意味着,異種腎移植手術並非為了拯救患者,只是一次在人體上進行的技術驗證。在 54 小時的觀察後,試驗結束。目前,這項研究並沒有經過同行評議,也暫無數據發表。
另一方面,雖然通過基因技術****敲除α-gal 後能夠逃避超急性排斥反應,但 α-gal 僅僅是超急性排斥反應靶點中的一個,其他靶點還包括但不限於:CMAH 基因,CMAH 基因存在和表達能夠引起異種移植免疫排斥;ASGR1 基因,ASGR1可以被受體的免疫細胞識別並攻擊,引起急性的血管內凝血,造成豬器官的快速失活,同時還可以誘發異種移植後受體發生血小板減少症等等。
人類對於器官移植的探索已經持續了數百年,並且已經解決了許多阻礙豬腎移植的歷史障礙。因此,面對豬腎異種移植作為緩解目前人體器官捐贈短缺的問題,併為終末期腎病患者提供更大的長期生存機會和更好的生活質量的這一潛力技術,我們也不妨多一些樂觀的希望。