老年痴呆被他玩明白了!首次發現有毒蛋白複製方式!_風聞
推医汇-汇聚健康行业资讯,推动学术交流。2021-11-15 17:41
“誰能告訴我,我到底是誰?”安東尼·霍普金斯飾演的主角在電影《困在時間裏的父親》中發出終極之問。

(圖片來源:網絡)
世界衞生組織發佈的最新數據顯示,目前全球超過5500萬人患有痴呆症,而且患者數量正以每年新發近1000萬例的速度不斷增長,相當於每3秒就有1人患病。預計到2050年,全球痴呆症患者將達到1.39億。而這一增長大部分將發生在中國、印度和拉丁美洲等快速發展和人口密集的地區。
這是一種很難研究的疾病,因為它發展了幾十年,只有在檢查死後的腦組織樣本後才能給出明確的診斷。
目前,研究人員主要依靠動物模型來研究這種疾病。然而,動物模型不能很好地再現兩種關鍵蛋白——tau蛋白和澱粉樣蛋白的聚集速率,使得研究進展非常緩慢。
人們一直認為,阿爾茨海默病的發展方式與許多癌症類似:導致阿爾茨海默病的有毒蛋白質在一個區域形成聚集體,然後擴散到整個大腦。
然而,近日一項由劍橋大學領導的國際團隊打破了這一認知:阿爾茨海默病不是從大腦中的單個點開始並引發導致腦細胞死亡的連鎖反應,而是早期就存在於大腦的不同區域,並隨着時間的推移不斷複製擴增。疾病通過產生有毒蛋白質簇“殺死”這些區域細胞的速度,限定了疾病整體的進展。

(圖片來源:Science Advances)
在阿爾茨海默病中,tau蛋白和β-澱粉樣蛋白(Aβ)形成纏結和斑塊(統稱為聚集體),導致腦細胞死亡和大腦萎縮。這會導致記憶喪失、性格改變和日常活動困難。
在本研究中,研究小組“破天荒”地使用了人體樣本——阿爾茨海默病患者的死後大腦樣本,以及活體患者(從輕度認知障礙患者到綜合型阿爾茨海默病患者)的PET掃描,來跟蹤tau蛋白的聚集。
研究人員採用了五種不同的tau量化方法,將它們應用於相同的數學模型中,觀察到了控制阿爾茨海默病進展速度的機制是大腦各個區域中聚集體的複製,而不是聚集體從一個區域到另一個區域的擴散。
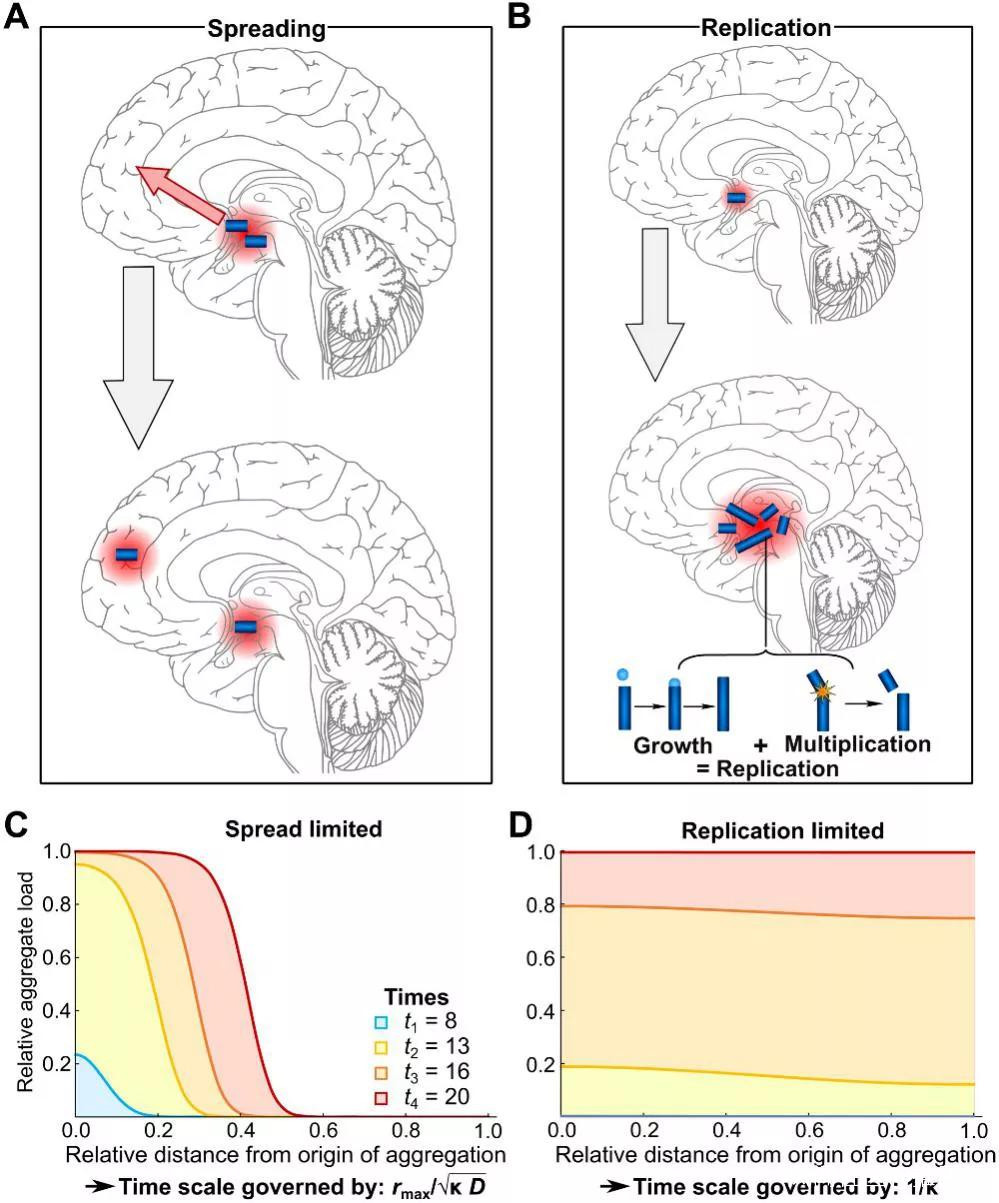
圖解tau聚集體形成的關鍵過程
( A ) 擴散,表示現有聚合體的空間重定位
( B ) 複製,即從現有種子本地化生產新種子
通過對去世的阿爾茲海默症患者的大腦進行解剖學分析,依據Tau蛋白組成的神經纖維纏結的位置將其分成了6個發展階段,即Braak分期。從1至6期,大腦中神經纖維纏結逐漸增多。
研究團隊觀察到,Braak 3期後,tau蛋白的分佈隨時間變化較快。同時,複製的減少顯著減緩了tau的總體積累。這意味着Braak 3期之後,tau蛋白累積的整體速率由複製速率決定,抑制複製會最大程度減緩整個過程。
有趣的是,tau蛋白聚集體的複製速度很慢,需要長達5年的時間。
“神經元在阻止有毒蛋白聚合物形成方面令人驚訝地好,但如果我們要開發一種有效的治療方法,需要找到使它們變得更好的方法。生物學是如何進化到阻止蛋白聚集的,這很吸引人。” 劍橋大學英國痴呆症研究所的David Klenerman教授説,“關鍵的發現是,在我們研究的疾病階段,阻止有毒蛋白聚集物的複製而不是它們的傳播會更加有效。”
這一研究“刷新”了人們對阿爾茲海默病發展的認知,使阿爾茲海默病治療邁向了一個新徵途。
但迄今為止,仍然缺乏有效的治療藥物。各路人馬正前仆後繼,不斷推出新的治療方法。
近日在《科學》子刊Science Signaling上發表的研究顯示,兩款已經上市幾十年的“老藥”聯用,在動物模型中不但顯著降低了與阿爾茨海默病相關的β澱粉樣蛋白沉積,而且改善了動物的記憶和認知能力。這為治療阿爾茨海默病提供了另一科學基礎。

(圖片來源:Science Signaling)
在這項研究中,美國拉什大學醫學中心的研究人員使用降脂藥吉非貝齊和維生素A衍生物視黃酸進行聯合治療。他們發現,吉非貝齊和視黃酸聯用可能改變星形膠質細胞的作用,讓它們成為幫助清除β澱粉樣蛋白的工具。
同時,在阿爾茨海默病的小鼠模型中,給小鼠服用這兩種藥物,可以顯著降低小鼠大腦中的β澱粉樣蛋白沉積,而且小鼠的認知功能在服藥兩個月後,與對照組相比也獲得了改善。
那麼這兩種藥物是如何產生作用的呢?
進一步研究發現,吉非貝齊和視黃酸能夠激活細胞中名為PPARα的受體蛋白,該蛋白調控的基因——TFEB的高度表達可以促進β澱粉樣蛋白的降解。
此外,這兩種藥物還刺激低密度脂蛋白受體(LDLR)的表達,LDLR在介導β澱粉樣蛋白被細胞攝取方面發揮關鍵性作用。
這兩種作用疊加在一起,增強了星形膠質細胞攝取和降解β澱粉樣蛋白的能力。
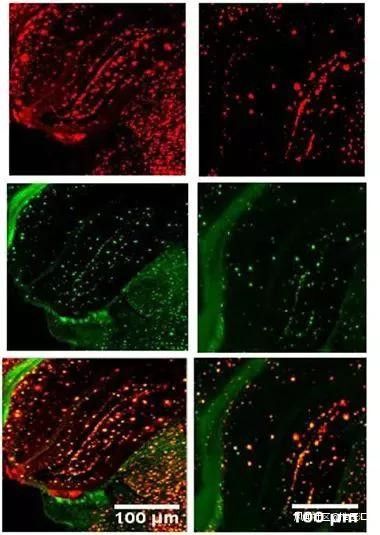
這一組合療法顯著降低小鼠大腦中β澱粉樣蛋白的沉積(紅色和綠色斑點)
(圖片來源:參考文獻)
儘管這一“老藥新用”搭配在小鼠模型中成效顯著,但能否在人類中起到相同的作用還需要未來更深層次的臨牀驗證。探索已經上市的“老藥”新用的一個優勢在於這些藥物的安全性已經得到了廣泛驗證,因此可以更快速地展開臨牀試驗,檢驗它們的療效。據悉,該項目研究人員已將吉非貝齊和視黃酸組合授權給一家公司,它正在準備遞交IND申請,在臨牀試驗中檢驗這一組合的效力。
目前,阿爾茨海默病等痴呆症仍無法治癒。隨着對病因的研究越來越多,期望隨着時間的推移,科學家能找到治癒阿爾茨海默病的方法,造福患者。
參考文獻:
Aβ Clearance The Uptapped Potential of Astrocytes? Retrieved November3, 2021, from https://www.alzforum.org/news/research-news/av-clearance-untpped-potential-astrocytes