RNA療法未來無限,Sirnaomics衝刺核酸藥物第一股_風聞
王新喜专栏-自由撰稿人-2021-12-10 20:18
文丨April Chen
來源:新浪醫藥新聞
自2018年起,多個針對多種遺傳或肝臟疾病的RNAi療法陸續獲批上市。其後,在新冠疫情全球爆發後不到一年的時間裏,BioNTech和Moderna兩家核酸藥公司就成功研製出了針對COVID-19的mRNA疫苗,僅一個季度就創造了數十億美元的全球收益。而今年,關於核酸藥物公司被跨國藥企投資或收購的新聞更是數見不鮮。核酸藥物的巨大市場潛力使得一二級投資機構紛紛加碼。就在今年7月,全球首家運用RNAi技術針對腫瘤取得積極臨牀IIa期數據的Sirnaomics Ltd.向港交所遞交了招股申請書,衝刺成為核酸藥物第一股。
1
RNA療法的主要類型
根據分子生物學中心法則,遺傳信息由DNA轉錄為RNA,再由RNA翻譯為蛋白質,調控着生命體的多種生理活動。不同於傳統小分子藥物和抗體藥物在蛋白質水平進行調控,RNA藥物可在蛋白表達水平的調節過程中發揮作用。與必須穿過細胞質和核膜並冒着整合到宿主基因組風險的基因治療方法不同,RNA療法可以通過到達宿主細胞質的生物機制來發揮作用,並且沒有潛在的基因組整合風險。
目前,RNA療法主要包括四種類型:RNA適配體(Aptamer),反義寡核苷酸(ASOs),RNA干擾(RNAi)和信使RNA(mRNA)。
截止當前唯一獲批上市的Aptamer藥物為2014年上市的Pegaptanib,靶向VEGF血管內皮生長因子亞型,用於治療新生血管年齡相關性黃斑變性的抗血管生成。
ASOs是當前獲批數量最多的RNA藥物類型,包括2016年獲批的全球首個SMA(脊髓性肌萎縮症)治療藥物,渤健公司的諾西那生鈉注射液(英文商品名Spinraza®),在今年被納入中國國家醫保目錄後,會為更多SMA中國患者提供治療機會。
而被業內譽為第三代技術浪潮且獲得諾貝爾獎的RNAi療法的發展,則幾經波折。在2010年左右,由於安全性差、療效低,羅氏、輝瑞等國際製藥巨頭紛紛放棄開發RNAi藥物。直到2018年首個RNAi藥物,用於治療hATTR(一類罕見的多發性神經疾病)的Patisiran獲批,才真正掀開了RNAi治療領域的新紀元。
目前,多家跨國藥企都在大舉佈局RNAi療法。
至於mRNA技術,其目前發展最快的研發方向是mRNA疫苗。mRNA疫苗在臨牀研究中高達95%的保護率,使得mRNA成為新冠疫苗開發中最為炙手可熱的技術。
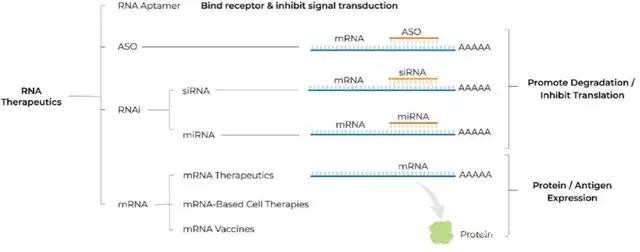
圖一:NA療法的主要類型
2
RNA療法發展的新浪潮
在2021年,全球有超過600個RNA療法處於開發階段。資本市場的不斷加碼,更是加速了RNA療法發展的新浪潮。
從研發管線來看,目前RNAi和mRNA療法在研項目的數量已經超過ASOs,成為在研最多的RNA藥物研發類型——前兩者佔所有RNA藥物開發項目總數的約70%。今年多個關於RNA療法的投資或者併購項目,也主要集中在這兩種技術,其中不乏跨國公司的大手筆舉動。
就在上個月,諾和諾德宣佈以33億美元收購專注於RNAi藥物開發的公司Dicerna;8月份時,賽諾菲宣佈以32 億美元收購專注於mRNA疫苗開發的公司Translate Bio。同時,國內的龍頭藥企也紛紛入局RNA。瀚森製藥今年10月宣佈分別與Silence Therapeutics和OliX Pharmaceuticals達成合作,前者涉及金額超13億美元,合作開發針對三個靶點的siRNA藥物;後者涉及金額超4.5億美元,合作開發針對關鍵靶向適應症的非對稱小干擾RNA(aiRNA)療法。此外,以疫苗為主營業務的雲南沃森生物也在今年早些時候與Sirnaomics簽訂了關於抗流感病毒RNAi藥物的合作授權。
除了投資和收購頻頻有大動作之外,國內核酸藥物的開發探索也方興未艾,聚集了像Sirnaomics、斯微生物、瑞博生物、鋭博生物等多家在該領域深耕多年的專業團隊。這些後來居上的公司在一級市場深受資本青睞,今年的融資額均超億元人民幣。其中,Sirnaomics年中剛剛完成其E輪融資1.05億美元,是今年國內RNAi領域融資額最高的企業。
3
RNA療法的優勢和挑戰
行業內交易和合作的增加大幅加快了RNA療法開發的速度。從以前主要針對罕見遺傳疾病,擴展至更為常見的臨牀指症,如癌症、心血管疾病和神經疾病等。
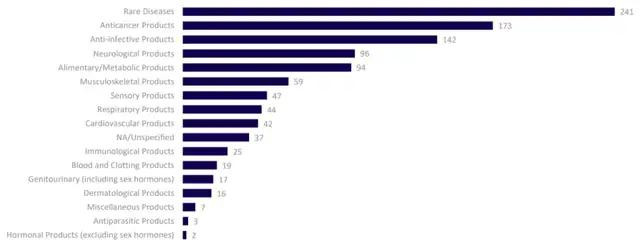
圖二:RNA療法研發管線適應症彙總(截至2021年7月)
RNA技術與其他治療方式相比具有多重優勢。RNAi可通過直接靶向mRNA的鹼基對及細胞質中的其他靶向RNA,並阻止疾病相關蛋白的生成來調節細胞外及細胞內各種蛋白質的表達,促進靶向降解,從而形成有效的靶向基因沉默。因此,RNAi技術可以擴大成藥的靶點範圍,比基於蛋白質的藥物具為有效,並且能夠個性化設計藥物以對患者特定的遺傳病變起作用。
在新冠流行期間,mRNA疫苗可根據最新的毒株突變,快速編碼對應的預防性mRNA,從目標識別到臨牀前概念驗證的時間可以縮短至幾個月,進而能在新冠疫情爆發或季節性流感病毒突變期間,迅速且有效地開發疫苗。
從目前已經上市的RNAi藥物和mRNA疫苗可以看出,RNA療法安全性普遍很好,且因其生產工藝相對簡單,給藥劑量低,所以規模化生產所必需的硬件投入也更少,從而製造成本也更低。
但是,目前RNA技術目前仍存在多種風險,其中最主要的挑戰就是靶向遞送。由於mRNA本質上是不穩定的,需要運輸工具來保護藥物免受RNA酶降解,因而就需要能成功將RNA藥物靶向遞送至治療部位的新型遞送載體。
脂質納米顆粒 (LNP) 是最常用的 RNA 遞送技術,2018 年獲得美國 FDA 批准的全球首個RNAi藥物採用的就是LNP 載體。目前國際上mRNA行業三大巨頭Moderna、CureVac和BioNTech所開發的新冠疫苗,均採用了 LNP 遞送技術。但 LNP製造工藝複雜,成品劑型的穩定性有限(只有6個月),且需要冷鏈儲存及運輸。
另一種常用的RNA遞送平台是GalNAc。唾液酸糖蛋白受體 (ASGPR) 的配體,結合後會觸發構建體的內吞作用。由於該蛋白在肝細胞上大量表達,所以RNA可以自然地集中在肝臟中,是針對肝臟靶向遞送的有效方法。基於這項技術的RNAi療法相對於LNP載體較為簡單,且成品劑型可以凍幹以提高穩定性,無需冷鏈儲存及運輸。2019年獲批上市的Givosiran是世界上第一個獲得 FDA 批准的以GalNAc作為載體的 RNAi 藥物。
因此,是否擁有核心的核酸藥物遞送技術,成為RNA行業內各家公司是否能獨佔鰲頭的關鍵所在。
4
Sirnaomics—全球首家使用RNAi技術取得抗腫瘤臨牀IIa期積極結果的生物製藥公司
Sirnaomics於2007年由創始人、總裁兼首席執行官Patrick Lu(陸陽)博士在美國創立。2008年,Sirnaomics的中國總部——聖諾生物醫藥技術(蘇州)有限公司在蘇州納米園誕生。公司主要針對RNAi及mRNA療法進行研發,在中國及美國均深耕多年且佔有重要的市場地位。Sirnaomics是全球首家使用RNAi技術取得抗腫瘤臨牀IIa期積極結果的生物製藥公司。不斷追求技術的創新、產品的差異化以及臨牀和產業化的全球佈局,是Sirnaomics在RNAi療法開發中每天都在做的事情。
在關鍵的藥物遞送技術方面,Sirnaomics擁有全球獨家的多肽納米導入系統(PNP)。PNP由天然氨基酸組成,其降解物天然無毒,克服了藥物的靶向性和穩定性障礙。可通過局部或全身給藥,毒性低、易製造、可觸達除肝臟外眾多靶向器官。同時,既可遞送siRNA也可遞送mRNA。PNP可同時攜帶多個不同靶向的siRNA,使其在同一靶向細胞中產生協同的基因沉默效應,從而提高RNAi的藥物療效。Sirnaomics也開發出了新型的GalNAc RNAi遞送平台GalAhead™和PDov,能夠實現對肝細胞的高效能、精準遞送。
此外,Sirnaomics還在不斷開發新的核酸藥物遞送平台,包括siRNA/化學藥物偶聯物的不同組合、肽配體腫瘤靶向以及通過呼吸道給藥進行疾病治療。
在佈局的疾病領域方面,Sirnaomics將RNAi藥物的適應症範圍從肝細胞相關疾病拓展到腫瘤、纖維化、皮膚、病毒感染及心血管類等指症,並在臨牀開發過程中逐步擴展其全球化佈局。
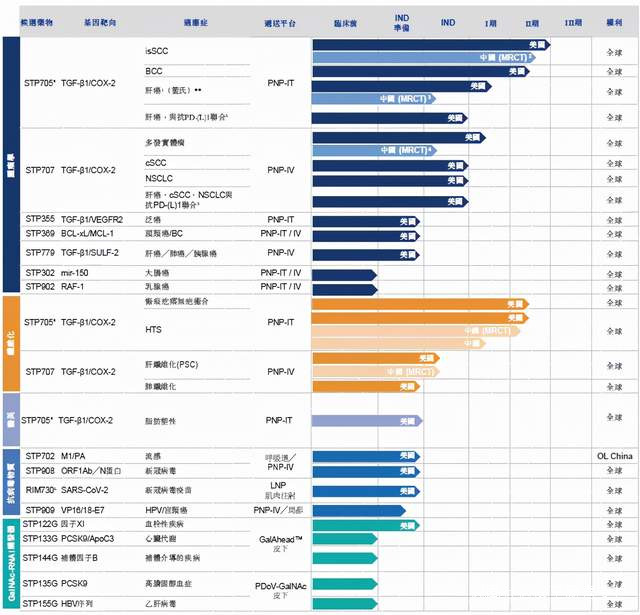
圖三:Sirnaomics現有的研發管線(截止到2021年12月)
Sirnaomics最矚目的兩個核心產品,是具有首創優勢的雙靶點RNAi藥物——STP705和STP707。
目前已進入臨牀IIb階段的STP705是一種TGF-β1/COX-2雙抑制劑。TGF-β1在包括皮膚癌及肝癌等多種癌症中過度表達;COX-2的慢性升高會導致慢性肝臟炎症、肝纖維化及肝硬化,且在皮膚癌(鱗狀細胞癌SCC及基底細胞癌BCC)患者中也有過度表達。STP705可同時抑制這兩個靶點,通過抑制腫瘤細胞增值、上皮間質轉化、血管生成等機制,抑制腫瘤細胞的生長。而針對纖維化疾病,同時抑制TGF-β1及COX-2可以通過減少炎症、激活纖維細胞的凋亡,來逆轉纖維化瘢痕的形成。STP705採取PNP遞送技術通過局部給藥的方式,直接作用於患病組織,目前正針對多種皮膚癌、皮膚組織纖維化和肝癌等疾病類型開展臨牀試驗。在目前已經完成的鱗狀皮膚原位癌isSCC的I/II期試驗中,76%(19/25)的患者在治療結束時實現了病變的組織學清除,且安全耐受性良好。STP705在基底細胞癌、瘢痕疙瘩和增生性瘢痕(HTS)的早期試驗中也展現了類似的療效和安全性。此外,STP705已獲得美國FDA頒佈的三項孤兒藥認證,用於治療肝細胞癌、原發性硬化性膽管炎和肝膽管癌,也計劃即將啓動與PD-1/L1抑制劑的聯用。
STP707對比STP705的區別在於,前者的給藥途徑為全身系統給藥。這充分説明了PNP遞送技術的靈活性。STP707通過靜脈給藥用於多種實體腫瘤治療的IND申請在今年7月份獲得美國FDA的批准進入臨牀試驗,即將於近期完成首位病患的給藥。
Sirnaomics產品線中開發進度最為靠前的STP122G項目,包含靶向因子XI的RNAi觸發器,採用GalAhead™遞送技術用於皮下給藥。在最近的非人靈長類的試驗中,STP122G單次皮下注射後顯示出超過26個星期靶點敲低的體內藥物效果。
在mRNA療法及疫苗的研發方面,Sirnaomics子公司RNAimmune是一家專注於mRNA疫苗及新型藥物研發創制的生物醫藥企業,目前其候選產品管線包括新冠疫苗,流感疫苗,狂犬疫苗,帶狀皰疹疫苗,廣譜RAS疫苗,和其他腫瘤疫苗等。該公司核心產品之一,是針對新冠病毒的疫苗候選產品RIM730,由應用脂質納米粒(LNP)遞送技術配置的編碼德爾塔變體SARS-CoV-2全長刺突蛋白的mRNA組成,使用方式為肌肉注射給藥。在體內小鼠模型中的臨牀前結果顯示,RIM730成功誘導了強烈的免疫反應,取得積極試驗結果。
在產品開發的市場佈局方面,Sirnaomics在中美兩地都有雄厚的科研生產和業務運營能力,且通過戰略互補中美兩地的監管優勢,來加速產品開發和臨牀批准。同時,Sirnaomics也在與中美的生物製藥公司及學術機構緊密合作,包括與信達生物及上海君實合作開發STP705和免疫檢查點抑制劑的聯合療法,與沃森生物簽訂協議共同開發抗流感核酸藥物等。
2021年7月中旬,Sirnaomics向港交所遞交了招股説明書,並於11月底成功通過港交所聆訊,即將成為中國核酸藥物第一股。在新冠病毒至今仍肆虐全球而mRNA疫苗逐步發揮效力的背景下,在中國生物醫藥產業日新月異發展而其中RNA領域進展尤為突出和矚目的背景下,Sirnaomics的上市,將會成為全球和中國RNAi/mRNA技術產業發展的一個新里程碑。