美國FDA緊急召回超2百萬新冠自測盒:不準確的診斷或危及生命
(觀察者網訊)據《紐約時報》(the New York Times)11月10日報道,美國食品藥品監督管理局(FDA)11月9日發佈聲明,宣佈召回澳大利亞醫療科技製造商Ellume生產的2212335份非處方居家新冠檢測盒,因該檢測盒存在缺陷,可能顯示假陽性結果。
美國FDA網頁刊載的召回聲明截圖
召回聲明顯示,Ellume公司稱其產品新冠檢測結果假陽性高於可接受水平,所謂“假陽性”,即測出陽性的受測者實際上沒未感染病毒。FDA和Ellume公司均表示,檢測盒測出陰性結果的可靠性未受影響。
此次召回被FDA標記為最為嚴重的1類(Class 1),FDA解釋稱,使用這種檢測盒可能導致嚴重的不利健康後果乃至死亡。
《紐約時報》報道稱,FDA指出,被誤檢出陽性的人可能會接受不必要的新冠治療,並導致對患者的真實病因的診斷出現延誤,並進一步耽誤治療。
該公司的一名代表表示:“Ellume已經調查了這個問題,找出了根本原因,並實施了追加的控制措施,我們已在生產新產品並正在向美國運送”。

Ellume公司生產的檢測盒外觀
FDA表示,已經有35起關於該檢測盒測出假陽性的投訴,但無與之相關的死亡報告。目前尚不清楚誤檢產生的假陽性案例一共有多少。
該公司此前曾在10月向FDA通報稱,由於生產問題一些批次的測試盒出現缺陷。
在該公司網站上發佈的一份聲明中,創始人兼首席執行官肖恩·帕森斯(Sean Parsons)向使用了瑕疵品的用户致歉。
Ellume公司還表示,該公司已糾正了製造上的問題,美國聯邦監管機構則表示,他們正在監督該公司繼續努力。
FDA在一份聲明中表示:“FDA正同Ellume共同評估該公司的糾正行動,如增加生產檢查及其他的糾正措施,以解決製造環節出現問題的原因,並幫助確保問題得到解決,不會再次發生。”
據美國全國公共廣播電台(NPR)報道,今年早些時候,拜登政府與Ellume公司達成了一項價值2.318億美元的協議,以在美國市場增加該測試盒的供應。
Ellume公司與美國國防部以及美國衞生與公眾服務部簽訂的合同為該公司在美首家工廠提供了資金,今年5月該廠在美國馬里蘭州弗雷德裏克開業。
在疫情持續的背景下,美國聯邦監管機構曾授予一系列公司進行檢測的緊急授權。
今年3月,FDA宣佈了簡化家庭測試授權流程的計劃,這一流程10月份進行了更新。
同樣是在10月,白宮宣佈額外撥款10億美元用於家庭(新冠)測試,以緩解持續的全國短缺。
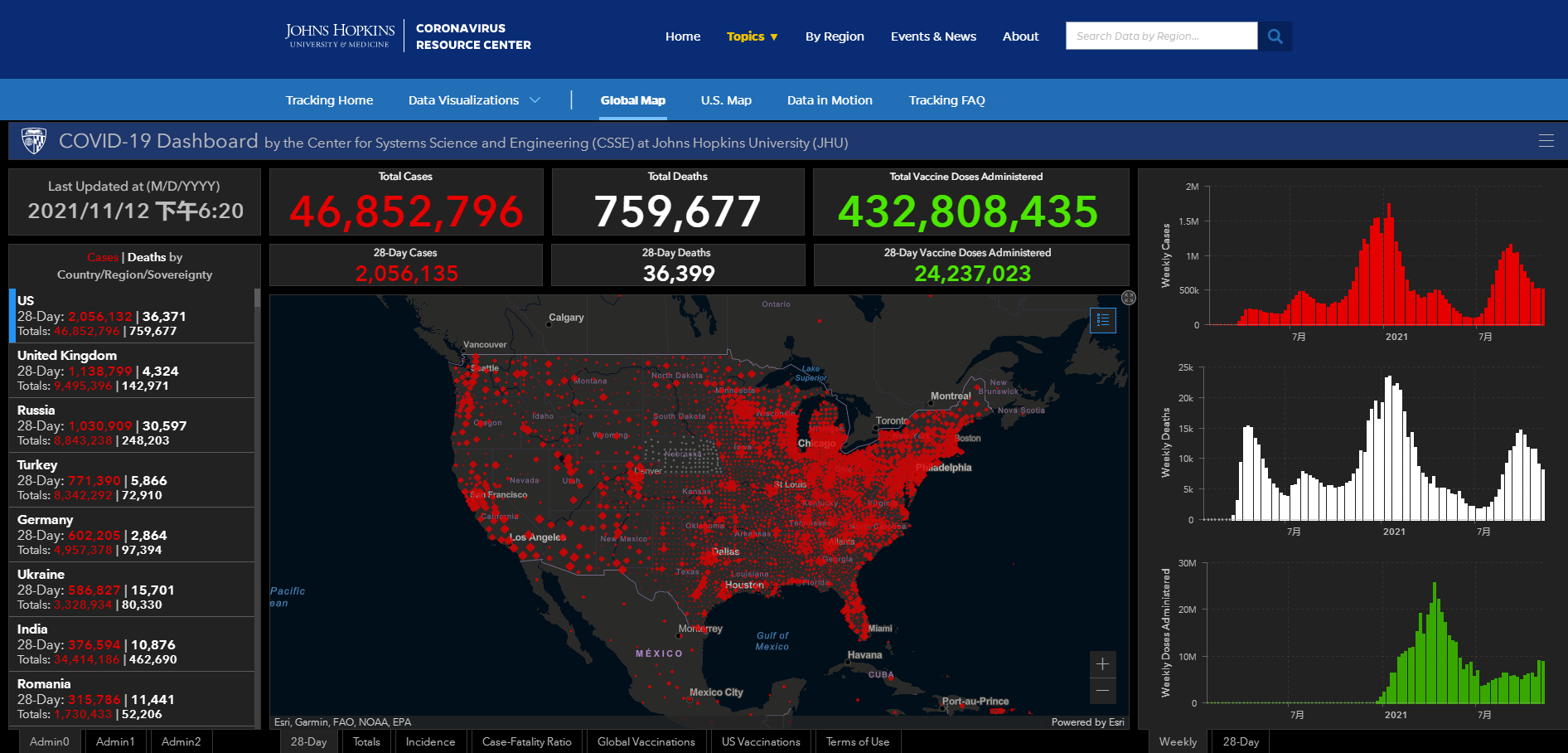
美國近期新增的新冠病例數及死亡數仍處於較高水平,根據美國約翰斯·霍普金斯大學統計數據,近幾周來,美國周新增病例數雖略有下降,但仍在50萬例上下,每週死於新冠肺炎的患者數也有約8000例。
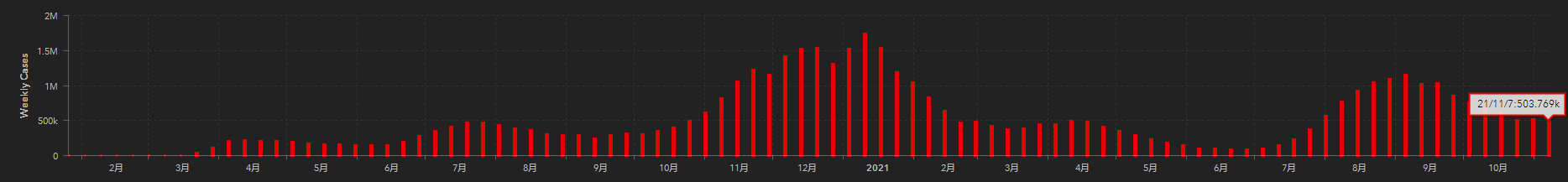
11月1日至7日這一週美國新增503769例新冠確診病例,而此前兩週新增確診數也大致在50萬例左右
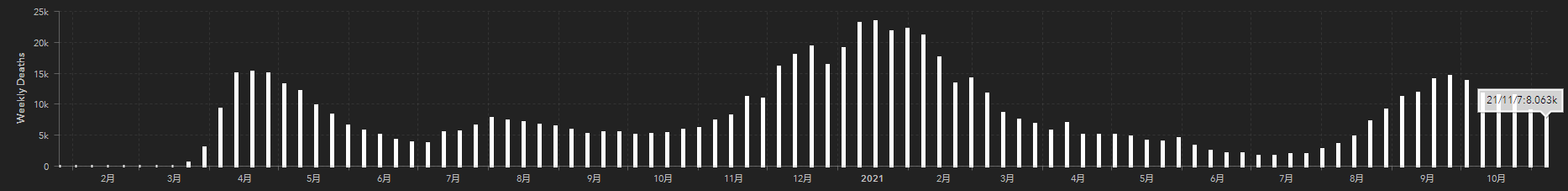
11月1日至7日美國新增新冠死亡病例數為8063例,已是兩個月來最低水平
截至北京時間2021年11月12日18時20分,美國新冠肺炎累計確診病例達46852796例,累計死亡病例759677例。