在工作中治療疲勞症狀的七種方法 - 彭博社
Arianne Cohen
 插圖:Dena Springer for Bloomberg Businessweek
插圖:Dena Springer for Bloomberg Businessweek 插圖:Carolina Moscoso for Bloomberg Businessweek
插圖:Carolina Moscoso for Bloomberg Businessweek
2015年,線上培訓平台Administrate的員工人數從13人增長到30人。當時35歲的首席執行官約翰·皮布爾斯在一個炎熱的夏日下午與投資者會面。他感覺不舒服,但還是繼續進行演講。“我開始出汗,感覺很熱,感覺像是在脖子上夾到了神經,” 皮布爾斯説。“我想,‘哇,情況不妙。希望沒人注意到。’” 他完成了演講,稍作交談後回到公寓樓。然後一切變黑了。“我就在樓梯間摔倒了。我想,‘嗯,我要死了。但至少我有關鍵人員保險,所以公司會得到保險賠償。’” 這不是理想的臨終遺言。
皮布爾斯倖存了下來,親身體會到身體崩潰的嚴重程度。這種認識後來塑造了總部位於愛丁堡的Administrate的文化和政策,該公司是最大的之一科技公司之一,自2015年起採用了長期的四天工作周。“在這裏工作32小時相當強烈,” 皮布爾斯説。“但之後你就可以休息了。”
BioMarin Pharmaceutical Inc.的一種用於遺傳性出血性疾病的新治療方案本應是一次勝利。針對的患者羣比這家生物技術公司通常瞄準的範圍更廣,Roctavian是其首次涉足基因療法領域,這是修複基因缺陷以潛在治癒疾病的有前途的醫學領域。
迄今為止,Roctavian在治療血友病A方面未能獲得進展——自去年六月獲批准以來,美國只有一個付費患者接受了這種療法,截至2023年底,首席執行官亞歷山大·哈迪在一月份在摩根大通醫療保健大會上表示。對於一個曾被預期在2023年實現超過1億美元收入的產品來説,這是一個嚴重的失望。
“他們未能讓這個項目起飛,”RBC資本市場的生物技術分析師盧卡·伊西表示。“許多這類療法的商業成功並不如我們所期望的那樣。”
Roctavian的低調開局給一家已經在與激進投資者艾略特投資管理公司達成協議的公司增加了壓力,並增加了一長串難以找到接受者的基因療法的名單。一個接一個,無論是大型還是小型製藥公司都發現高昂的製造成本、數百萬美元的價格和其他挑戰使這些療法難以銷售,並在某些情況下,對其生存構成威脅。
目前有大約2,000種基因療法正在研發中,許多針對癌症和罕見疾病,而且熱度前所未有。一月份,Eli Lilly & Co.的Akouos部門表示其基因療法幫助一名11歲男孩第一次聽到聲音。就在兩種鐮狀細胞病基因療法獲得美國食品和藥物管理局批准的一個月後。總統喬·拜登表示這一進展“代表了醫學創新改善美國人生活的力量。”
基因治療支出預測
來源:2023年11月發表在《基因治療》雜誌上的研究
分析僅考慮截至2020年12月在美國市場上或正在開發中的基因治療
這項技術已經至少有一個商業成功案例。Zolgensma,諾華製藥的基因治療藥物,治療脊髓性肌萎縮症,過去三年每年創收超過10億美元。儘管這種遺傳疾病罕見,大約每1萬人中就有1人患病,但這種藥物銷售得很好,部分原因是因為需求巨大;如果不接受治療,許多患有嚴重疾病形式的兒童在兩歲之前就會死亡。
但其他基因治療並沒有那麼成功。人們對葛蘭素史克的Strimvelis寄予厚望,該藥於2016年在歐洲獲批用於治療一種潛在致命的疾病,稱為嚴重聯合免疫缺陷,每位患者的治療成本約為70萬美元。這種疾病有時被稱為“泡泡男孩病”,在20世紀70年代和80年代初,年輕患者大衞·維特大部分時間生活在一系列無菌環境中,直到12歲去世。Strimvelis在近兩年時間裏僅治療了少數患者,直到英國製藥公司將其轉讓給了意大利研究慈善機構,現在這種藥物由他們負責。
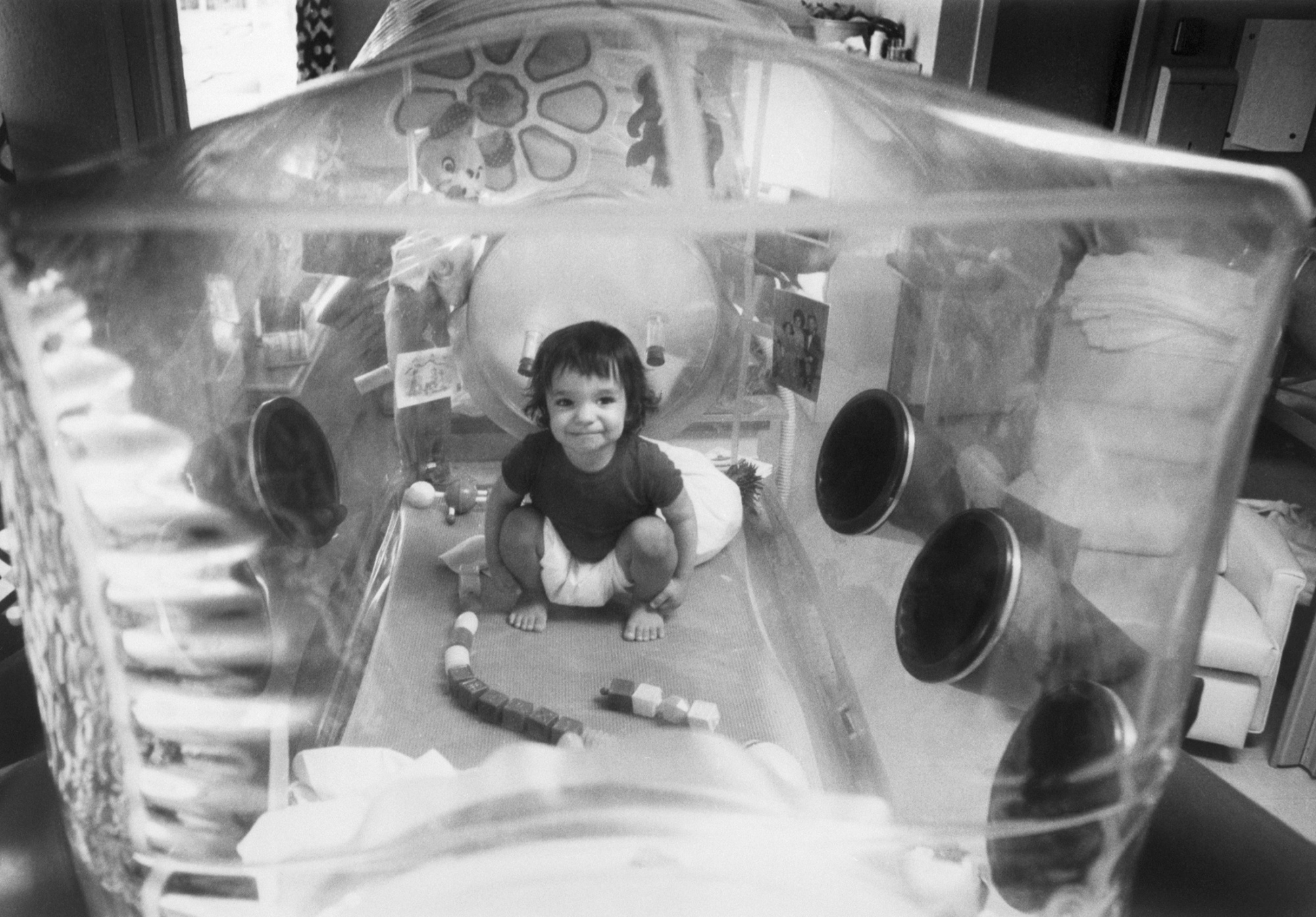 1973年,大衞·維特在封閉的塑料環境中玩耍,以保持免受細菌感染。他於1984年因所謂的“泡泡男孩病”去世,這是一種嚴重削弱免疫系統的遺傳病。圖片:Getty Images大約有30種基因療法獲得批准,類似的故事比比皆是。2019年,羅氏控股股份有限公司同意支付48億美元收購Spark Therapeutics,後者是治療遺傳性視力喪失和其他疾病的藥物製造商。但到2022年,這家瑞士藥企已經減記了超過10億美元的收購價值,原因是Spark已批准和實驗產品的銷售預期下降。
1973年,大衞·維特在封閉的塑料環境中玩耍,以保持免受細菌感染。他於1984年因所謂的“泡泡男孩病”去世,這是一種嚴重削弱免疫系統的遺傳病。圖片:Getty Images大約有30種基因療法獲得批准,類似的故事比比皆是。2019年,羅氏控股股份有限公司同意支付48億美元收購Spark Therapeutics,後者是治療遺傳性視力喪失和其他疾病的藥物製造商。但到2022年,這家瑞士藥企已經減記了超過10億美元的收購價值,原因是Spark已批准和實驗產品的銷售預期下降。
藍鳥生物公司的Zynteglo,一種每位患者售價280萬美元的基因療法,有望在患有一種稱為β地中海貧血的血液疾病的人中避免數百次輸血,但銷售一直不佳。這家生物技術公司的股價從2018年的約150美元暴跌至最近的約1美元。
藍鳥公司在一份聲明中表示,對Zynteglo的推出“非常滿意”,稱其“符合這種推出的預期”。
使用這些療法的最大障礙之一是成本,無論是對於藥企還是為其支付費用的保險公司。儘管基因療法的價格標籤達數百萬美元,但這些療法的利潤率可能很低,這可能會嚇跑長期投資者,Dark Horse Consulting Group創始人安東尼·戴維斯表示,該公司的客户包括這些治療藥物的製造商。
為了解決高昂的前期成本和長期療效的問題,製造商經常在治療效果隨時間減退時向保險公司提供部分退款。即便如此,根據美國基因與細胞治療學會委託的一項研究,幾個美國州的醫療補助計劃——其有限的預算並不足以支付這筆鉅額費用——已經對資格設定了限制。拜登政府在一月底宣佈了一項計劃,旨在讓各州更容易支付基因療法的費用。
開發一次性治癒方案的藥企面臨另一個挑戰:患者羣體數量下降。根據《基因療法》雜誌去年十一月發表的一項研究,預計2025年至2034年間,接受批准或正在開發的基因療法治療的新美國患者數量將減少三分之一,而這些治療的醫療支出預計將從2026年的253億美元降至2034年的210億美元。
麻省理工學院經濟學家喬納森·格魯伯(Jonathan Gruber)表示,這些數據並未考慮未來可能批准的基因療法,從而推高整體支出。但它們説明了問題所在:每個被治癒的患者都意味着潛在市場中減少了一個。對於任何一種基因療法來説,“成本會趨於穩定並下降,因為患有該疾病的初始人羣遠遠大於每年新患者的數量流入”,格魯伯説。
一些患者由於其免疫系統攻擊用於將基因傳遞至細胞的無害病毒而不符合某些療法的資格。最近的一項研究發現,全球超過500名血友病A患者中多達59%的人體內存在針對基因療法中使用的不同病毒類型的抗體。
此外,治療本身可能會帶來健康問題。例如,新的鐮狀細胞病基因治療需要先服用強烈的癌症藥物,可能會導致患者不孕。
現在,隨着治療更廣泛的疾病,像羅克塔維安這樣的治療方案——其美國上市價格為290萬美元——正在與現有藥物競爭,雖然這些藥物不能治癒,但可以給患者帶來足夠的緩解,以至於他們可能會猶豫嘗試一些新的、相對未經驗證的東西。
根據TD Cowen的研究,在美國至少有十幾種獲批的血友病A治療方案,包括羅氏的 Hemlibra,這是一種非常成功的藥物,一年的治療費用超過60萬美元。雖然價格昂貴,但與每年更換患者凝血蛋白的費用相比,後者可能高達50萬美元左右。
羅克塔維安的目標是通過一次手術消除那些昂貴的多年治療。但總的來説,接受基因治療的患者在增加凝血因子產生5到10年後,效果就會減弱,根據國家出血性疾病基金會的首席醫學和科學官邁克爾·雷希特的説法。
BioMarin仍在研究羅克塔維安的長期療效,今年公司將專注於擴大患者羣體,一位發言人表示。“我們對患者、醫生、患者倡導團體、血友病治療中心和支付者對羅克塔維安表現出的高度興趣感到非常鼓舞,”這位發言人在一封電子郵件中説。
成立於1997年,總部位於加利福尼亞州馬林縣的聖拉斐爾,BioMarin長期專注於治療大型藥企忽視的疾病。其中一款暢銷產品是 Voxzogo,用於治療骨發育不全症,一種侏儒症。在JPMorgan會議上,BioMarin的Hardy表示,這種藥物雖然不是基因療法,但有望成為暢銷產品,即年銷售額至少達到10億美元的藥物的行業標準。
Roctavian預計也會很成功。一年前,BioMarin預測該藥將於2023年上市,銷售額高達2億美元。但在去年11月,這一預期下調至不到1000萬美元。根據彭博智庫的數據,分析師曾預計Roctavian到2027年的銷售額將達到約22億美元,但他們對該年的平均預測已下調至約8億美元。
Hardy在會議上表示,進展“比任何人預期或希望的都要慢”。他説,這款產品提供了“一個非常明確、引人注目的價值主張”,但需要時間。“—與 Tom Contiliano**閲讀下一篇: 最神秘的長壽實驗室終於開放大門