疫苗史上重大技術飛躍,實際應用不只是新冠肺炎!_風聞
已注销用户-2022-01-17 15:33
近期,奧密克戎(Omicron)讓世界各國都人心惶惶。
據科技日報報道,去年底,美國哥倫比亞研究人員與中國香港大學科學家合作,他們將疫苗接種產生的抗體與活病毒和實驗室構建的模擬奧密克戎假病毒相結合,測試了抗體中和奧密克戎的能力。
從結果看,現有疫苗和抗體對奧密克戎效果不容樂觀:莫德納、輝瑞-生物科技、阿斯利康和強生四種疫苗的完全接種者的抗體,中和奧密克戎變異株的效果明顯比其中和祖先病毒的效果差。不過研究人員仍建議人們接種一次加強針,因為接種者依然會因免疫力的提高而受益,它仍然是我們對抗疫情的有力武器。
在測試中,前兩者都為mRNA疫苗,這****種疫苗從誕生起,就得到了全世界的關注。
其實新冠肺炎之外,mRNA疫苗技術還能用於一些目前尚無有效疫苗,或現有疫苗不理想的疾病疫苗研發。比如艾滋病,採用mRNA技術的艾滋病疫苗臨牀試驗已於2021年8月啓動,結果有望在2023年出爐。
我國也一直關注mRNA疫苗技術的發展,一些國內企業積極引進海外產品、技術同時,也在嘗試“兩條腿走路”,進行自主研究和開發的探索。
不禁令人好奇,這個技術究竟有何出類拔萃之處呢?
文丨Klaith 新藥臨牀開發工作者、前神經內科醫生
編輯丨王乙雯 瞭望智庫
本文為瞭望智庫原創文章,如需轉載請在文前註明來源瞭望智庫(zhczyj)及作者信息,否則將嚴格追究法律責任。
1980 年,世界衞生組織(WHO)向全球宣佈,肆虐全球數千年的嚴重傳染病天花被徹底根除,而這歸功於醫學界的偉大發明:疫苗。
作為預防疾病的重要手段,疫苗已得到廣泛應用。尤其新冠肺炎疫情暴發以來,疫苗接種始終處於世界各地疫情管控政策的關鍵位置,再次彰顯其在公共衞生領域的重要性。
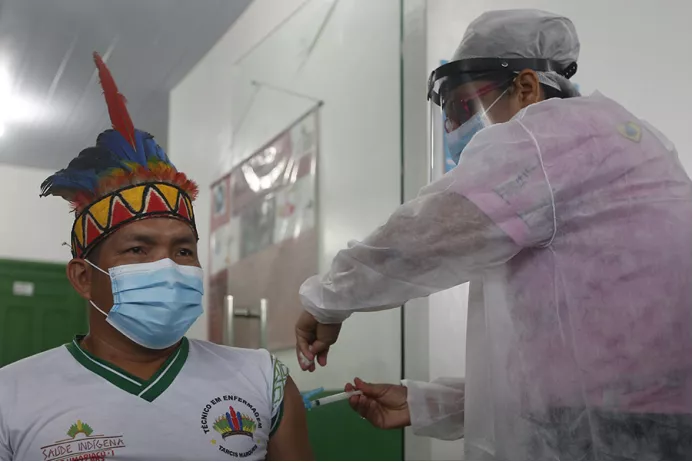
1月19日,巴西亞馬孫州塔巴廷加市,醫護人員為一名原住民接種中國新冠疫苗。圖|新華社
我國是全球首批自主開發新冠疫苗成功的國家,除了用於國內疫情防控,我們的國產疫苗還漂洋過海支持了其他國家、地區的抗疫工作。我國最早問世的兩款新冠疫苗均為滅活疫苗,這是一種歷史悠久、發展成熟的技術:通過物理或化學手段殺滅致病微生物,再將殺滅微生物的全部或部分內容製成疫苗。
然而本次疫情中,另一項新興疫苗技術才是全世界矚目的焦點——mRNA(信使核糖核酸)疫苗,堪稱疫苗史上的重大技術飛躍**。**新冠mRNA疫苗不僅在試驗、實用階段展現出振奮人心的效果,更成就了一批BioNTech、Moderna這樣的新鋭生物技術企業,撼動了傳統的世界疫苗產業。
全球知名科技媒體《麻省理工學院技術評論》(MIT Technology Review)2021 年發佈的年度十大突破性技術名單中,mRNA疫苗榜上有名。儘管新冠肺炎疫情前,mRNA疫苗從未實際應用,但其理論優越性使人們相信,這****一技術有望變革醫療格局。
我國也高度重視mRNA疫苗發展動向,已經積極組織資源投入mRNA疫苗研究開發工作,爭取儘快將這項潛力巨大的新技術本土化。
1
一鳴驚人
信使核糖核酸(mRNA)最早發現於上世紀60年代,是脱氧核糖核酸(DNA)生產蛋白質的中間產物。人類的遺傳信息以DNA形式存儲,以其為模板生產各類蛋白質,才能進行維護身體、輸送物質、新陳代謝、調節功能等生理活動。細胞會以DNA為模板先生成mRNA,接着再根據mRNA合成對應的蛋白質,完成從DNA到蛋白質的整個流程。

2020年1月29日,上海,工作人員在研究新型冠狀病毒mRNA疫苗。圖|新華社
根據 mRNA 的作用,科研人員大膽設想:**如果將特定mRNA分子注射入人體,細胞攝取後,是否能夠在體內產生對應蛋白質呢?**如果這種蛋白質與滅活疫苗成分一樣,可以引起對目標緻病微生物具有防護作用的免疫反應,是否能夠實現疫苗功能呢?
**上世紀80、90年代,這個念頭被證實並非空想。**1987年,科研人員將脂肪包裹的mRNA分子注射入分離到體外的人體細胞,確實能夠生產蛋白質。1990 年,科研人員又將mRNA分子注射入動物體內,檢驗到活體動物產生的相應蛋白質;兩年之後進一步證實,這樣生成的蛋白質同樣能夠發揮生理作用。至此,mRNA疫苗概念得到驗證。
然而,與絕大多數科學技術相同,mRNA疫苗技術的研究、應用之路並不平坦,最初即面臨了嚴重難題:從體外注射的mRNA分子穩定性差,在體內幾分鐘便徹底分解,根本無法通過它們產生足夠蛋白質;同時還會引發人體劇烈免疫反應,直接威脅健康。
因此,mRNA疫苗一直未被大眾熟知,只能在實驗室裏默默發展。過去十餘年間,隨着一系列生物技術日趨成熟,mRNA疫苗的技術難點被逐一解決,一部分比較成熟的產品進入臨牀研究階段。
2020年初,**新冠肺炎疫情席捲全球,科研人員突然意識到這是mRNA疫苗應用的絕佳場景。**憑藉技術的獨特優勢,科研人員獲知新冠病毒基因信息後不到 48小時就完成了疫苗設計,不到6周就生產出了動物實驗所需的疫苗成品。
2
優勢在哪?
新冠mRNA疫苗從臨牀試驗起就備受矚目,不僅是生逢其時,更因為技術本身極具潛力,或許能夠補足現有疫苗短板,甚至擴展至腫瘤治療等領域。
傳統疫苗從產品設計到臨牀試驗完成上市,通常需要數年至十數年。新冠 mRNA疫苗整個流程不到兩年,傳統疫苗技術的速度難以望其項背。這得益於其開發機制:疫苗研究人員只需識別出能夠引起關鍵免疫反應的蛋白質,反向轉化為簡單的mRNA分子即可——實際生產則完全交給人體細胞,無需再絞盡腦汁考慮人體外的複雜工藝。
即使新冠病毒發生明顯變異,原來的關鍵蛋白質出現差異,mRNA疫苗技術理論上仍然可以根據新的蛋白質信息,通過修改舊疫苗 mRNA 內容,實現針對變異病毒疫苗的快速更替。
進入生產階段後,**mRNA疫苗技術允許人類第一次像組裝汽車零件那樣工業化生產疫苗,擺脱傳統疫苗必須依賴活生物體或細胞生產的繁複技術。**mRNA疫苗幾乎所有生產原料都已商業化供應,可以快速、低成本地規模化生產。儘管部分原料產量偏低、成本偏高,由於新冠肺炎疫情中需求大幅增長,供應能力也正逐步改善。
過去三十年圍繞mRNA疫苗的技術發展,始終聚焦其有效性、安全性。**經過化學修飾、改造的mRNA分子,進入人體後更穩定,生產蛋白質效率更高,卻不影響其本來生理分解過程,代謝產物對人體無額外毒性。**藥物遞送(delivery)技術的改進(如當前主流的脂質微球包裹mRNA分子),提高疫苗效果同時,降低了人體對mRNA分子本身的免疫反應,增強其安全性。
mRNA疫苗在開發、生產便利性、有效性、安全性上的優勢,固然與其本身特性密不可分,同樣離不開科研人員方方面面精益求精的執着追求。正是依靠這些優勢,mRNA 疫苗不僅能夠有效、安全,還成為最適合應對新發致病微生物導致傳染病疫情的疫苗技術。
3
mRNA疫苗國產化
2020年初新冠mRNA疫苗初露端倪,國內就有製藥企業敏鋭覺察到mRNA疫苗技術的前景,立即與領頭羊企業開展合作。同時,一些藥企也陸陸續續加入自主研究開發新冠mRNA疫苗的行列,僅2020年初就已有 10 餘家企業投身其中,其中不乏行業巨頭。

2021年11月7日,在上海第四屆中國國際進口博覽會上展示的復星醫藥和BioNTech合作研發新冠 mRNA 疫苗。圖|新華社
然而,生物醫藥行業的技術發展、產品開發向來困難重重。這10餘家雄心勃勃的製藥企業,只有三家企業疫苗進入臨牀試驗階段。
進展最快的,去年中已啓動國內、國際兩項Ⅲ期臨牀試驗,成功即可申報上市。相關企業在雲南玉溪建設的mRNA疫苗模塊化廠房去年下半年也正式交付,標誌國內企業已經基本掌握mRNA疫苗研究、開發、生產的全過程。另外兩家製藥企業的新冠mRNA疫苗,則仍處於臨牀試驗早期階段。
除此以外,mRNA疫苗生產原料的中上游企業抓住國內mRNA疫苗契機,迅速發展起來。雖然它們仍存在經驗不足、產業鏈欠完善、短期供應跟不上等問題,但隨着政策、資源傾斜,以及本土技術成熟,相信能很快解決。
4
縮短差距的大好機會
有人説,我國防疫措施積極,國產疫苗有效,已經向全世界遞交了一份成績優秀的抗疫答卷,所以不再需要關注mRNA疫苗技術了。
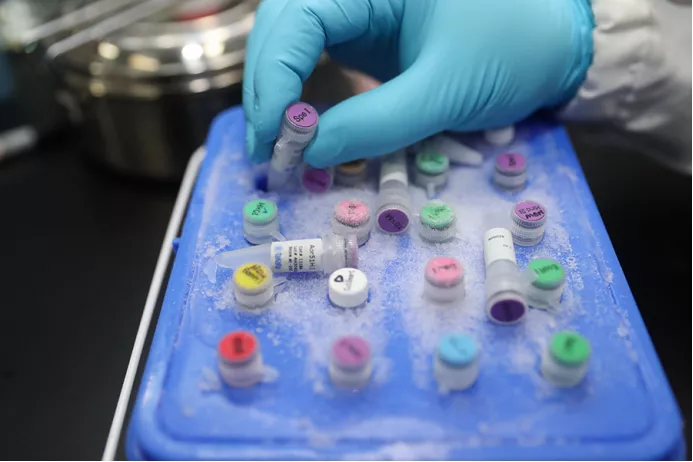
1月29日,上海,工作人員在演示新型冠狀病毒mRNA疫苗研發實驗過程。圖|新華社
其實,我們不一定要用功利的眼光去看待mRNA疫苗技術。
今天的 mRNA疫苗,歷經數十年發展才真正為人類所用,背後是許許多多緊密關聯的生物技術齊頭並進、優勝劣汰的結果。**這些生物技術不僅可以服務 mRNA疫苗產業,也可以為mRNA疫苗以外的生物技術行業提供支持和幫助。**正如上文提及,mRNA疫苗技術本土化,已經激勵了一大批中上游企業成長壯大。推動我們自己的mRNA疫苗,本身也在促進我們的生物產業發展。
此外,由於mRNA疫苗根據關鍵蛋白質可反推、設計、合成,無須耗費大量資源利用活體生物或細胞合成,本身又可以引發全面有效的人體免疫反應,有可能為一些目前尚無有效疫苗,或現有疫苗不理想的疾病——如艾滋病、流行性感冒、寨卡(Zika)病毒、埃博拉(Ebola)病毒——開發疫苗。
mRNA疫苗技術還**為腫瘤患者提供了又一個腫瘤免疫治療的形式****。**國外已有醫藥企業、醫療機構,採集患者腫瘤標本,尋找其細胞表面的關鍵蛋白質,逆向轉化為mRNA分子,量身定製成腫瘤疫苗,用於治療。科研人員甚至通過 mRNA疫苗技術,嘗試令接種者體內製造抗體治療疾病,取代從體外注射的單克隆抗體藥物。
由此可見,**mRNA疫苗技術雖然應新冠肺炎疫情而生,但實際應用卻不侷限於新冠肺炎,擁有更廣闊空間,潛力大大超出傳統疫苗。**有人預言:新冠肺炎之後,世界將迎來一個嶄新的時代;而mRNA 疫苗首次獲批上市,也開創了生物醫藥技術的嶄新時代。
新技術仍需時間充分驗證,但積極、審慎地進入新技術領域,不失為我們縮短與西方發達國家醫藥產業差距的大好機會。