結核,被遺忘的瘟疫_風聞
返朴-返朴官方账号-关注返朴(ID:fanpu2019),阅读更多!2022-03-25 16:02
如今,卡介苗問世已過百年,仍是目前唯一被批准用來抗擊結核病的疫苗。但結核這個惡魔卻從來沒有被徹底打敗過。幾十年來,科學家一直在努力開發更好的選擇。在試驗了幾十種方法,經歷了多次臨牀失敗後,研究人員表示,第二種肺結核疫苗有望上市。豐富的渠道,大量的候選疫苗,讓戰勝結核充滿了希望。
撰文 | Anthony King
編譯 | 鹹姐、Idobon
1921年7月18日,一名嬰兒在巴黎呱呱墜地。他的母親分娩不久便死於結核分枝桿菌(Mycobacterium tuberculosis,Mtb)的感染,照顧他的祖母也患有結核病(tuberculosis ,TB)。為了保護這名新生兒,醫生為他接種了一劑活的牛分枝桿菌,這便是人類歷史上第一名接種卡介苗的嬰兒。
如今,全球每年有1億多新生兒接種卡介苗,主要集中在發展中國家。這一舉措可以挽救數萬人的生命。但是,卡介苗提供的保護仍然是不完全的,結核病仍然是這個星球上的頭號傳染病殺手。據估計,在過去的200年裏,結核奪走了約10億人的生命,僅2019年就有140萬人命喪於此。現在,醫生們擁有可以治療結核病的抗生素,卻也使得這個“巨大的負擔”變得更加不幸——因為我們似乎開始忘記,結核病是一種瘟疫。
卡介苗的缺點
兒童感染結核常見於肺部以外,可能以粟粒性結核和結核性腦膜炎的形式出現。前者會影響多個器官,若不及時上抗生素治療幾乎就是致命的;後者則是因為大腦和脊髓周圍的膜受到了感染。卡介苗最大的優點就是可以預防這些感染。新生兒接種卡介苗,能夠可靠地預防結核桿菌在兒童間的傳播。
而超過90%的結核病例則是青少年和成年人,表現為我們熟知的肺結核。這是一種嚴重的肺部疾病,可引起胸痛或咳血。卡介苗為肺部提供了更多樣化的保護,但出於某些原因,比起其它結核,卡介苗預防肺結核的效果卻差一些。
奇怪的是,卡介苗對青少年和成年人的保護力度存在地域差異:在斯堪的納維亞和其他高緯度地區,卡介苗有很好的效果,但對靠近赤道的人羣保護力卻較弱。一個最受認可的解釋是,赤道地區有一些不同種類的分枝桿菌,它們可以觸發人體產生免疫記憶,從而使身體能夠識別出卡介苗,並減少卡介苗的複製。這種解釋有一個有力的流行病學證據:世界上卡介苗效果不佳的地區,人們接觸非結核分枝桿菌的幾率往往也是最高的。
更復雜的是,結核分枝桿菌可以在人體內潛伏數十年。全球大約有20億人可能感染了這種病菌,當時機一到,例如免疫系統受到抑制時(艾滋病患者中很常見的情況),結核桿菌就會激活,使人生病,並很容易通過空氣傳播感染其他人。
理解這些動態過程的關鍵在於瞭解免疫反應。結核分枝桿菌與人類已共存了數千年,它已經進化出了一套“分子把戲”來逃避我們的免疫雷達,甚至在被檢測到時還能夠減弱免疫反應以求自保。伴隨着人們的呼吸,空氣中的結核桿菌進入肺部,吸引了在肺裏“巡邏”的免疫細胞:肺泡巨噬細胞。
結核分枝桿菌有一層蠟狀的厚層黴菌酸構成的囊狀結構,不易被免疫系統識別。當巨噬細胞認出併吞噬了結核桿菌,躲在“蠟囊”中的結核桿菌可以阻止吞噬溶酶體成熟,這樣它們就不會被殺滅,甚至還能複製。同時,結核桿菌還會干擾抗原遞呈,使“前線”的免疫細胞無法向輔助T細胞傳遞結核桿菌的信息,推遲保護性T細胞做出反應,並限制T細胞啓動後的效應。
可以説,巨噬細胞無意中為結核桿菌提供了它們所渴望的“庇護所”——在巨噬細胞內,結核桿菌正好可以免受抗體的襲擊。
至此,人體最終將結核分枝桿菌隔離在一種叫做“肉芽腫”的免疫細胞羣中,猶如一顆“定時炸彈”,等待你的防禦系統崩潰的那個最佳時機。
當然,並非所有情況都很嚴重。大多數感染了結核桿菌的人都不會發病,只有5%-15%的人會患上結核病。畢竟結核與人類之間經歷瞭如此長時間的鬥爭和博弈,已經建立了輸贏的平衡。
徒勞的探尋:結核免疫的指標究竟是什麼?
卡介苗雖然已經用了一百年,但其實科學家並沒有完全弄清楚它究竟是怎樣調動免疫系統保護孩子們的,也沒有弄清楚成年人到底要產生什麼樣的免疫反應,才算接種成功。與大多數疫苗一樣,卡介苗在刺激抗體產生這方面比激發強大的T細胞反應這方面要強得多。幾乎所有的疫苗都是通過產生中和抗體來起作用的,但是對於結核而言,中和抗體的作用似乎遠遠不夠。
保護性關聯值(correlates of protection,CoP)是評估疫苗效力的一組指標。只有當數千人規模的安慰劑對照試驗(即臨牀3期)取得成功時,才可能挖掘、制定出這些指標。然而,在結核病患者的血液中,卻找不出任何指標能表明“這位患者已經打過疫苗、受到疫苗保護”。
多年來,科學家們一直認為,卡介苗所引發的T細胞的強烈反應是抵抗結核病的關鍵,它能消滅感染了結核桿菌的細胞。大量研究也顯示,CD4+ T細胞(也叫TH1細胞)對控制感染、預防傳播性疾病是必不可少的。然而,CD4+ T細胞越多,卻未必等於抗結核病的能力越強,因此難以將它的丰度作為評估疫苗效力的指標。另外,近年來,人們認為產生促炎細胞因子的輔助性T細胞17(也稱Th17細胞)也可以保護人體。
為了研製一種能夠有效招募並激活T細胞的疫苗,牛津大學的Helen McShane團隊利用一種改良的安卡拉牛痘病毒(MVA)作為載體來傳遞結核抗原,命名為“MVA85A疫苗”。據McShane回憶,在早期臨牀試驗中,MVA85A疫苗激發了理想中正確的免疫反應——CD4+ T細胞被誘導了出來,分泌了干擾素γ、腫瘤壞死因子和白細胞介素-2。然而,南非的一項嬰兒試驗缺表明,加種MVA85A疫苗並沒有顯示出比僅接種卡介苗更有效的抗結核效果。這可能意味着,研究人員搞錯了方向、找錯了CoP指標。最終,McShane團隊總結道, MVA85A疫苗誘導的T細胞反應水平不足以增強卡介苗接種後的保護作用。
倫敦衞生與熱帶醫學學院的免疫學家Hazel Dockrell認為,我們不應忽略結核病首先是一種呼吸道感染,然而現在的研究卻幾乎總是盯着血液中發生了什麼。這並不能幫助我們瞭解肺裏發生了什麼。也許肺裏存在着可能對抗結核的關鍵特殊細胞呢。
卡介苗
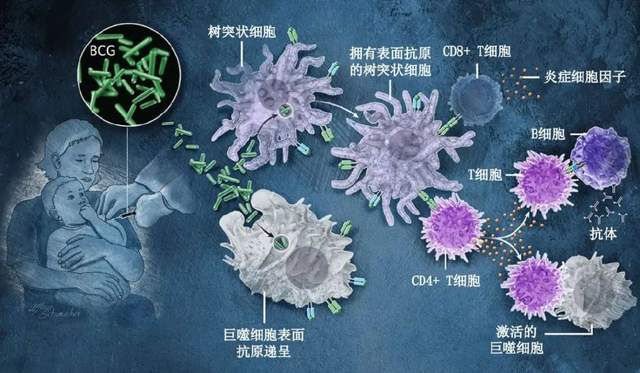
正在研發中的結核疫苗
目前已有十幾種結核病疫苗正在進行臨牀試驗,雖然新的結核疫苗可能還無法防止感染,但有些疫苗已經可以阻止帶菌者發展為結核病。必須承認的是,阻止感染一直是疫苗成功的“聖盃”,但這其實是個非常非常高的標準,因此,將標準稍微變通一下也未嘗不可——比如,阻止感染者發展為結核病,就可以作為一個評判疫苗標準。畢竟,在幾乎所有的結核病疫苗試驗中,受試者都接種過卡介苗,並感染了潛伏的結核病。
領跑的在研疫苗
目前有兩種候選疫苗正在進行臨牀3期試驗,還有八種疫苗緊隨其後,處於臨牀2期試驗階段。再往前,有三種疫苗處於1期試驗階段(未顯示),還有少數臨牀前候選疫苗正在爭取進入人體試驗階段。
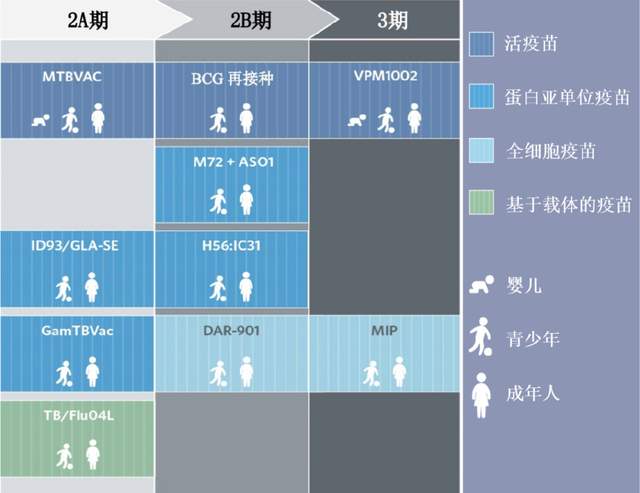
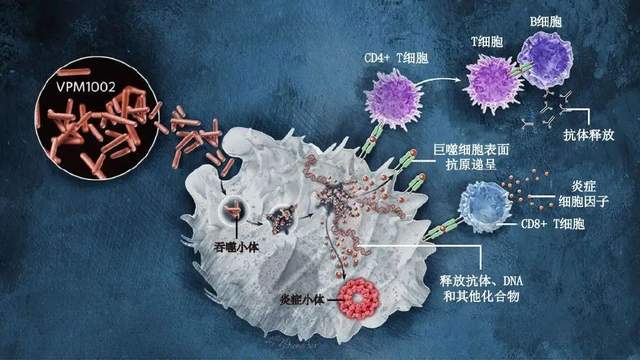
VPM1002:活的減毒卡介苗,含有另一種細菌的成孔蛋白,可使抗原和分枝桿菌DNA從吞噬體進入細胞質
BCG再接種:再注射一針卡介苗
MTBVAC:帶有毒性基因突變的、活的、遺傳上減弱的結核分枝桿菌(是此類疫苗中第一個也是唯一一個進入臨牀試驗的)
蛋白亞單位疫苗
M72 + ASO1:由兩種結核分枝桿菌抗原和一種佐劑組成的重組融合蛋白
H56:IC31:由兩種早期分泌蛋白、一種潛伏蛋白以及一種佐劑組成的蛋白質疫苗
ID93/GLA-SE:四種結核分枝桿菌毒性抗原與一種佐劑的融合
GamTBVac:融合兩種結核分枝桿菌抗原和一種佐劑的亞單位疫苗
全細胞疫苗
DAR-901:布氏桿菌(Mycobacterium obuense)的滅活製劑,不引發疾病
MIP:由分枝桿菌 M. indicus pranii組成的滅活疫苗,該菌生長迅速,不會引起疾病
基於載體的疫苗
TB/Flu04L:經鼻給藥、含有結核分枝桿菌兩種抗原、減毒、活流感病毒
大多數結核病候選疫苗都是在青少年和成年人中進行試驗。不過有兩種疫苗值得關注,那就是處於2A期臨牀的MTBVAC疫苗和處於3期臨牀的VPM1002疫苗。它們可以同時在成年人以及嬰兒、新生兒中進行試驗,並且可能對免疫缺陷的艾滋病兒童特別有用。當然,如果我們能夠阻止青少年和成年人感染結核病,就不用擔心兒童對結核疫苗的需求了。
目前,幾乎人人都在談論的候選疫苗是葛蘭素史克(GSK)正在研發的蛋白質亞單位疫苗——M72疫苗。該疫苗包含來自結核分枝桿菌的兩種蛋白的融合,採用了一種名為AS01的佐劑(GSK曾將這種佐劑用於轟動一時的帶狀皰疹疫苗和處於行業領先的瘧疾候選疫苗)。儘管M72疫苗在非人靈長類動物身上的作用看起來並不樂觀,但在最近的一次涉及肯尼亞、南非和贊比亞3000多名成年人的試驗中,它在3年內將肺結核的發病率降低了54%。
卡介苗是一種活的、可複製的載體,類似於自然感染結核桿菌的“緩慢進程版”。雖然卡介苗在青少年時期的保護作用減弱了,但畢竟在整個兒童時期都能有效抵禦結核病。而M72疫苗的成分主要是一些蛋白質,所以早期遭到了一些學者的懷疑。他們認為,像卡介苗這種可提供足夠長的免疫期以避免自然感染的疫苗才是最合適的結核疫苗。但M72疫苗提供了持續3年的保護,證明了這種想法的侷限性。
華盛頓大學傳染病科學家Thomas Hawn雖然沒有參與M72疫苗的研發,但他認為M72疫苗的效果歸功於疫苗的佐劑。AS01佐劑可以觸發一種名為toll樣受體4(TLR4)的先天免疫受體,從而產生強大的免疫反應,除了產生抗體的B細胞外,還會召喚T細胞。“從前,我們還沒有那麼高效力的佐劑。如今,有了新的佐劑,我們以更微妙的方式觸發不同免疫反應的能力大大提升了。”
M72蛋白亞基疫苗
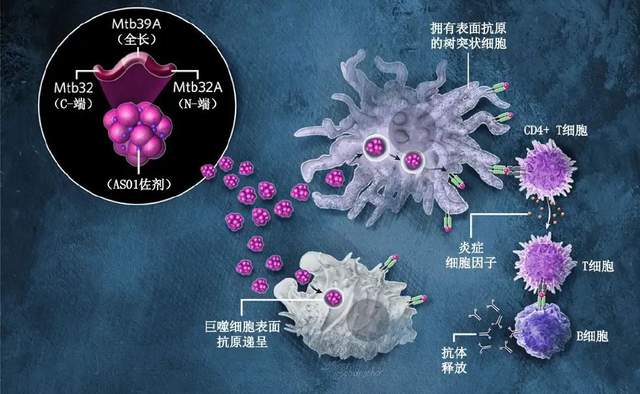
但不容忽視的是,M72目前的試驗規模很小,安慰劑組僅含有26例結核患者,疫苗組也只有13例結核患者。毫無疑問,想要尋求監管機構的緊急使用授權,必須先進行萬人規模的試驗。
與此同時,丹麥國立血清研究所正在開發兩種亞單位疫苗,其主要候選疫苗H56(由三種抗原和一種新型佐劑組成)正在坦桑尼亞和南非進行2B期臨牀試驗。另一種名為H107的亞單位疫苗,含有8種結核分枝桿菌的特異性抗原,由於這些抗原不是卡介苗所共有的,因此H107疫苗不會與卡介苗發生交叉反應,這就意味着二者可以聯合使用。
但是,也有不少含佐劑的蛋白質亞單位疫苗半路夭折。它們在早期和中期試驗中顯得很有潛力,卻最終失敗了。一些科學家因此對亞單位疫苗失去了興趣。澳大利亞昆士蘭詹姆斯·庫克大學的疫苗學家Andreas Kupz就是其中之一,他轉而認為採用原始卡介苗的方法制作的活疫苗更具有潛力。例如,比爾和梅琳達·蓋茨醫學研究院正在進行一項試驗,為南非10-18歲的人注射增強劑量的卡介苗。一開始,大家認為這種方法肯定無效,但試驗結果卻表明,在南非青少年中,此法可以預防45%的人感染繼發性結核,且即使感染了6個月內也可痊癒。值得一提的是,這種方法並不能阻止感染結核桿菌(血檢呈陽性),但有更多的人最終結核轉陰了,感染最終被清除了。
也有一些新的活疫苗正在研發中,其中走在最前列的是VPM1002疫苗。這是一種轉基因卡介苗,目前正在進行3期臨牀試驗,由柏林馬克斯·普朗克感染生物學研究所的Stefan Kaufmann牽頭。Kaufmann表示,他們並不認為卡介苗很糟糕,但是希望可以改善新生兒卡介苗,使其最好也能用於成年人和青少年。他們為疫苗添加了李斯特菌產生的一種致孔蛋白(李斯特菌溶血素O)的基因。一旦結核桿菌被“前線”免疫細胞(如巨噬細胞)吞噬,它就會被隔離到吞噬小體中,而李斯特菌溶血素O則能穿透吞噬小體膜,泄露VPM1002來源的分子泄漏。這些分子出現在細胞表面,誘導CD8+ T細胞攻擊感染細胞,並使DNA逃逸,觸發促炎途徑。
VPM1002全細胞疫苗
另一種候選活疫苗與卡介苗的區別更大,因為它使用的是結核分枝桿菌本身。有一種觀點認為,更直接地模擬自然感染可能是疫苗的成功之路。西班牙薩拉戈薩大學的研究人員刪除了結核分枝桿菌的兩個致病基因以使其更安全,從而研發了改良版的MTBVAC疫苗, 現在正處於2a期試驗中。MTBVAC所模擬的過程可能比卡介苗更接近於真實的結核感染,並能誘導更加相似的記憶免疫反應,從而起到更好的保護作用。
還記得本文開頭提到的卡介苗的保護作用有地域差別的現象嗎?上文提到,目前最有利的證據是:赤道附近的分枝桿菌數量越多,似乎就越容易降低卡介苗對成年人的效力。這意味着,同樣的現象很可能會在這些新的活分枝桿菌疫苗中重演。確實,已有證據表明,對環境中的分枝桿菌的免疫反應會干擾卡介苗的效率,那麼現在要關心的就是,這一點在多大程度上會成為MTBVAC和VPM1002的問題?將這些疫苗接種給終生接觸分枝桿菌的老年人會發生什麼不一樣的事情嗎?如果分枝桿菌之間的交叉反應確實會影響疫苗效力,那麼蛋白亞單位疫苗或基於載體的疫苗(如McShane團隊目前正在研究的疫苗)可能是更好的選擇,畢竟“不要把雞蛋都放在一個籃子裏”。
消滅結核病
要想重振結核疫苗,研究人員必須考慮到,卡介苗不只可以預防結核病,還能激發免疫系統,抵禦更廣泛的呼吸道疾病,乃至敗血症。當然,研究人員在卡介苗廣泛應用後不久就觀察到了這種非特異性保護作用:當時卡介苗接種不僅減少了兒童的結核死亡,還減少了其他原因造成的死亡。目前,卡介苗還被用於早期膀胱癌的免疫療法:將其直接注入膀胱,可以觸發患者的免疫系統攻擊腫瘤。相應地,VPM1002疫苗在臨牀試驗中也顯示出治療膀胱癌的潛力。
在過去十年中,研究人員逐漸揭示了這些非特異性效應的機制,發現它涉及先天免疫細胞的基因重組,這種現象稱為訓練免疫(trained immunity)。從本質上來説,卡介苗會給細胞留下表觀遺傳學印記,以便它們對隨後的其他感染做出反應。一些科學家甚至推測,這種免疫防禦的通用機制足以(基本)解釋卡介苗為什麼能對抗結核。雖然目前大多數正在研發的結核疫苗都是專門針對肺結核進行試驗的,但是默多克兒童研究所及墨爾本大學的結核疫苗研究員Nigel Curtis正在領導一項跨國試驗,調查接種過卡介苗的醫務人員,看看卡介苗是不是也能影響新冠病毒感染。
疫苗接種
20世紀20年代,卡介苗是口服的;很快,醫生們就開始皮下注射(這已經成為近一個世紀以來的標準做法)。不過現在,研究人員正在考慮新的接種方式,比如直接送入肺部和靜脈注射。
牛津大學的疫苗研發人員Helen McShane表示,他們正在努力嘗試將疫苗送入肺部,因為這是結核進入身體的渠道。一些動物實驗數據表明,入肺是最好的保護方式,當結核疫苗通過氣霧劑接種時,肺部和血液中的免疫反應更為強烈。
澳大利亞昆士蘭詹姆斯·庫克大學的疫苗科學家Andreas Kupz也表示,當卡介苗通過鼻腔或噴霧直接進入肺部時,駐留的記憶細胞將被激活——局部記憶T細胞,也可能是記憶B細胞,時刻準備着應對特定病原體的再次出現。
這些細胞似乎也受到卡介苗靜脈注射的刺激,Nature雜誌最近的一項研究報告指出,與接受鼻腔和皮內給藥的猴子相比,靜脈接種卡介苗的恆河猴的CD4+和CD8+ T細胞的應答更佳。McShane認為,靜脈注射卡介苗可以讓我們更多地瞭解那些免疫反應是必需的,這樣我們就能有針對性地設計疫苗來誘導這些反應。
目前,結核疫苗的開發因新冠疫情而變得複雜。接受Science雜誌採訪的專家指出,一些結核疫苗試驗已經推遲或放緩。如果不是新冠疫情暴發,M72疫苗的試驗應該已經完成。此外,在大流行期間,很可能存在結核病例沒有上報、甚至治療滯後的情況。針對新冠病毒的全球封鎖破壞了“終止結核”的計劃。
事實上,根據非政府組織“遏制結核病夥伴關係”(Stop TB Partnership)的數據,結核病例最多的國家中,有9個在2020年結核病感染的診斷和治療方面出現了數量大幅下降,降幅從16%到41%不等。該組織估計,新冠暴發12個月,抵消了全球抗擊結核 12年所取得的進展。由於新冠疫情的干擾,2020年結核病的官方病例數和死亡人數可能會下降,但是2020年結核病死亡人數可能會超過新冠,因為那些未確診的結核病患者將無法得到應有的治療。
全球95%以上的結核病死亡發生在低收入至中等收入國家,倫敦衞生與熱帶醫學學院的一項研究估計,基本的社會支持可以將結核病負擔減少85%。人類已經適應了結核的存在,但惡劣的生活條件、貧困、過度擁擠、艾滋病毒導致的免疫功能低下,都會導致更多的疾病。世界衞生組織表示,要實施現有的結核干預措施,還存在33億美元的資金缺口。
毫無疑問,疫苗可以成為防治結核全球戰略的關鍵部分。倘若我們有一種疫苗能夠阻止接種者因感染結核桿菌而發展成結核病,甚至,能完全阻止感染,那一定是了不起的成就。
雖然新冠疫情暫時阻礙了結核疫苗的研發,但是,新冠疫苗的研發工作中也有望出現一些“化學反應”。例如,一些研究人員就認為,對免疫系統具有強烈刺激作用的mRNA疫苗不僅非常靈活,而且具有極高的免疫原性,正適用於靶向結核病。
面對傳染病中的“頭號殺手”,我們需要一種更好的結核疫苗。然而,無論答案在哪裏,研究人員都一定會找到它,並勇往直前,推進臨牀項目的進行。
本文經授權編譯自TheScientist 在線雜誌,鏈接地址:
https://www.the-scientist.com/features/tuberculosis-the-forgotten-pandemic-68894
特 別 提 示
1. 進入『返樸』微信公眾號底部菜單“精品專欄“,可查閲不同主題系列科普文章。
2. 『返樸』提供按月檢索文章功能。關注公眾號,回覆四位數組成的年份+月份,如“1903”,可獲取2019年3月的文章索引,以此類推。
版權説明:歡迎個人轉發,任何形式的媒體或機構未經授權,不得轉載和摘編。轉載授權請在「返樸」微信公眾號內聯繫後台。