初窺“AI製藥”:BAT們的下個萬億試煉場_風聞
锦缎-锦缎官方账号-为上市公司提供知识产权解决方案2022-06-06 08:22
本文系基於公開資料撰寫,僅作為信息交流之用,不構成任何投資建議。

眾所周知,創新藥研發迄今仍逃不開“雙十定律”——研發費用10億美元,研發週期10年。高投入與高風險,不僅考驗投資人的耐性與運氣,更令憧憬於改變產業格局與人類健康命運的創新藥公司與科學家,長期徘徊於“一念天堂一念地獄”之間。
就在5月27日,天境生物(NASDAQ:IMAB)公佈其“CD73抗體尤萊利單抗藥物”的中國II期臨牀研究數據。數據顯示,在19例可評估療效患者中,5 例達到部分緩解(PR),客觀緩解率(ORR)為 26%;9 例疾病穩定(SD),疾病控制率(DCR)為 73.7%。
有評論人士認為,兩藥聯用26%的ORR,可能單用PD-1也不比這個數據差多少,這吃了和沒吃有啥區別嗎?二級市場隨之投出不信任票,天境生物市值本來就日漸萎靡的市值被一刀砍翻,當日重挫26.88%。這則案例,也再度印證了創新藥研發之難,對於醫藥公司而言如同一場“生死劫”。

圖:天境生物市值 來源:雪球
如何能通過技術革命,“更快、更好、更強”地進行新藥研發,從本質上實現醫藥公司“逆天改命”式救贖?在這個問題上,除了祈禱,更多的創新藥公司正將希望寄託在“AI‘製藥’”上——
隨着賽諾菲與英國藥物研發AI技術服務提供商Exscientia達成了一筆52億美元的AI製藥大單;英矽智能,半年內兩次宣佈發現新藥,並率先進入臨牀試驗新階段;阿斯利康、默克、輝瑞、梯瓦等製藥巨頭聯合建立的AI藥物研發實驗室AION Labs宣佈正式啓動……各界無不期待“AI‘製藥’”重新定義製藥流程,為世界帶來一場巨大變革。
那麼,AI製藥到底是什麼?
01
AI如何“製藥”?
19世紀以前,人們主要利用天然植物、動物、礦物直接用於部分疾病的治療。例如《本草綱目》記錄了各種動物和人體組織等“奇葩”藥材。這個時期,只要是自然界存在的物質,人們都拿來試試能不能做成藥。
20世紀隨着隨着藥理學和有機化學等科學的發現,人們可以合成一些自然界不存在的全新化合物。這些藥物以人體為研究對象,以人體代謝和作用機制為抓手,研究出了抗生素、維生素、磺胺類藥物、精神病藥物、麻醉鎮痛、疫苗等的新藥。
20世紀60-80年代,一些與疾病相關的酶、激素、神經遞質的受體和底物被發現。物質分析檢測技術和計算機的發展應用。人們開始嘗試擺脱隨機發現轉向到主動編輯化合物。
20世紀80年代之後,基因組學、蛋白質組學、生物信息學等現代分子生物學科得到發展,以靶點為基礎的新藥研發模式得到應用。
如今,新藥物發現的大致過程需要先發現靶點-驗證靶點-發現先導物-優化先導物,從數十萬個化合物中選出幾個候選藥物,最後再進入臨牀試驗環節。靶點可以理解為不同疾病關鍵點構成的“鎖”,人們在眾多藥物分子可能性中,設計和篩選最合適的分子作為“鑰匙”去解鎖。

人們利用計算機輔助製藥(CADD)來評估分子多樣性、構建化合物庫、開展基於分子相似性的篩選。建立大型化合物庫與生物靶標自動對接軟件,並分別打包變成研發系統的組件。
CADD的應用,一方面能夠允許研究者減少實驗來評估化合物的有效性,直接在電腦上就能設計和“改造”分子。但另一方面,這些分子仍需要人工搭建生成,並與資料庫比對。這些前期工作需要從上萬個化合物中一個個篩選無異於“大海撈針”。
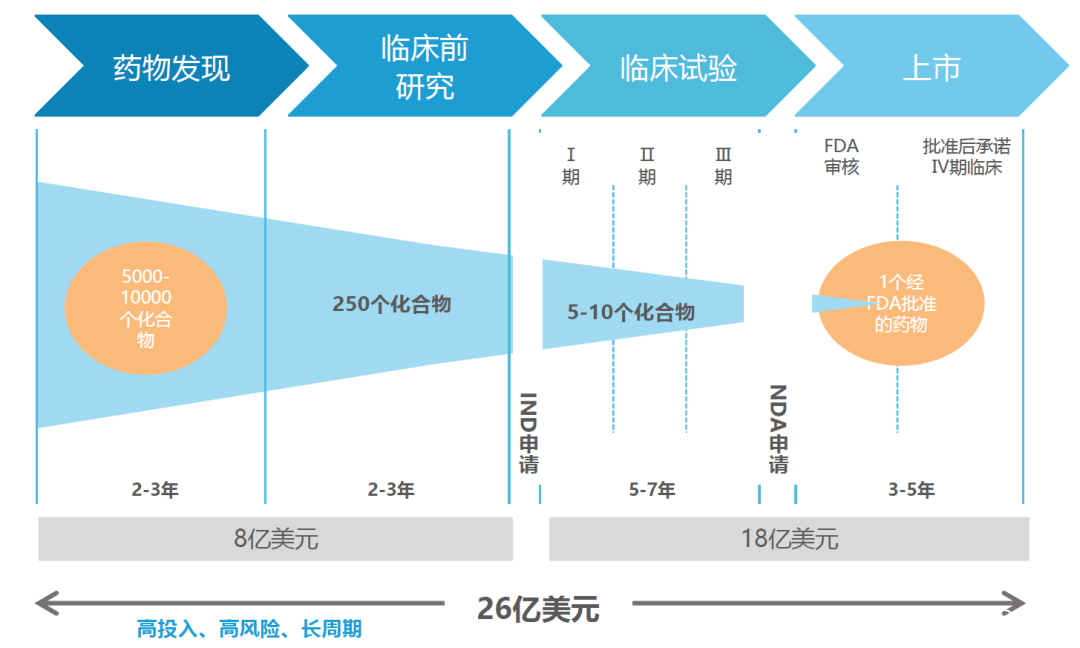
圖:藥物研發流程示意。來源:塔夫茨藥物開發研究中心
這種對人來説的繁瑣工作,恰恰是AI非常典型的應用場景。
今天所説的AI製藥就是利用AI的歸納推理能力,分析實驗數據優化藥物研發環節;利用AI算力優勢,物理層面演繹分子結構從而加速篩選優化先導物。換句話説,AI製藥把創新藥行業的規則扭轉到了比特幣“挖礦”的邏輯。誰的算力大,誰的模型做的好,誰就能率先進入臨牀試驗。
AI製藥可以跳過原來漫長的臨牀前的研發時間,降低前期研究所耗費巨大的人力和材料成本,直接推選出最符合要求的候選藥物。而這恰恰是創新藥前期研發的全部流程。誰能率先發現新的靶點,誰就能擺脱其他的同類追隨者。

以治療腫瘤的PD-1為例,這個靶點上密密麻麻趴滿了等待套利的偽創新藥企業,同業競爭壓力巨大。跟這些追隨者競爭,就算成功跑了出來,在中國也要面臨醫保費用有限購買力的“大剪刀”,讓這些fast in follow、me too、me better企業蹦躂不了太高。
AI製藥的大面積應用這將允許藥企能夠擺脱經費不充足的壓力,可以不再追熱度、抄作業,向着Best in Class(同類最優)甚至First in Class(同類第一)進軍。更好地吃到獨家特效藥所帶來的收益,為社會和股東創造價值。
在算力取得長足進步的今天,AI製藥在硬件上具備了施展的可行性。AI製藥的實力如何,還得看賽道上的玩家做得怎麼樣。
02
賽道上都有誰?
目前,AI藥物研發市場有三大類公司,IT巨頭、AI藥物研發初創企業和大型藥企。三類企業依託各自在平台、算法和數據的優勢切入行業。

大型藥企這邊,近年來世界頭部藥企如輝瑞、諾華、強生、阿斯利康、默沙東等都有積極佈局AI藥物研發領域;國內醫藥行業的龍頭,如中國生物醫藥、藥明康德等也抓住機遇紛紛佈局此賽道,開展與AI藥物研發初創公司的合作。
佈局方式上,國外醫藥公司多與初創型AI藥物研發公司合作,共同開發新藥模式為主,也會以投資的方式合作。國內醫藥企業在AI藥物研發的佈局雖然相較海外略晚,但也是合作與投資兼有。其中藥明康德前後已參與了4家AI藥物研發初創公司的投資。

圖:國內公司與AI公司合作情況 來源:健康界研究院
IT公司這邊,從2018年開始,阿里、騰訊等巨頭都開始相繼佈局此賽道。主要發力方向是利用公司算力和AI模型的優勢,介入到AI製藥的環節中。
例如百圖生科推出的“免疫圖譜卓越計劃”,實質上是結合百度自有的算力和AI經驗,結合10億元資金補貼吸引生態聯盟合作伙伴共同運作的生物運算引擎平台。不過,目前這些科技公司搭建的平台都是以搭載數據庫訓練模型為主,並未產生太多實際應用。

圖:國內IT巨頭佈局AI製藥數據平台 來源:億歐智庫
初創企業是AI製藥的主力軍,是AI製藥的主要推動者和實踐者。2021年,全球融資總額約為266億元(超42億美元)。其中,中國在該領域的融資金額超過90億元。
2022年一季度,AI製藥領域發起40多起融資,總金額金額累計超24億美元。投融資活動仍主要發生在中美兩國,佔總融資事件的80%。其中,國外的Schrodinger、Exscientia、Abcellera和國內的英矽智能、晶泰等公司較為優秀。

圖:截止至2022年初,全球AI製藥融資情況 來源:BiopharmaTrend
Exscientia(納斯達克上市,市值14億美元)
從2012年成立到現在,exsientia成功讓兩個AI研發的藥物走上臨牀試驗階段。分別是治療強迫症的化合物DSP-1181和免疫腫瘤藥物EXS21546。這兩款藥的前期研發週期均不超過一年。
Exscientia的核心能力源自於紮實的數據庫(ChEMBL)和主動學習的AI。ChEMBL是一個包含了大量臨牀實驗藥物和批准藥物的治療靶標和適應症的平台,是成為AI製藥公司們訓練並生成藥物分子最重要的數據源之一。公司的主動學習AI,可以在數據很少打標籤,或者不打標籤的情況下,通過讓模型更多關注或者學習。做到能在較少的訓練樣本下獲得較好的模型。
Schrodinger(納斯達克上市,市值19億美元)
Schrodinger的核心能力是業界絕對領先的分子計算模型和大量已經成熟的藥物開發模組。
Schrodinger成立於1990年,經過多年的發展,他們發現了一個精度非常高的用於描繪分子動態變化的模型。在化學分子計算中,你所能模擬的分子越精確就相應的能獲得更好的預期編輯效果。因此,隨着現在發現新藥的難度越來越高,越來越多的製藥企業尋求通過計算來探索新的藥物發現之路。
這家公司能一直維持收入超過30%的增速。目前,Schrodinger的軟件已經在全球有了1600個客户,自己也有25個管線。
除此之外Schrodinger還提供了一整套分子模擬的解決方案,也就是CADD中常説的薛定諤軟件。其中包含太多業內文明的模塊,比如:Glide(分子對接)、FEP+(自由能微擾)、Desmond(分子動力學模擬)、PyMol(蛋白可視化工具)等。這些套件在業內的藥物開發環節中,不可或缺。
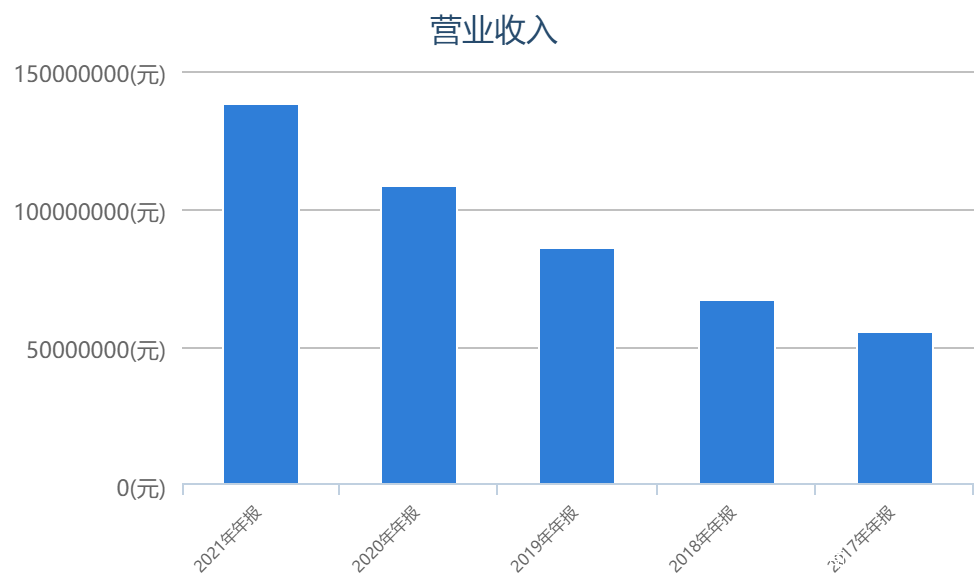
圖:Schrodinger營收增長 來源:Chioce
Abcellera(納斯達克上市,市值22億美元)
Abcellera的核心能力在擁有紮實的數據基礎之上,將AI、工程學、數學、化學、生物學等學科領域綜合起來的能力。
2月12日,美國EUA了一個針對Omicron有效的中和抗體Bebtelovimab,這也是Omicron出現以後,第一個針對Omicron設計的中和抗體。該項目研發時間被壓縮到了90天,震驚世界。
Abcellera是怎麼做的呢?首先,Abcellera擁有他和美國眾多醫院合作收集的資料。接下來Abcellera從幾百萬個細胞中篩選出幾百個用於實驗。為了達到如此效率,他們使用一次性能夠過篩25600個細胞,卡片大小的篩選器來進行操作。
這些細胞在測出氨基酸序列後,他們採用NLP(自然語言處理)來處理數據。然後在利用AI的歸納能力對幾百個特徵進行整理。為了保證結果準確性,他們接着把來自同一個捐獻者的所有抗體重新測序,以獲得單個細胞與所有免疫細胞之間的角色關係。
最後Abcellera再通過高通量的實驗和前面產生的各種排列組合再對抗體進行優化,從而推出少數幾個抗體。
如此技術只能説令人瞠目結舌。得益於高強的技術,目前Abcellera已與全世界眾多藥企展開合作,研發實力毋庸置疑。

圖:Abcellera的合作機構 來源:公司官網
晶泰科技(國內,未上市)
晶泰科技成立於2014年,是中國最早一批AI製藥初創公司之一,目前共獲得6輪融資,總融資金額高達7.85億美元。
該公司的主要專攻方向是AI晶型預測。這個流程能夠預測化合物的不同結晶狀態,並指出不同狀態下的用藥效果。從而提高藥效和縮短研發週期,使藥企能夠通過註冊晶型專利的方式延長專利週期。
晶泰科技的技術平台不僅能準確預測晶體結構,並大幅縮短時間,同時還可以幫助優化分子結構。
2016年,晶泰科技獲得了輝瑞晶型預測的盲測機會。隨後晶泰科技正式成為輝瑞藥物晶型預測等服務的供應商,並不斷擴展了兩家公司之間的合作,包括基於晶泰科技的AI技術,為輝瑞定製化開發人工智能藥物模擬平台,用於新藥發現。
目前晶泰科技已和多家藥企達成合作,包括與世界排名前十藥企中的7家達成正式付費合作,其主導的藥物發現項目有幾十個,絕大多數都是first in class(業界首創)。
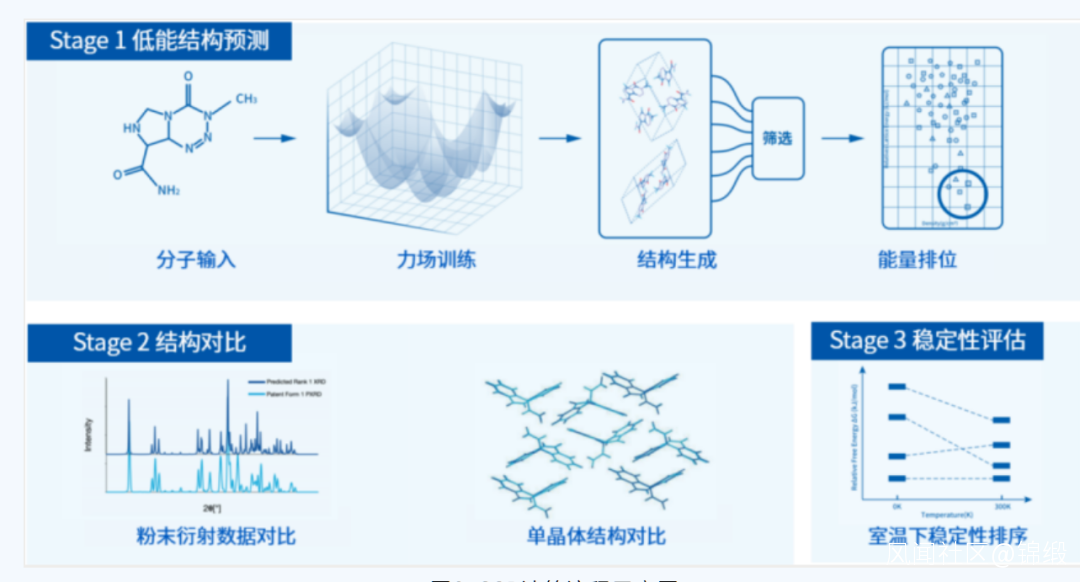
圖:晶泰科技晶型預測流程 來源:公司官網
英矽智能(中國香港,未上市)
2018年6月,英矽智能獲得了由藥明康德領投的一筆戰略融資,成為藥明康德投資的第三家AI藥物研發公司。2019年4月,英矽智能總部由美國轉移落户香港。2021年的英矽智能,全球首次利用AI發現了一種全新機制的用於治療特發性肺纖維化(IPF)的臨牀前候選化合物,整個研發過程只花了不到18個月的時間和大約200萬美元,刷新了新藥研發的速度和最低成本紀錄。
今年1月12日,英矽智能拿到了來自復星醫藥的1300萬美元的首付款和未來的里程碑式付款,這是國內AI製藥公司迄今最大的一筆訂單。
英矽智能的主要優勢在於其提供的AI製藥研發模組可覆蓋大部分藥物開發環節,如靶點發現、化合物合成、臨牀試驗結果預測等藥物開發等。
與其他公司主要採用的機器學習、深度學習、神經網絡再輔以獨家模型的操作模式不同,英矽智能採用的是生成式對抗網絡(GANS)和強化學習(RL)的技術。該技術能夠強調數據之間的內學習,從而發現藥物起效的新機制、新關聯。
英矽智能發現一款靶向主蛋白酶(3CL)的臨牀前候選藥物,用於治療新型冠狀病毒引起的肺炎。該候選藥物的全新分子結構由英矽智能自主研發的AI平台所生成,該化合物是一項全新的分子構造。從原料到製備化合物僅需兩步,合成效率高。
AI製藥在今天的成就從近年的投資熱度也能瞥見,上述這些風格迥異的研發成就給了資本信心。
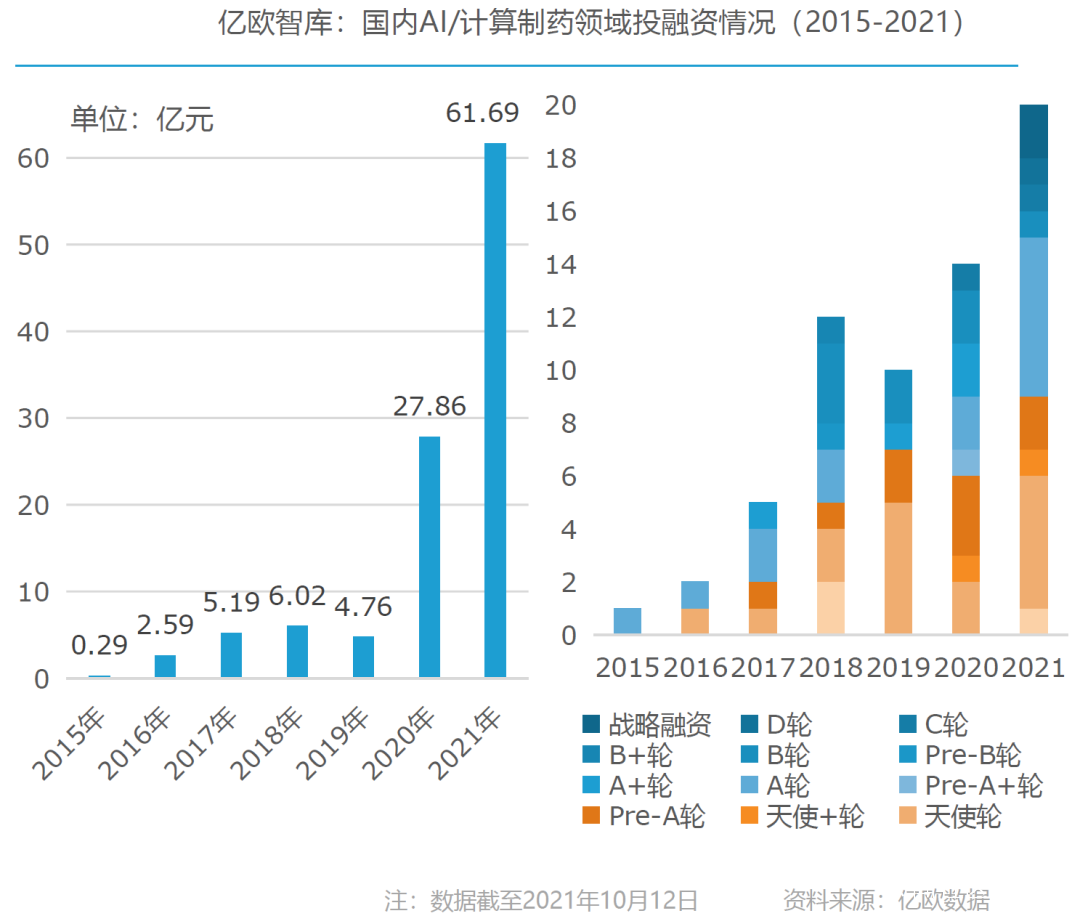
圖:2015-2021國內AI製藥融資情況 來源:億歐智庫
但資本的火熱並不代表AI製藥的成熟。早年彼得·蒂爾(Peter Thiel)一眼相中Abcellera的研發能力,該公司在上市之初市值一路幹到了200多億美元。不過因為AI製藥公司需要長期的研發支出,外加醫藥領域對AI製藥的謹慎態度,使得Abcellera今天的市值縮水到當初的十分之一。
03
AI製藥的挑戰
梳理了眾多的AI製藥公司後可以發現,AI製藥雖然取得了不少成果,但仍算是一個相當早期的階段。從產業研發特性來説,AI製藥是一個高科技、跨學科、高支出、強監管的產業,這些挑戰每一項都稱得上是懸在頭頂的“達摩克里斯之劍”。
首先,AI製藥的跨界人才壁壘極高。AI製藥不同於今天的各類型AI科技公司,AI製藥對人才在AI和生物學、化學、物理學等等學科都要求精通。
對於AI科技公司來説,自動駕駛稱得上是AI難度的巔峯之一了。但自動駕駛的核心難度在於如何將不同類型傳感器的信息進行融合,對這些數據進行綜合彙算,最後再調整汽車不同系統之間的配合,達到自動控制的效果。但成為一名駕駛員只需要考一本駕照。
而AI製藥需要從業者擁有兼具兩者的綜合能力。不精通其他學科,調製的AI輸出結果無效,白白浪費數據和時間。對AI技術不精通,那製作的模型和統計的數據就不能很好地被AI所用。
對於AI製藥來説,這些差距是不能僅通過燒錢、跑測試就能彌補的,Abcellera和Schrodinger能夠獨霸一方,靠的正是多年專業能力的積累和AI技術的獨門秘籍。
其次,AI製藥初創公司難以獲得高質量的數據。
擁有有效且翔實的數據來源是能夠保障AI輸出結果正確度的保障。目前,AI製藥公司的數據源多來自於公開資料,如已發表的醫學文獻,公開的靶點庫,藥企、科研機構或院校的公開數據等。但最主要的高質量數據是來自藥企自身的研發實驗室,這部分數據屬於商業機密,十分寶貴。
目前做的比較好的AI製藥公司基本上要麼是有自建實驗室和研發管線,要麼就是和大型藥企以投資的方式合作(如藥明康德領投Schrodinger的E輪融資)。
同時,缺乏數據也是大型科技企業的AI製藥平台產出成果緩慢的核心原因。
缺乏數據和主動權的AI製藥想要在業內真正擁有話語權,難度很大。不過目前特殊的例子也有,例如Relay Therapeutics(納斯達克上市,市值18億)在分子動力學的計算上見長。當然,這是因為他們真的有一台超算。
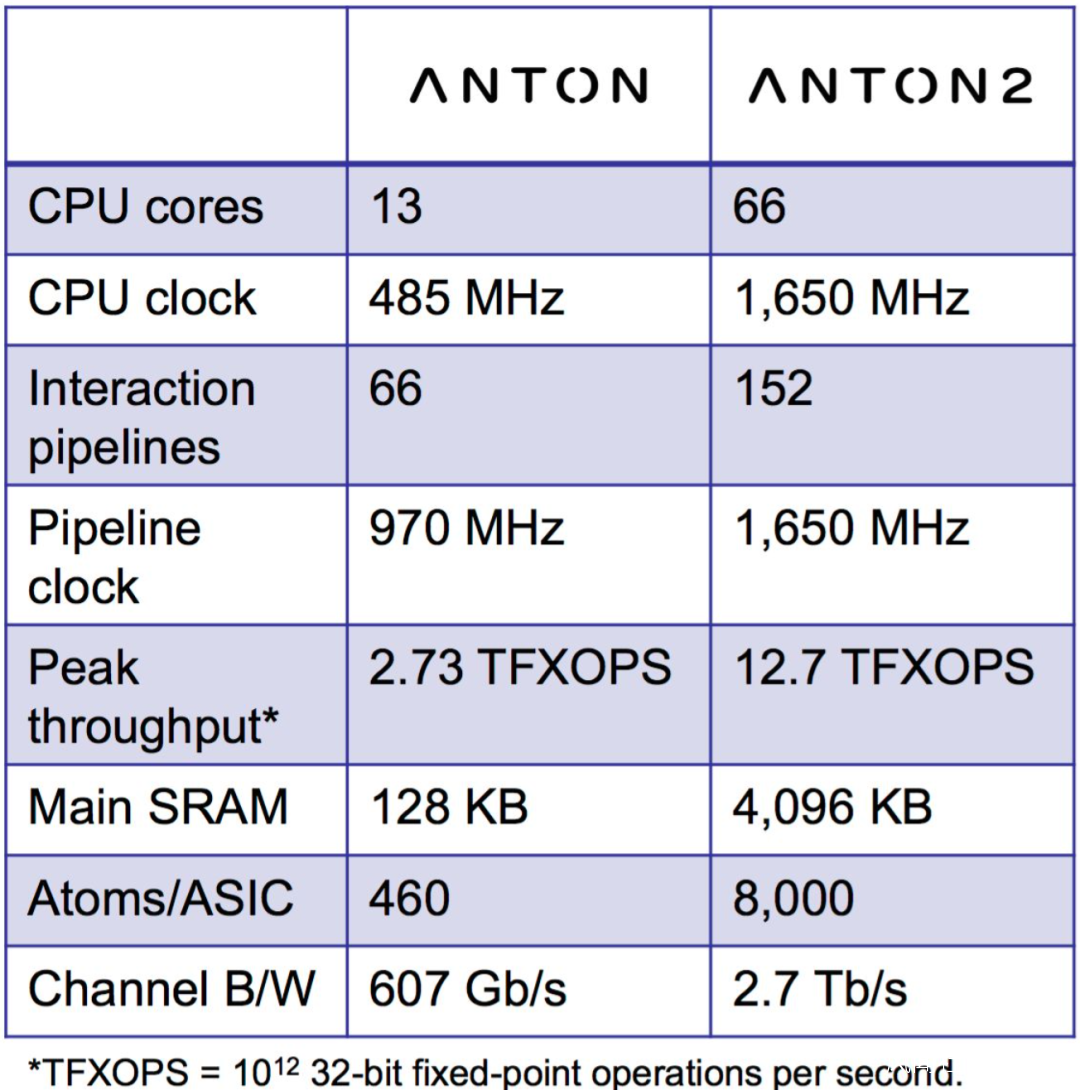
圖:Relay的超算ANTON 來源:網絡
最後,AI製藥仍不可替代真正的實驗,當前也並沒有AI製作的藥物真正上市。
醫藥領域的超強監管使得創新藥的研製一定需要漫長的臨牀實驗週期。目前這些AI藥物還都在慢慢的走臨牀實驗流程。未能上市就不能直接證明藥物價值,進而無法體現公司價值。
而技術上,市面上大部分AI製藥,依然停留在以數據驅動的AI模型輔助藥物分子發現的階段。對於分子的模擬上,即從物理模型驅動的AI模式,最大的挑戰在於計算效率和計算精度無法兼顧。比如傳統的分子動力學模擬在應對複雜的蛋白體系以及蛋白動態構象採樣方面的還是力不從心。這就意味着現階段AI製藥仍受限於技術研發,實驗室的實驗成本不能完全取代。