基石藥業:好故事從肺癌藥“小宇宙”開始_風聞
天府财经网-天府财经官方帐号2022-06-09 07:46
國家藥監局官網顯示,基石藥業潛在同類最優PD-L1抗體藥物擇捷美®(舒格利單抗注射液)拓展適應症在近日獲批,用於在接受鉑類藥物為基礎的同步或序貫放化療後未出現疾病進展的、不可切除、III期非小細胞肺癌患者(NSCLC)的治療,擇捷美®因此成為全球首個獲批用於治療同步或序貫放化療III期非小細胞肺癌患者的PD-(L)1抗體。此次獲批也是基石藥業自2021年以來取得的第八項新藥上市申請的批准。而同樣不久之前,港股基石藥業發佈了2021年報。
我是從21年半年報開始關注這家公司,那時它的兩款小分子精準抗癌藥剛上市。這次年報中披露,全年有四款藥物獲批上市,在這家創新藥企商業化的第一年,獲批藥品數量已經和一些創立時間更早的老牌港股18A持平,以兩款小分子為主的銷售額超過1.6億,此外還獲得了超過八千萬的管線授權費用,整體表現不錯。
提到基石藥業,業內評價是:肺癌藥高手。為何?因其構建了一個聚焦非小細胞肺癌(NSCLC)的創新藥“小宇宙”,核心是全球同類最優PD-(L)1抗體擇捷美®。再加上中國首個RET抑制劑普吉華®和全球同類最優藥物洛拉替尼,三軍共同圍剿中國最大的細分癌種—NSCLC。目前洛拉替尼治療ROS1陽性晚期非小細胞肺癌的關鍵性臨牀試驗在中國展開,普吉華®和擇捷美®都已經獲批,且擇捷美®已經在NSCLC領域獲批了兩個適應症。
肺癌之外,基石藥業早早就開始了管線2.0戰略以發展下一代藥物,包括進度全球前三的靶向ROR1 的抗體偶聯藥物(ADC)CS5001,業界重點關注的三特異性抗體CS2006,公司強大的研發實力得到業界公認。根據年報,基石藥業在21年底現金有16億,也是儲備了足夠的彈藥推進這兩個項目的臨牀進展。
凡是過往,皆為序章。之前,中國創新藥企故事側重於前半部分—研發;如今,投資者開始盯着故事的後半部分,它的評價對象是市場能力,即創新藥企要能賺錢。基石藥業從管線立項起就以商業化潛力為根本,與國內外大型藥企達成多項商業合作,可謂胸有成竹。
1、肺癌藥“小宇宙”核心--同類最優的PD-(L)1
在國內卷生卷死的PD-(L)1市場,截至目前從跨國藥企到本土創制,已上市的品種達到12個,其中三分之二獲批了NSCLC適應症,因為NSCLC市場真的大到不能放棄。2020年中國肺癌新發患者約有82萬人,NSCLC患者佔比約85%,其中七八成處於III期和IV期階段。
這麼多選手同場競技,如何判定誰是同類最優PD-(L)1抗體?我認為必須從三個角度出發:
1)臨牀研究受到業界同仁的認可程度,即研究本身的質量問題,這是藥品評價的起點;
2)臨牀研究療效數據的直觀比較,即同類最優的尺度問題;
3)可獲益患者規模,即市場潛力問題。
這三個問題,擇捷美®給出了很好的答案。
首先,其臨牀研究質量在業內受到同仁高度認可——1月15日,全球臨牀研究期刊“頂流”--The Lancet Oncology(《柳葉刀-腫瘤學》)以雙響炮的形式,重磅發表了基石藥業擇捷美®的用於NSCLC領域的兩項研究結果,分別來自於名為GEMSTONE-301和GEMSTONE-302的臨牀試驗。須知,在柳葉刀雜誌上發表的研究,質量得是全球同行公認的。
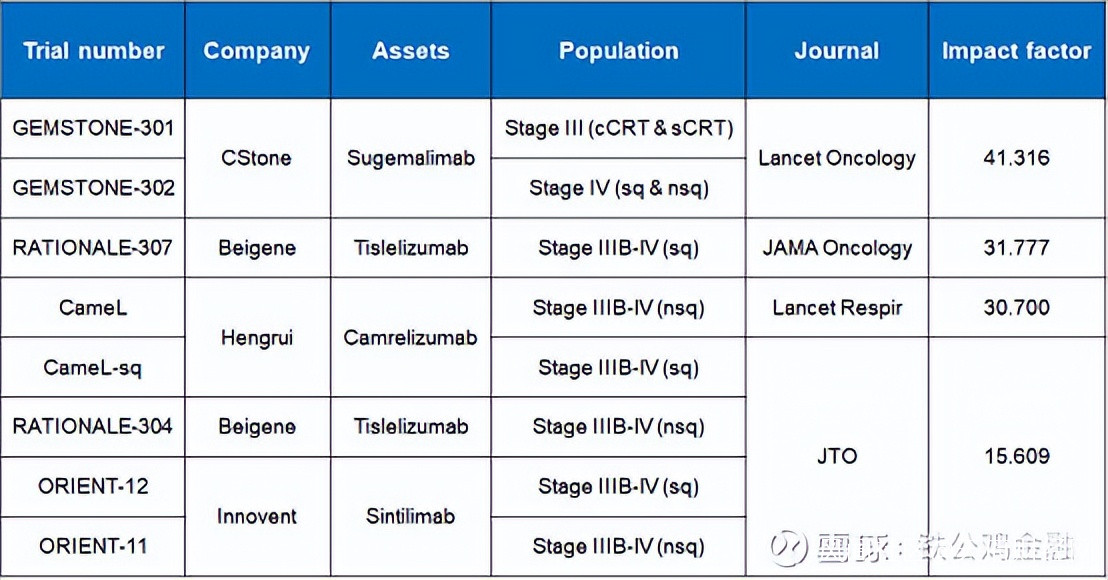 (本土創制的幾款PD-(L)1抗體用於NSCLC的註冊性臨牀研究所發表文獻的影響因子對比)
(本土創制的幾款PD-(L)1抗體用於NSCLC的註冊性臨牀研究所發表文獻的影響因子對比)
實際上,早在2021年9月舉辦的兩場腫瘤研究者全球峯會--世界肺癌大會年會和歐洲腫瘤內科學會年會上,GEMSTONE-302和GEMSTONE-301研究就分別入選大會口頭報告並向全球公佈。
在強者如雲的臨牀研究界,擇捷美®臨牀研究的質量得到了同行研究者的交口稱讚,“大家都説好才是真的好”,世紀初家喻户曉的廣告語在此分外貼切。
第二,擇捷美®在療效數據比較中再勝一籌。要證明療效好,擇捷美®怎麼能不和K藥(帕博利珠單抗)、O藥(納武單抗)、I藥(度伐利尤單抗)這種霸王龍級別的對手較量一番呢?
先看GEMSTONE-302研究,擇捷美®獲批用於聯合化療一線治療IV期鱗狀和非鱗狀NSCLC患者就是基於這個研究。
下圖比較了包括K藥和O藥在內的多款PD-(L)1抗體用於IV期NSCLC患者時,降低疾病進展或死亡風險的比例,以及中位PFS延長時間。擇捷美®在非鱗癌中的表現與K藥相當,在鱗癌中的表現勝過K藥,整體表現更是勝過K藥、O藥在內的所有對手。
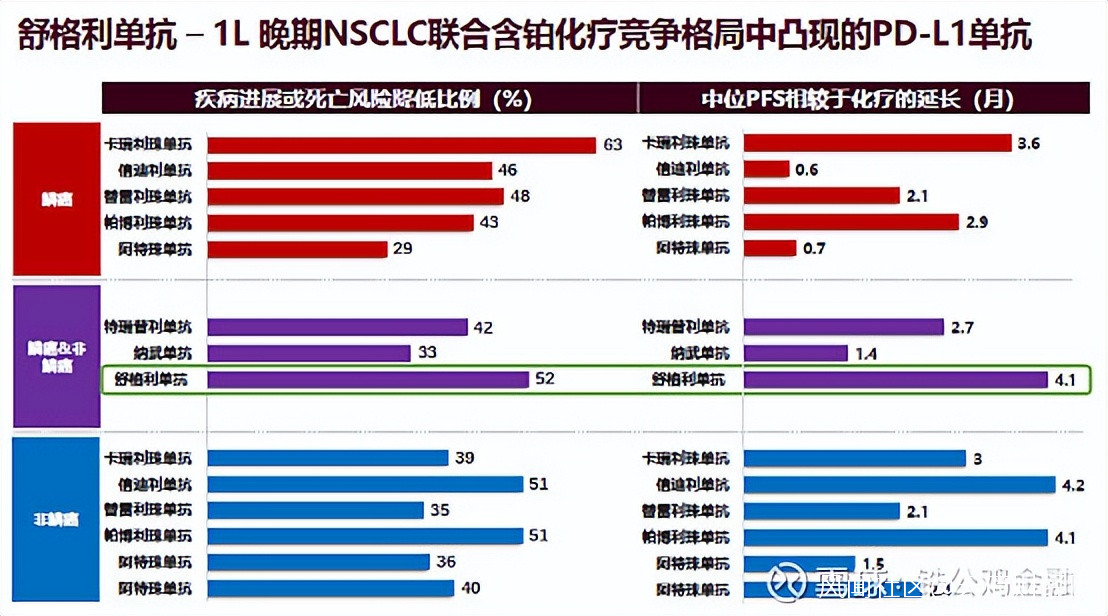 就在今年1月,GEMSTONE-302研究又公佈了更新數據,它達到總生存期(OS)的研究終點,成為全球首個聯合化療顯著改善鱗狀和非鱗狀IV期初治NSCLC患者OS的PD-L1單抗。眾所周知,OS是評價腫瘤藥物療效的金標準。主要研究者周彩存教授表示,OS數據證明擇捷美®有望改變晚期NSCLC一線治療格局,成為晚期NSCLC的首選腫瘤免疫治療藥物。
就在今年1月,GEMSTONE-302研究又公佈了更新數據,它達到總生存期(OS)的研究終點,成為全球首個聯合化療顯著改善鱗狀和非鱗狀IV期初治NSCLC患者OS的PD-L1單抗。眾所周知,OS是評價腫瘤藥物療效的金標準。主要研究者周彩存教授表示,OS數據證明擇捷美®有望改變晚期NSCLC一線治療格局,成為晚期NSCLC的首選腫瘤免疫治療藥物。
再看GEMSTONE-301研究,擇捷美®剛剛獲批用於在同步或序貫放化療後未發生疾病進展的、不可切除的III期NSCLC患者的鞏固治療就是基於這個研究。
與預期相同,擇捷美®獲得了同步或序貫放化療的兩種患者PFS均獲益的數據,而且OS獲益趨勢非常明顯。而所有其他的PD-(L)1中,僅有I藥獲得了同步放療患者獲益的數據,並沒有獲得序貫放化療患者獲益數據。
進一步,I藥的註冊性臨牀試驗PACFIC中53%的入組患者是IIIA期,而GEMSTONE-301研究中只有29%是IIIA期,其他都是更晚期的IIIB和IIIC期。在入組病人晚期比例更高的情況下,擇捷美®和I藥仍然可以比肩論道,甩下其他所有競爭者。
綜合兩個註冊性臨牀數據,擇捷美®治療III期和IV期NSCLC的綜合實力,獨佔鰲頭。
第三,擇捷美®可獲益患者規模遠超競品。所覆蓋的III期和IV期NSCLC患者全人羣大約年增50萬人,按目前5萬一年藥費測算,潛在市場規模250億元。而且,擇捷美®是獲批針對序貫放化療後未發生疾病進展的III期NSCLC患者的唯一PD-(L)1抗體。國內此類患者中70%是序貫放化療,每年大概新增15-20萬例,僅這一市場規模就能達到80億元。
在如今瞬息萬變的市場上,成為同類最優產品的商業意義自不必多論,但基石藥業擇捷美®的潛力不止於此。它在擴展肺癌領域以外適應症的道路上亦是健步如飛。
今年1月,擇捷美®治療復發或難治性結外自然殺傷細胞/T細胞淋巴瘤(R/R ENKTL)的註冊性臨牀研究(GEMSTONE-201)達到主要研究終點,擬遞交新適應症上市申請。目前尚無PD-1或PD-L1抗體被批准用於治療R/R ENKTL,擇捷美®有望成為同類首創。由於該項研究成果具有高度價值,美國FDA和中國CDE全都授予了突破性療法評定。
並且,擇捷美®在針對食管鱗癌和胃癌適應症方面的研發也非常順利,同在1月完成兩項重磅三期註冊性臨牀試驗的受試者入組。
綜合上述適應症的開發進展,擇捷美®已是中國適用人羣最廣泛的PD-L1抗體。
儘管優點多多,要把擇捷美®賣好,仍然是要鋪大量銷售人員到具體醫院的。以基石藥業目前的體量無法支撐上千人腫瘤銷售團隊,於是有了基石與輝瑞雙向選擇的故事,在本文的第三部分再細説。
2、從肺癌鐵三角,到攬入ADC黃金靶點ROR1的管線2.0
任何個體現象的出現,背後一定有嚴絲合縫的體系。基石藥業在選擇臨牀的靶點和適應症時,早已設計好了未來管線構架的互補和差異化。基石藥業目前有15個管線,自然是針對不同的靶點和適應症,不過目前上市/快上市的新藥中成合圍之勢的,是在肺癌治療領域。如果説擇捷美®是肺癌領域的突圍猛將,那其身側也不乏精準強兵。
2021年,除了免疫藥物擇捷美®外,基石藥業還有兩個靶向藥獲批上市,普吉華®(普拉替尼)和泰吉華®(阿伐替尼)。普吉華®是國內首個獲批上市的RET抑制劑,目前上市適應症是RET融合陽性NSCLC患者的II線治療,今年很可能會提交此類患者的一線治療的補充上市申請。泰吉華®是全球首款用於治療攜帶PDGFRA外顯子18突變的胃腸道間質瘤(GIST)成人患者的藥物。
2021年6月,基石藥業與輝瑞宣佈合作開發洛拉替尼,12月獲批在中國開展用於ROS1陽性NSCLC患者的關鍵性臨牀研究,2022年5月實現首例患者入組。中國NSCLC每年確診病例中2-3%為ROS1陽性,當前缺乏靶向治療藥物。而洛拉替尼在之前的研究中表現出對ROS1陽性晚期NSCLC患者顯示出強效、選擇性的抑制活性。
擇捷美®,普吉華®和洛拉替尼形成的鐵三角意味着,基石藥業現有NSCLC管線版圖囊括了免疫治療方式的主流PD-(L)1市場,以及靶向治療方式中有潛力且競爭者相對較少的針對RET和ROS1靶點的細分市場。
這大概是基石藥業被稱為肺癌藥高手的由來,對肺癌市場的充分理解,豐富的肺癌臨牀經驗,以及滿足關鍵臨牀需求的管線佈局。不過,基石藥業並不是一家只針對肺癌的創新藥企,它的強項還有很多,比如用於胃腸道間質瘤的泰吉華®,用於血液瘤的拓舒沃®,用於肝細胞癌的CS1003,特別是在這兩年業界最火的創新藥類別--抗體偶聯藥物(ADC)方面,它也有品種全球領先。
今年1月,基石藥業宣佈靶向受體酪氨酸激酶樣孤兒受體1(ROR1)的ADC--CS5001獲得FDA批准開展臨牀研究。
儘管國內ADC只上市了4個,其中3個進口,但在研品種已經很多。基石藥業選擇了打差異化策略,放棄那些已經有扎堆趨勢的ADC靶點,而是針對初步展示出治療潛力的黃金靶點ROR1進行開發。
由於起步早,進展快,數據好,基石藥業已然與兩家一線跨國藥企並列在該領域全球第一梯隊,而另外兩家ROR1 ADC的交易價格都已超過10億美元。不得不讚嘆基石藥業的眼光精準。
此外,去年9月,基石藥業還有一款藥CS2006在國內獲批新藥臨牀試驗,這也是一款潛在同類首創/最優腫瘤藥,是靶向PD-L1/4-1BB/HAS的三特異性抗體,極有可能成為下一代腫瘤免疫治療的領先藥物和腫瘤聯合治療的新骨架分子。
整體上,從基石藥業2.0階段的管線來看,基石藥業明顯是分析市場現狀後知己知彼的佈局——更加強調商業化。目前基石藥業已建立了15種腫瘤候選藥物組成的豐富產品管線,管線就是藥企的生命線,看管線就能看到未來。
3、商業化前景:廣闊天地大有作為
內卷時代,一家創新藥企能不能活下去,除了看研發成果,還要看商業化能力。而商業化能力首要考驗的就是臨牀進度夠不夠快,畢竟天下功夫唯快不破。可以説,盯不盯得準管線,看的是眼光。拿不拿得下臨牀,看的是本事。
從基石藥業的表現來看,不僅拿下了臨牀,而且推進得又好又快。基石藥業加速擇捷美®的臨牀開發從國內第12位進入臨牀,上升至全球NSCLC第一梯隊,僅僅用了四年左右時間。與其他本土生物製藥企業相比,基石藥業擇捷美®IV期NSCLC臨牀試驗時間縮短了1/2;而III期NSCLC臨牀試驗時間,與大型跨國製藥企業相比,更是縮短了約2/3。
正因為基石藥業管線佈局兼顧技術成熟性與市場潛力,且能夠以極高效率推動臨牀進展,業界翹楚們才競相與其合作。
2021年11月22日,恆瑞醫藥將花費最高約13億元引進基石藥業的CS1002在大中華區的研發、註冊、生產和商業化的獨佔權利。恆瑞醫藥將向基石藥業支付包括5200萬元的首付款、2500萬元的研發里程碑付款,以及11.85億元的商業化里程碑款。除此之外,恆瑞醫藥還將向基石藥業支付10%至16%的銷售提成。消息一出,舉座皆驚。
CS1002是基石藥業研發具有同類最優潛力和差異化給藥方式的全人源抗CTLA-4單克隆抗體,目前處於臨牀開發階段。CTLA-4是為數不多的經過臨牀驗證的腫瘤免疫聯合療法的靶點,與PD-1聯合的雙免疫檢查點療法具有顯著優勢。CS1002在早期臨牀開發中取得了巨大的成果,包括髮現了不同的給藥方案,在多種適應症中顯示出有效性和優越的安全性。
眾所周知,恆瑞是國內最大最強的傳統藥企之一,擁有頂級的流通和商業化能力,但去年日子不算順遂,在這種時刻選擇基石藥業的CS1002,只能説明恆瑞對這款藥非常看好。對基石來説,獨立開發CS1002的投入巨大,而與恆瑞的聯姻如虎添翼,CS1002與恆瑞已有PD-1等腫瘤管線聯合,將最大程度釋放商業化潛力。
這不是基石藥業第一次因鉅額授權而藝驚全場。2020年,基石藥業將擇捷美®的開發與商業化先後授權出去,在中國大陸地區的授權給了輝瑞,在海外的授權給了EQRx公司。這兩項授權給基石藥業帶來豐厚回報,與輝瑞的合作最高達到2.8億美元的里程碑付款,中至高十位數比例的分級特許權使用費,與EQRx公司的合作帶來1.5億美元的預付款、最高達11.5億美元的里程碑付款以及淨銷售額的兩位數比例的分級特許權使用費。
擇捷美®國內市場的重點在公立醫院。輝瑞深耕中國多年,廣泛覆蓋超過4600家醫院,約佔市場的90%,商業化能力驚人,但當前自身在華沒有獲批的PD-(L)1抗體,故而主推臨牀優勢明顯的擇捷美®。海外市場上,由於美國政界已出現針對中國藥企臨牀研究的苗頭,EQRx目前在廣泛推進英國、中東、土耳其和非洲的申報註冊工作。
基石藥業自身的市場能力當下聚焦在普吉華®、泰吉華®和拓舒沃®這三款靶向藥物上,大約300人的團隊鋪到了核心地區的600家醫院,商業保險合作計劃達到了60餘家,今年醫院和商保計劃數還將增加。
普吉華®、泰吉華®、拓舒沃®作為精準治療藥物,患者只要有相關基因突變就可以用藥取得較好療效。要解決的問題就是患者必須知道自己有這個突變。通過參與臨牀指南編寫,藥企宣傳教育,優化第三方實驗室合作伙伴的檢測流程,最重要地,參與“大愛無罕”公益項目免費為患者檢測,基石藥業已將RET+(普吉華®靶點)/PDGFRA外顯子18(泰吉華®靶點)檢測率從藥品上市前40%提高到60%,IDH1檢測率(拓舒沃®)提升到目前的70%,且2022年還將努力持續提升患者基因檢測率。基石藥業還建立了“生命基石”項目,包含大量患者教育課程,通過“生命守望”平台便於患者隨訪和保留,目標是將70%的患者納入到患者管理計劃。
基石藥業各款藥物已列入CSCO NSCLC/GIST診療指南、中華醫學會指南及非小細胞肺癌分子病理檢測臨牀實踐指南等10多項中國國家指南,通過在精準治療論壇、專病研討會、藥品上市會、罕見病大會廣泛發聲,以及多個患者使用案例的互聯網分享,醫生認知程度不斷提升。2021年,基石藥業參與1,500多項活動,觸達超過10,000名全國重要的KOL和醫療專業人士。今年7月將舉辦拓舒沃®上市會,預期包括國家血液系統疾病臨牀醫學研究中心主任王健祥在內150個血液病專家會參與。2022年,基石藥業精準治療藥物的推廣目標之一是要爭取所覆蓋醫院的90%開具出處方,80-90%的醫療專業人士主動推薦。
上面這些市場投入都是不低的,但長期將帶來巨大回報。隨着NDA數量進一步增加,銷售額的快速提升,相信基石藥業市場團隊的規模也會做相應的擴大,千人團隊並不遙遠。
一個藥企的未來,不僅看研發能力,還要看商業化進程。廣闊天地大有作為,從肺癌藥“小宇宙”的研發到商業化,基石藥業的好故事剛開始。