Cell發佈首份遺傳學核心關係圖譜:將人類基因與其在細胞中的作用一一聯繫了起來_風聞
中国生物技术网-中国生物技术网官方账号-2022-06-15 11:23
繪製遺傳變化與其基因型與表型之間之間的關係對於理解基因和細胞功能至關重要,這也是遺傳學的核心。單細胞CRISPR篩選是一種新興的工具,可以用來探索哺乳動物基因功能和基因調控網絡,以產生豐富的基因型-表型圖譜。然而,到目前為止,它們的使用還僅限於研究預先選擇的基因和預先定義的生物學問題。
2022年6月9日,發表在**《Cell》上的一項新研究中,來自麻省理工學院**(MIT)領導的研究團隊報告了第一個在超過250萬個人類細胞中執行基因組規模的單細胞CRISPR篩選結果,這些數據將人類基因與其在細胞中的作用一一聯繫了起來,揭示出基因與細胞功能的多維景觀,從而提供了更為全面的基因型-表型關係圖譜。


**該圖譜使科學家們可以深入研究各種生物學問題,包括用它來探索具有未知功能的基因對細胞的影響、研究線粒體對應激的反應,並篩選出導致染色體丟失或獲得的基因。**這在過去是不可能完成的任務。
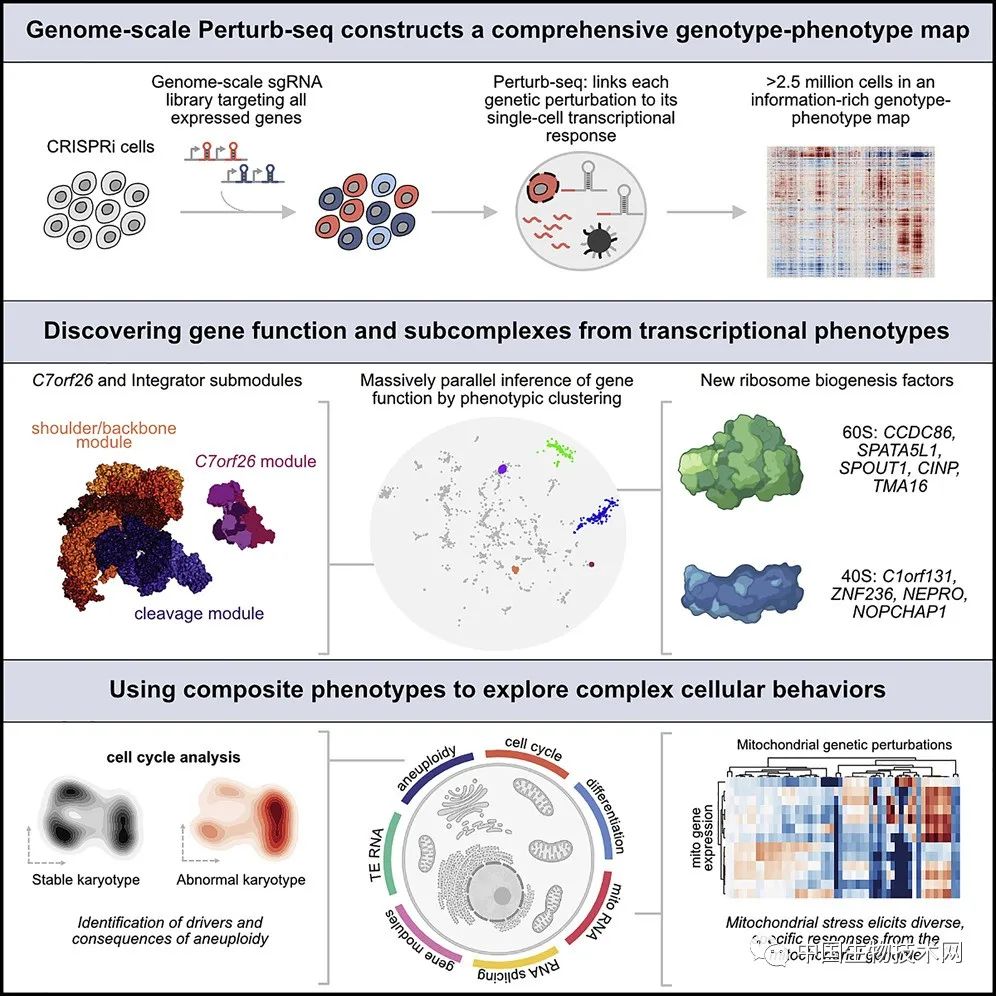
20多年前,曾參與人類基因組計劃的MIT生物學教授Jonathan Weissman是這項新研究的負責人。他説:“這是一個極為豐富的資源,就像人類基因組那樣,所有科學家都可以使用。你可以利用它進行基於發現的研究。有了這個基因型-表型關係圖譜,你不需要預先定義你要研究的生物學問題,就可以直接進入並篩選數據庫,而且,你也不需要做任何實驗。”
該研究共同通訊作者、Weissman實驗室的前博士後研究員Tom Norman説:“我認為這個數據集將使來自生物學其他領域的學者進行我們從未想到過的分析。”
這項研究使用了Perturb-seq方法能夠**以前所未有的深度跟蹤基因開啓或關閉的影響。**該方法於2016年首次由Weissman等人首次提出,但當時只能用於小規模的基因,且成本高昂。
2020年3月,發表在**《Nature Biotechnology》**上的一項概念研究中,該團隊與合作者共同創建了可以擴大規模的新版本Perturb-seq,擴展了科學家們研究複雜細胞過程的遺傳控制能力。

Perturb-seq方法使用CRISPR-Cas9基因組編輯技術將遺傳變化引入細胞,然後使用單細胞RNA測序來捕獲有關因特定遺傳變化而表達的RNA信息。由於RNA控制着細胞行為的方方面面,因此,這種方法有助於解碼遺傳變化對細胞的諸多影響。
自從發表了首個概念驗證研究以來,Weissman等人已經在較小規模研究中使用了這種篩選方法。例如,他們在2021年使用Perfert-seq探索了人類和病毒基因在感染常見皰疹病毒HCMV的過程中是如何相互作用的。
在這項新研究中,Weissman團隊將該方法擴展到了整個基因組。他們利用人類血癌細胞系和來自視網膜的非癌細胞,對超過250萬個細胞進行了Perturb-seq測序,並利用這些數據構建了一個將基因型與表型聯繫起來的全面圖譜。
在完成篩選後,研究人員使用新數據集研究一些生物學問題。
Norman説:“Perfert-seq的優點是,它可以讓你以一種無偏差的方式獲得一個大數據集。沒有人會知道你在使用這種數據集時會遇到什麼限制。現在你更應該關注的是,到底用它來做什麼?”
第一個最明顯的應用是研究具有未知功能的基因。由於新篩選讀出了許多已知基因的表型,研究人員可以使用這些數據將未知基因與已知基因進行比較,並尋找相似的轉錄結果,這可能表明基因產物會作為更大複合物的一部分協同工作。
其中一種名為C7orf26的基因突變尤為突出。研究人員注意到,將其刪除後導致相似表型的基因是稱為整合子的蛋白質複合物的一部分,該複合物在產生核RNA中發揮作用。整合子複合物由許多較小的亞基組成,之前的研究表明其包含14種單獨的蛋白質。現在,研究人員證實,C7orf26是構成這種複合體的第15個組成部分。
他們還發現,15個亞基在較小的模塊中協同工作,執行整合子複合物中的特定功能。研究人員表示,如果沒有這些重要的見解,就無法弄清楚不同的模塊在功能上是否存在差異。
Perfert-seq的另一個優點是,由於分析側重於單個細胞,研究人員可以使用這些數據來觀察更復雜的表型。通常,這些表型與來自其他細胞的數據一起研究時會變得混亂。
Weissman説:“我們經常把‘基因X’被敲除的所有細胞當作整體來觀察它們是如何變化的。但有時,當你敲除一個基因時,缺少同一個基因的不同細胞會表現出不同的行為,而這種行為可能會被忽略。”
研究人員發現,刪除一個基因子集會導致不同細胞產生不同的結果,這與染色體分離有關。它們的移除會導致細胞失去一條染色體或增加一條額外的染色體,這種情況被稱為非整倍體。
Weissman説:“你無法預測丟失這個基因的轉錄反應是什麼,因為它取決於你獲得或丟失的染色體的次級效應。我們意識到,這個局面其實是可以扭轉的,創建這種複合表型,尋找獲得和丟失染色體的特徵。通過這種方式,我們首次在全基因組範圍內篩選出正確分離DNA所需的因子。”
Norman説:“我認為非整倍體研究是迄今為止這一數據最有趣的應用。它捕獲到到一種只能通過單細胞讀數獲得的表型。你無法以任何其他方式去追蹤它。”
研究人員還利用他們的數據集研究了線粒體如何應對壓力。線粒體是由自由生活的細菌進化而來,其基因組攜帶13個基因。在核DNA中,大約1000個基因與線粒體功能有關。
長期以來,人們一直對核DNA和線粒體DNA在不同細胞條件下如何協調感興趣,尤其是當細胞受到壓力時。
研究人員發現,當他們擾亂不同的線粒體相關基因時,核基因組對許多不同基因變化的反應是相似的。然而,線粒體基因組的反應要多得多。
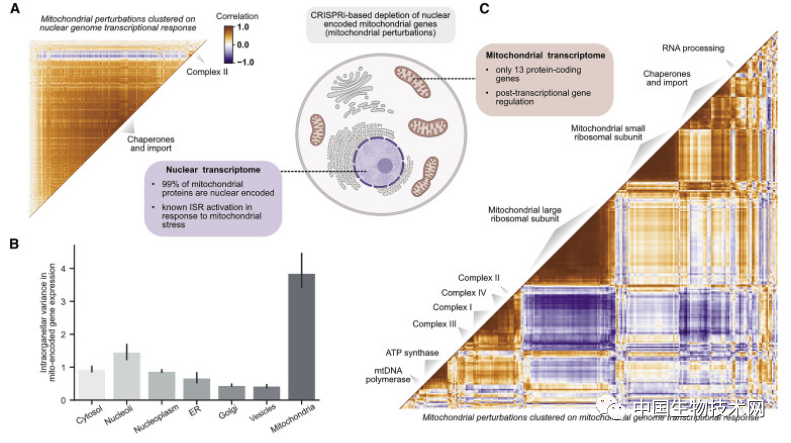
研究人員表示,為什麼線粒體會有自己的DNA,這仍然是一個懸而未決的問題。從他們的研究中可以看出,擁有單獨線粒體基因組的一個好處可能是對不同的應激源進行局部或特異性的基因調節。
Weissman説:“如果一個線粒體損壞,而另一個線粒體是以不同的方式損壞,那麼它們可能會做出不同的反應。”。
在未來,該團隊還將繼續探索基因功能圖譜,並希望在癌細胞系之外的不同類型細胞上使用Perturb-seq。
Norman説:“這真的是大家多年共同合作的成果,我很高興看到它再次成功並得到擴展。”
論文鏈接:
https://doi.org/10.1016/j.cell.2022.05.013
https://www.nature.com/articles/s41587-020-0470-y