二次感染防不勝防?謝曉亮團隊證實奧密克戎並非“天然疫苗”_風聞
心之龙城飞将-2022-06-20 22:28
知識分子公眾號2022年06月20日 14:50:54194人蔘與22評論
通過普遍感染奧密克戎來實現羣體免疫難以實現 | 圖源:istockphoto,wildpixel
導 讀
根據6月17日中國研究團隊發表在《自然》雜誌上的一篇論文,目前針對奧密克戎早期變異株研發的疫苗,已被新出現的亞型逃逸,因此或許無法對後續新的奧密克戎變異株產生免疫保護。**這意味着通過普遍感染奧密克戎來獲得羣體免疫難以實現。**該項研究也提示研究人員需要尋找到更為廣譜的疫苗與抗體藥物。
訪談、撰文|既來知 錢煒
● ● ●
新型冠狀病毒通過突變先後衍生出阿爾法 (Alpha) 、貝塔 (Beta) 、伽馬 (Gamma) 、德爾塔 (Delta) 等變異株。曾有人 “擔心” 這樣突變下去,希臘字母會不夠用了。
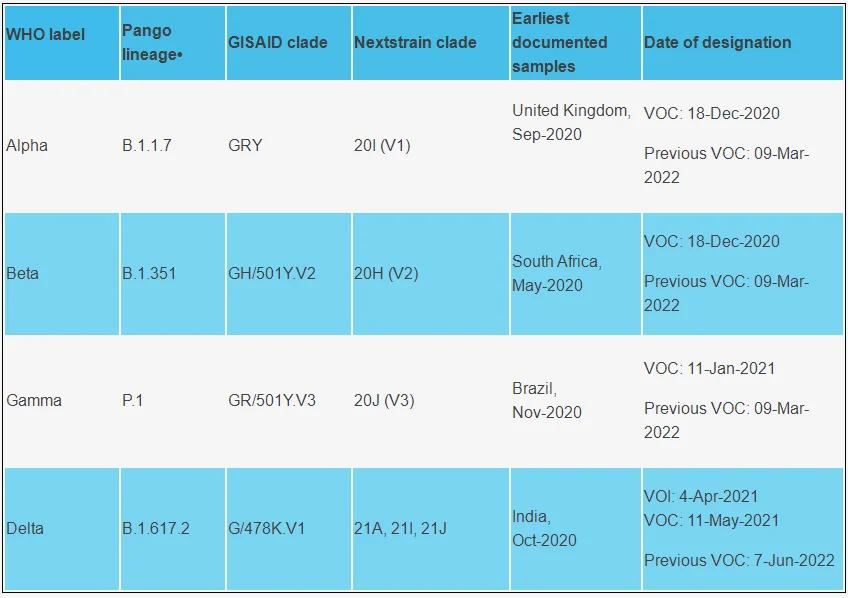
圖1 圖源:WHO
然而,自奧密克戎 (Omicron) 變異株BA.1亞型被發現以來,相繼衍生出BA.2、BA.2.12.1、BA.2.13、BA.3、BA.4和BA.5等亞型,奧密克戎變異株似乎已 “自立門户”,成為一個龐大的家族,彷彿消除了上述 “命名名額” 的問題。高突變率和高傳播速度是奧密克戎給人留下的最深印象,也曾一度引起人們對病毒擴散和疫情持續的擔憂。
先進的科研手段能讓我們能迅速掌握奧密克戎的致病特點。現在我們已經知道,雖然現有疫苗接種者以及新冠肺炎康復者體內的體液抗體對奧密克戎BA.1和BA.2株的中和活性有所降低 [1] ,且多數已上市的治療型單克隆抗體藥物被證實對奧密克戎BA.1失效 [2] ,但研究人員通過動物實驗發現,奧密克戎BA.1和BA.2株的致病性均顯著低於早期新冠毒株,一些單克隆抗體和抗病毒藥物也能抑制奧密克戎BA.2在動物下呼吸道的增殖速率 [3] 。從樸素的進化角度來説,病毒要想活下去就需要依賴宿主,“悶聲複製,快速傳播”。
如果我們可以把奧密克戎稱作一個家族的話,家族成員共同和各自的特點究竟是什麼?近期,北京大學生物醫學前沿創新中心及昌平實驗室謝曉亮教授團隊聯合中科院生物物理所、中國食品藥品檢定研究院和南開大學等機構在《自然》雜誌發表文章,系統回答了上述問題 [4] 。
新亞型免疫逃逸的原因
研究人員首先通過結構生物學手段解析奧密克戎不同亞型刺突蛋白三聚體的三維結構,並檢測了奧密克戎不同亞型受體結合域 (RBD) 與受體蛋白ACE2的結合能力。結果顯示,包括BA.4/BA.5在內的所有奧密克戎亞型RBD都保持較高的ACE2親和力,與奧密克戎BA.1相比,BA.2亞型 (包括BA.2.12.1和BA.2.13) 與ACE2的親和力略有增強。
研究人員進一步發現,相比於BA.2,奧密克戎BA.2.12.1和BA.4/BA.5對三針劑免疫者產生的抗體的免疫逃逸能力更強。對於接受過三針劑免疫的奧密克戎BA.1感染者產生的抗體,BA.2.12.1和BA.4/BA.5同樣表現出相似較強的免疫逃逸能力。也就是説,三針劑免疫者以及BA.1突破感染者產生的抗體,對BA.2.12.1和BA.4、BA.5的中和效力都顯著降低了。
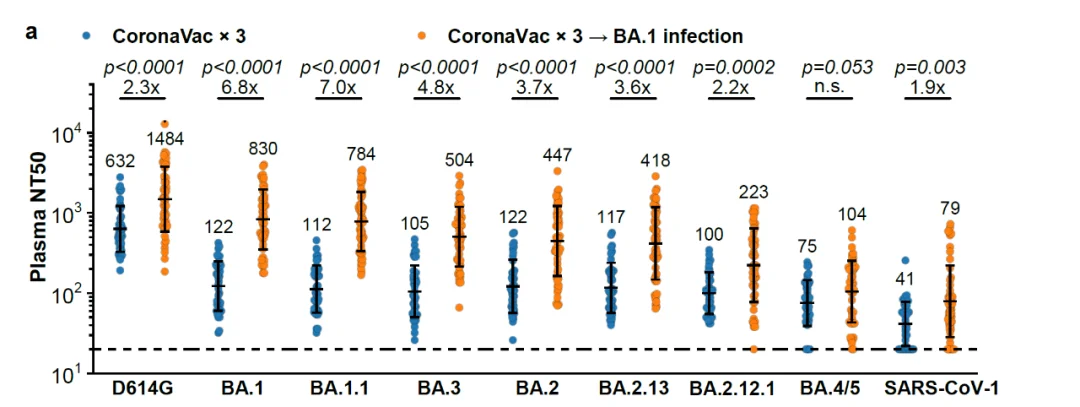
圖2 奧密克戎不同亞型對科興滅活疫苗接種者的免疫逃逸能力 | 圖源:圖源[4]
同屬奧密克戎 “家族”,為什麼成員之間還存在差異?我們首先想到的就是突變點不一樣。科研人員則更深層次、更清晰地揭示了其中奧秘。
研究人員從BA.1突破感染康復患者體內分離出生產抗體的B細胞進行單細胞測序,明確編碼抗體的核酸序列,並通過高通量深度突變掃描分析了抗體識別的表位與逃逸位點。結果顯示,三針劑完全免疫後的BA.1突破感染主要喚醒原始毒株激發產生的記憶B細胞,產生交叉結合新冠原始株和BA.1 RBD的抗體,而BA.2.12.1 (L452Q) 及BA.4/BA.5 (F486V/L452R) 的突變則可成功逃逸這些抗體的識別。也就是説,雖説BA.1和BA.2、BA.2.12.1、BA.4、BA.5是 “一家人”,但BA.1感染激發的抗體無法精準識別它的“兄弟”。
6月14日《科學》雜誌刊發的英國帝國理工學院 ROSEMARY J. BOYTON 教授團隊的論文 [5] ,也與前述發現類似。該團隊發現,疫苗免疫產生的針對奧密克戎的保護效力,與個體是否曾被新冠病毒感染及毒株種類有關。例如,某個人在疫苗接種前曾感染過某個原始株,那他在接種三劑疫苗後產生的針對奧密克戎RBD區域的抗體滴度會顯著下降。
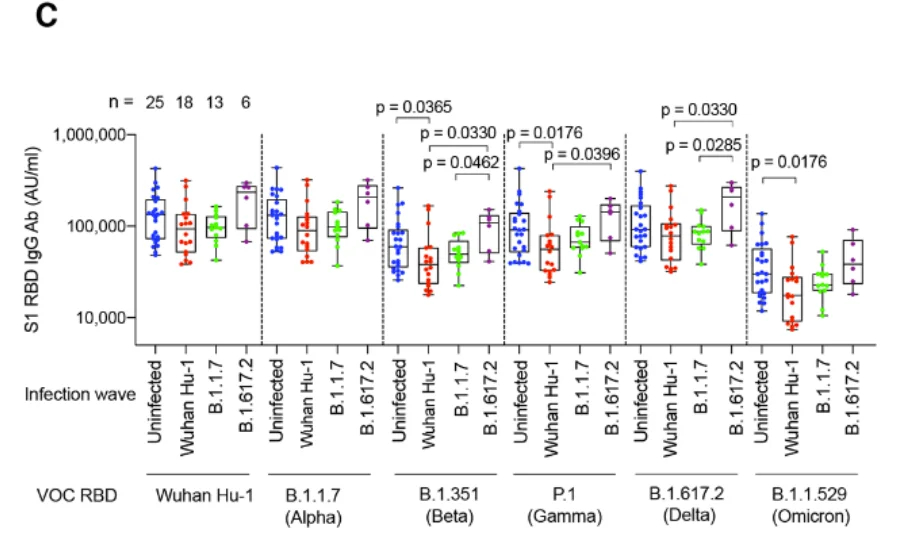
圖3個人新冠病毒感染史對疫苗產生的抗體滴度的影響**|**圖源[5]
相似的道理,如果一個人很不幸,曾被原始株感染,而後進行了疫苗免疫,但又被奧密克戎感染了。那此人體內針對奧密克戎的抗體,相比單純奧密克戎突破感染者 (未曾被其他新冠毒株感染) 體內的相應抗體滴度也下降了。
也就是説,原始株感染降低了疫苗免疫及後來奧密克戎感染 “喚醒” 免疫應答的能力,即新冠病毒感染史會影響疫苗免疫應答和機體對新一輪病毒感染的反應水平。
總結一下,假如一個人正常接種了三針劑疫苗,那麼他的體內就會產生識別新冠病毒的細胞,以產生針對病毒的抗體。如果他不幸又遭到奧密克戎BA.1感染,但很快康復,在感染過程中,BA.1會喚醒患者體內因疫苗免疫產生的細胞,激發抗體生成,但這種抗體只能較好地識別原始野生毒株和BA.1,奧密克戎其它突變亞型則基本能逃過這類抗體的識別與中和作用。
免疫原罪
抗體只識別其第一次遇見的病毒,對後續變異病毒只喚起之前病毒的免疫記憶,而不能針對突變抗原做很好的免疫應答,這種現象,被稱為 “免疫原罪”。這既體現了機體免疫應答的專一性,也同時反映其侷限性。
那麼,“免疫原罪” 的現象只在奧密克戎變異株上存在嗎?謝曉亮在接 受《知識分子》採訪時解釋,“免疫原罪” 不是一個新概念,流感疫苗也面臨同樣的問題。流感疫苗為什麼每年都要更新?正是因為流感病毒也在不斷變異,人們所接種的流感疫苗,喚起的都是針對原先 (比如上一年) 毒株的抗體,而新的變異株能逃逸這些抗體的中和作用。
他強調,現在的 “免疫原罪” 絕對不是奧密克戎才有的,只不過之前的新冠變異株的變異程度不足大,原有的疫苗還能管用。現在奧密克戎跟原始株的差異則非常大,因此對疫苗的免疫逃逸也越來越多。
杜克-新加坡國立大學醫學院新發突發傳染病研究所所長、病毒學家王林發今年5月曾在《科學》雜誌上發表評論文章,根據Omicron毒株的免疫學特徵,建議將其定義為 SARS-CoV-3,認為它已經是一種與現在已有的新冠病毒變異株完全不同的病毒。
此前有説法認為,感染了一次新冠後,人體形成的免疫力會對變異株起到一定的交叉免疫保護作用,是什麼因素決定着在感染一個新毒株時,體內的抗體會產生免疫交叉保護,還是發生免疫逃逸?對於這一問題,謝曉亮表示,關鍵還是變異株新的突變位點。他們的研究發現,BA.2.12.1、BA.4與BA.5都有L452突變,這一突變以及BA.4和BA.5攜帶的F486V突變會導致這些變異株在面對人體因接種疫苗或感染BA.1產生的抗體時發生免疫逃逸。
不是 “天然疫苗”
此前,有很多人都曾認為奧密克戎是新冠肺炎的 “天然疫苗”,其中的代表人物是比爾·蓋茨,他在今年早些時候曾説,奧密克戎變異株就是一個產生T細胞和B細胞免疫力的疫苗,而且它向世界傳播,比我們用疫苗接種來得更快、做得更好。
謝曉亮説,在當時的科學認識下,比爾·蓋茨説的也不是完全沒有科學根據。早期就有研究表明,奧密克戎引發的症狀集中於上呼吸道,以輕症居多,相比德爾塔等毒株來説,是一個毒力相對較弱的病毒。然而,由於奧密克戎超強的傳播力與突破感染能力,它會在人羣中形成一個比過去更加龐大的感染基數,而那些年齡偏大的、合併有基礎病的感染者依然有較高的死亡風險,這樣一來,奧密克戎引發的超額死亡與總死亡人數並不比德爾塔要少,這在美國已有數據可證明。
但更重要的是,謝曉亮指出,根據他們的這一研究及國外近期的一些研究結果,奧密克戎新變異株具有很強的免疫逃逸能力,可以針對性地逃逸早期奧密克戎變異株感染所誘導的抗體。感染了奧密克戎BA.1的康復者,並不會對奧密克戎其他變異株產生很高的免疫力。由於新冠病毒存在 “免疫原罪” 現象並且可以快速進化出免疫逃逸突變位點,通過奧密克戎感染實現羣體免疫是極難實現的。從這個意義上來説,奧密克戎是天然疫苗的説法並不成立。
“這一發現意味着,基於BA.1的奧密克戎疫苗所誘導出的抗體對新變異株將不具有廣譜保護效力,可能已不適合作為現有免疫背景下的疫苗加強針。尤其對於BA.1滅活疫苗來説,更是如此。” 他説道。
那我們還需要研發針對奧密克戎的疫苗嗎?
“YES!” 對此,謝曉亮明確表示,研發針對奧密克戎的加強針疫苗依然是很有必要的,但是可能需要改變思路,不是利用天然的毒株或蛋白直接生產疫苗,而是通過人工設計抗原研發出廣譜疫苗。這個方向在業內已經提出了很長一段時間,國內外很多團隊正在研發,目前仍處在設計階段。
謝曉亮進一步解釋,所謂廣譜疫苗,就要設計出一個在遞送進人體後,能夠激發出同時具有幾種重要表位的抗體的抗原。實現廣譜疫苗,主要靠蛋白疫苗和mRNA疫苗等技術路線。不過,廣譜疫苗不容易做,流感的廣譜疫苗也提了很多年,尚未實現。
中和抗體或有更多作為
同時,針對新冠病毒抗體藥物,謝曉亮團隊研究發現現存的大多數抗體藥物都對奧密克戎變異株的中和活性大大下降。BA.2、BA.4 和 BA.5攜帶的S371F、D405N和R408S位點突變導致大部分乙型冠狀病毒支系B (sarbecovirus) 廣譜抗體 (如S309) 失活,而LY-CoV1404 (Bebtelovimab) 和COV2-2196/COV2-2130 (Evusheld) 仍然對 BA.2.12.1 和 BA.4/BA.5 保持高中和活性。
該團隊篩選出一對廣譜乙型冠狀病毒中和抗體組合SA58和SA55,該抗體組合對能高效中和包括奧密克戎株新亞型在內的所有新冠突變株,及非典病毒,蝙蝠RaTG13,穿山甲Pangolin-GD等Sarbecovirus病毒,有望成為兼具強效預防和治療效果的藥物。
與疫苗類似,謝曉亮説,奧密克戎大家族的免疫逃逸特性要求科研人員找到廣譜抗體。他們的優勢是高通量酵母顯示深度突變掃描技術,利用這一創新技術,他們找到了很難被逃逸的廣譜乙型冠狀病毒中和抗體。對此,他表示,“找到活性高的中和抗體不難,關鍵是要找到不易被逃逸的中和抗體。”
在謝曉亮看來,中和抗體藥物的作用要比目前已知的更為廣泛。他解釋道,抗體經過工程改造後的半衰期可以達到3個月左右,在臨牀應用中,可以半年打一次。全人源抗體由於副作用小,除了用做治療,也可以用來預防。
阿斯利康的Evusheld 作為類似中和抗體預防藥物已證明對預防感染有效率85%,遠高於滅活疫苗和mRNA疫苗。中和抗體的優勢是比疫苗更安全有效,特別是對於疫苗反應較弱的人羣,但缺點是價格比較貴。抗體現在的價格是一針數千元,如果將來技術普及大規模推廣,價格可以下降到數百元,未必比一個療程的小分子藥成本高, 但仍然高於疫苗接種,因此更適宜於老年人、密接者、免疫缺陷人羣等高風險人羣的小範圍使用。
謝曉亮表示,當我們擁有更有效的疫苗與藥物後,在面對新冠病毒的戰役中才能掌握更多的主動權並進一步完善防疫策略。
參考文獻:
[1] Rössler A, Riepler L, Bante D, von Laer D, Kimpel J. SARS-CoV-2 Omicron Variant Neutralization in Serum from Vaccinated and Convalescent Persons. N Engl J Med. 2022 Feb 17;386(7):698-700. doi: 10.1056/NEJMc2119236.
[2] Cao, Y., Wang, J., Jian, F., Xiao, T., Song, W., Yisimayi, A., Huang, W., Li, Q., Wang, P., An, R., Wang, J., Wang, Y., Niu, X., Yang, S., Liang, H., Sun, H., Li, T., Yu, Y., Cui, Q., Liu, S., … Xie, X. S. (2022). Omicron escapes the majority of existing SARS-CoV-2 neutralizing antibodies. Nature, 602(7898), 657–663. https://doi.org/10.1038/s41586-021-04385-3
[3] Uraki, R. et al. Characterization and antiviral susceptibility of SARS-CoV-2 Omicron/BA.2. Nature https://doi.org/10.1038/s41586-022-04856-1(2022).
[4] Cao, Y., Yisimayi, A., Jian, F. et al. BA.2.12.1, BA.4 and BA.5 escape antibodies elicited by Omicron infection. Nature (2022). https://doi.org/10.1038/s41586-022-04980-y
[5] C. J. Reynoldset al., Immune boosting by B.1.1.529 (Omicron) depends on previous SARS-CoV-2 exposure. Science10.1126/science.abq1841 (2022).