章雪晴團隊開發新型吸入式核酸納米遞送系統治療肺纖維化_風聞
天府财经网-天府财经官方帐号2022-07-08 13:50
特發性肺纖維化(idiopathic pulmonary fibrosis,IPF),是進行性的間質性肺病並伴有持續的肺功能損傷。目前全球約有500萬人患有IPF,平均中位生存期為3-5年。然而迄今為止的上市藥物僅有吡非尼酮和尼達尼布,且為FDA弱推薦藥物,存在巨大未滿足的臨牀需求。
2022年6月22日,上海交通大學藥學院章雪晴教授團隊聯合新澤西理工學院許曉陽教授團隊在Science Advances上發表了題為Inhaled siRNA nanoparticles targeting IL11 inhibit lung fibrosis and improve pulmonary function post-bleomycin challenge的研究論文。基於可吸入的核酸納米遞送載體,成功遞送小干擾RNA(siRNA)到達纖維化小鼠的肺部,實現肺纖維化的治療。

siRNA具有治療各種疾病的巨大前景,但目前上市siRNA藥物全部使用肝部遞送技術,尚無上市載體能將siRNA安全有效的遞送到非肝器官或組織。本研究利用脂質化合物製備的納米粒包載針對IL11的siRNA(siIL11)得到siIL11 PPGC NPs,具有以下突出優勢:1)具有良好的穩定性,能承受霧化過程中產生的剪切力並維持霧化前後的粒徑、形貌、細胞攝取和包封率不變;2)可濃縮成小體積;3)霧化後穿過肺黏液層到達肺組織深處。
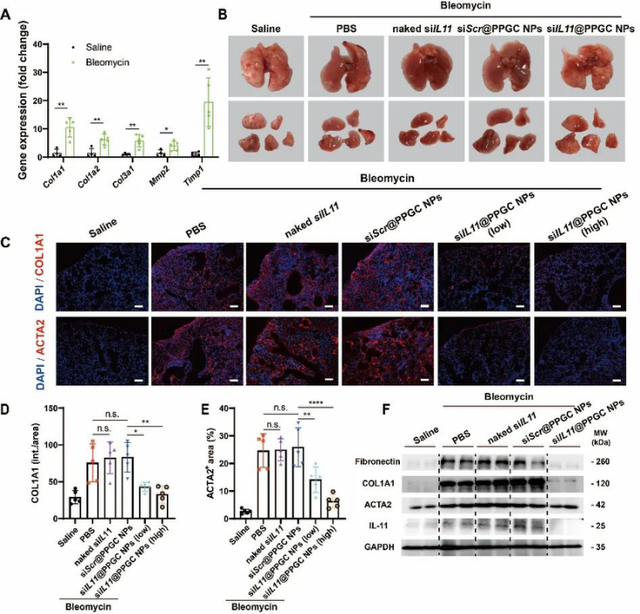
體外實驗表明,siIL11 PPGC NPs可以顯著抑制成纖維細胞向肌成纖維細胞的轉化,細胞外基質的沉積以及成纖維細胞的遷移。在博來黴素誘導的小鼠肺纖維化模型中,霧化吸入的siIL11 PPGC NPs能夠有效降低ACTA2和COL1A1的表達,顯著降低羥脯氨酸含量並改善纖維化面積和膠原含量。該納米藥物不僅抗纖維化效果顯著,而且顯著改善肺纖維化小鼠的肺功能,為修復肺組織損傷和干預肺纖維化後的功能恢復提供新的治療方法。siIL11 PPGC NPs沉默IL-11的表達,抑制ERK磷酸化,在介導抗纖維化治療中發揮了重要作用。
該研究中採用的納米粒經吸入給藥後,沉積在整個細支氣管和肺泡上皮中,大大提高依從性並減少全身暴露,為肺纖維化的治療提供了巨大契機。此種可吸入核酸遞送納米載體,實現靶向遞送治療核酸分子至肺部,為探索目前被定義為治療肺部疾病的“難以成藥”的靶點提供了潛在的機會,在治療包括IPF在內的多種呼吸系統疾病方面表現出巨大的臨牀應用前景。
據悉,以本研究為基礎,章雪晴教授團隊在可吸入核酸納米遞送系統的研發上不斷迭代優化,目前已形成更加安全有效的第二代可吸入核酸遞送載體,並應用到抗肺纖維化的核酸納米藥物開發的轉化工作中。
以章雪晴博士作為領銜人的榮燦生物技術團隊在核酸遞送領域有十幾年的積累,一直致力於開發獨立自主知識產權的核酸納米遞送系統,現已就新型可離子化脂質化合物及LNP載體系統申請了多項國內、國際發明專利,為開發創新型核酸藥物奠定了堅實的基礎。