當糞便成為“黃金”,糞便的明天是什麼?_風聞
根新未来-2022-07-27 09:09
文/觀察未來科技
糞便是人們最熟悉的排泄物。曾有一組美國學者估算,正常成年人每天排便量平均約為 400-500 克,一個人一年就會產生約 145 千克的糞便。過去,這些糞便對人類來説,顯然是個不小的負擔,需要人類的堆肥、焚燒、封存或填埋。
而現在,隨着人們對細菌影響力的日漸深入,糞便正在展現出別樣的價值。糞便對於人體微生態結構的重建可能,使得糞便移植成為許多疾病最積極的治療方式。於是,從糞便移植研究的興起,到糞便銀行的建立,當前,糞便似乎正在成為一種新的“黃金”。
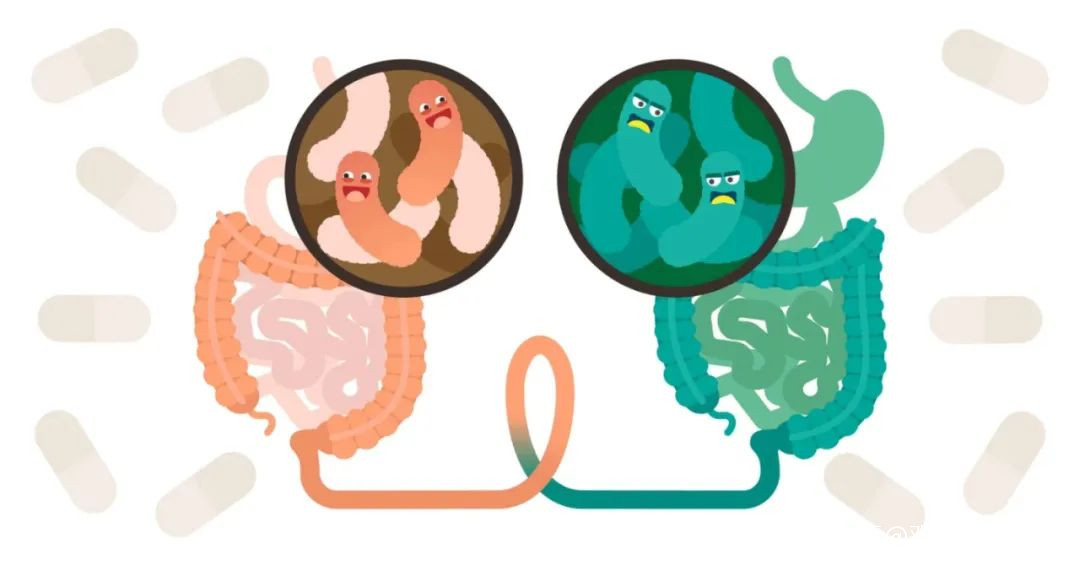
糞便的真相
到目前為止,大多數人對糞便的認識,大概都停留在“人體排泄物”的層面。事實也確實如此,當人們攝入各類色澤繽紛,質地多樣的食物時,從另一頭出來的,往往救變成了氣味令人掩鼻、顏色單調、質地均勻、有一點軟綿的、帶有裂紋的條狀物,即糞便。而產生糞便的這個過程,則發生在我們的腸道里。
人們常把腸道視為一條通到肛門的管道,這條管道會把人們攝入的食物慢慢轉變為噁心的糞便。可以説,腸道就像一種肉質的污水處理系統,從食物中提取出我們需要的養分,排放出我們不要的垃圾。不過,止於此的認識顯然太過簡單了——糞便是垃圾,但又不完全是垃圾。
科學家對於糞便的分析結果顯示,它和一般生物體的很多成分一樣,大部分(大約75%)是水。其餘固體成分包括膽固醇和一些其他脂質,幾乎不含蛋白質,還有一些無機物,比如骨骼和牙釉質的主要成分磷酸鈣。糞便裏面還有一些人體無法消化的食物,比如纖維素和膳食纖維中的成分。
將糞便放到放到顯微鏡下,人們還會看到腸壁細胞,它們是在糞便穿過腸道,進入直腸再從肛門出去的過程中從腸壁脱落的,正是這些細胞菜讓研究人員能夠從糞便中收集到遺傳物質DNA。
**如果把顯微鏡的放大倍數調大,還會看到固體中大約1/3,有時也會高達60%的,就是細菌微生物。**糞便的重量和臭味就是因為這些微生物所造成的,這些單細胞生物聚集在人類的糞便裏,也正是它們的存在給人類提供了線索,讓人類能夠了解腸道里究竟在發生着什麼。
要知道,人體內的腸道菌羣種類繁多,包括了至少100萬億個細菌,是人體細胞總數的10倍,分屬1000多個種,具體來看,人體腸道菌羣按來源分類,可分為原籍和外籍菌羣,原籍菌羣多為腸道正常菌羣,除了主要的細菌外,腸道微生物還包括病毒羣、真菌羣、螺旋體羣等。
**這些腸道菌羣按一定的比例組合,相互制約、相互依賴,在質量和數量上形成生態平衡。**腸道菌羣的平衡也在很大程度上支撐了人類的健康——腸道微生物在消化、調解人體免疫功能、抵禦疾病以及生產人體必須的維生素方面都扮演着重要角色。
比如**,在協助人體消化****方面,**一些腸道微生物具備豐富的生物化學途徑和代謝途徑,能夠消化口腔、胃和小腸難以分解的碳水化合物蔬菜水果裏那些結構複雜的支鏈多糖。某些情況下,這些細菌還能把這些大分子分解為簡單的糖分子,比如人體可以吸收的葡萄糖。另外,人體的腸壁會分泌大量黏液,幫助內容物通過腸道,黏液裏常有結構複雜的碳水化合物,也能被這些細菌消化。
腸道微生物除了為分解人們愛吃卻難以消化的分子提供援助服務,還是生產某些維生素的內置生化工廠。眾所周知,維生素是人體正常行使功能不可缺少的微量物質,但人體自身無法生成,而除了從食物中攝入維生素外,腸道微生物羣落中的某些菌種也能夠合成和供應包括維生素B、生物素、維生素B12,以及維生素K2等。
**另外,腸道菌羣還能夠讓人們更容易從食物中吸收某些重要的金屬元素。**人體的生理機能和基本結構有賴於鈣、鎂和鐵等金屬,一般來説,金屬的活性較強,我們會從食物中少量攝取以分子或離子形式存在的金屬。而消化道內由細菌分解產生的脂肪酸有助於我們更好地吸收這些金屬。
更重要的是,腸道微生物還有一項能力,就是協助人體抑制有害病原菌的生長,也就是“通過競爭排斥進行種間競爭”。有害細菌通過入侵腸壁細胞對人體造成傷害,有些情況下還會入侵人體內的其他細胞。而有益的或者無害的細菌附在腸道內壁,則會把可用的空間佔滿。這就讓那些有可能入侵細胞、對人有害的細菌種類難以進入人體,難以對人體產生傷害。
可以説,糞便之所以這麼有價值,就是因為糞便中的微生物指向了腸道中發生的一切,而腸道微生物,則對人體健康具有重要意義。
糞便移植大有所用
實際上,我國早在1700年前,就已經有古人認識到糞便可能的價值,並出現了最早的糞便移植。東晉時期,葛洪著《肘後備急方》中記載用新鮮的糞汁或發酵的糞水治病:“飲糞汁一升,即活。”書中還描述了用人糞清治療食物中毒、腹瀉、發熱並瀕臨死亡的患者。明代李時珍所著的《本草綱目》則記載了多達二十多種用人糞治病的療方。
17世紀法布西里(Fabricius)等發現在牲畜藥物中加入糞菌可增強藥物的止瀉作用,1958年首例糞便移植獲得成功,艾斯曼(Eiseman)等用人糞清灌腸的方法治癒了4例對萬古黴素和甲硝唑治療無效的偽膜性腸炎患者,但其後糞便移植並未受到重視,逐漸淡出人們的視野。
直到20年後,1978年,難辨梭狀芽孢桿菌感染被認為是導致偽膜性腸炎的主要原因,並與抗生素的使用密切相關,因為糞便移植能夠通過重建受損的腸道菌落來抵禦難辨梭菌的腸道定植和感染,所以糞便移植再次得到關注。
不過,即使對於艱難梭菌感染而言,也不能隨隨便便進行糞便移植,必須對糞便進行嚴格的篩查,排除諸如肝炎或艾滋病病毒等病原體。對於當時來説,這個耗時的過程排除了許多人選,最後可能很難找到捐贈者。即便如此,糞便移植依然成為治療致死率極高的艱難梭菌感染的最後一道防線。
於是,一些醫療機構只能採取冷凍的辦法,把符合標準的糞便樣本冷凍起來。非營利組織“開放生物羣”(OpenBiome)就運營着這樣一家糞便銀行。潛在的捐贈者如果通過了一系列篩選測試,他們的糞便就會經過過濾、膠囊包裝,最後被冷凍起來,陸續送到有需求的醫院。
在現在看來,吞下冷凍大便膠囊的行為,確實是一件很奇怪的事情——冷凍大便膠囊看起來是一顆普通藥丸,但其包裝在很大程度上毫無典型特徵。每顆藥丸都出自一名志願者之手,而非工廠的流水線,每一次生產都各有不同。這些膠囊之間的差異之大,驚動了美國食品藥品監督管理局(FDA)。
**終於,2013年5月,FDA決定把糞便作為一種藥物來管理,**FDA宣佈可將人類糞便作為藥物使用和監管,使得糞便移植技術的研究前景更加廣闊,也得到了全世界科學家的高度關注。同年,糞便移植技術被美國《自然》雜誌評為“人類年度十大科學進展”之一。
從糞便移植的醫學成就來看,通過糞便移植成功治療克羅恩病是糞便移植髮展至今最令人興奮的一個突破。克羅恩病是一種自身免疫性疾病,患者的免疫系統會攻擊胃腸道,進而使腸道出現炎症、出血和瘢痕等症狀。據統計,美國目前每10萬人中就有5人患有這種疾病,由於數據不足或存在誤診的可能,患病人數甚至可能更多。
**克羅恩病是一種炎性腸病,會損害腸道。**它與腸易激綜合徵有很大不同,腸易激綜合徵雖然也是腸道疾病,但該病不會引起腸道炎症或潰瘍。潰瘍性結腸炎也是一種炎性腸病,該病一般發生在結腸和直腸,而克羅恩病會影響整個胃腸道。與腸易激綜合徵不同,克羅恩病和潰瘍性結腸炎都無法被完全治癒。
針對克羅恩病的治療方法有很多,但療效各不相同。過去,最常見的治療方法是使用消炎藥和免疫抑制劑,目的是減輕腸道炎症。這些療法通常是直接針對腸道的。除此之外,醫生還會採取手術來切除患者小腸和結腸受損的部分。其他治療方法還有增加腸道中的益生菌、益生元等。
**而糞便移植療法卻對克羅恩病展現出驚人的療效。**糞便移植的過程也比較簡單,就取少量健康人的糞便,加水後用攪拌器攪拌,然後灌入克羅恩病患的腸道。事實證明,到目前為止,這種治療非常有效。糞便移植療法在克羅恩病人身上的成效使研究人員對也其他疾病進行類似的研究。
糞便移植的現在和未來
糞便移植的醫療前景讓人們對糞便移植的興趣呈指數級增長,針對在各種疾病上嘗試該技術的呼聲也不斷地為科學家們增加壓力。但問題是,人們還不清楚這種做法的長期風險——這也是攔阻糞便移植髮展的重要原因。
動物實驗明確表明,移植微生物組會讓接受者更容易肥胖,也容易發展出炎性腸症、糖尿病、精神病、心臟病,甚至癌症等;然而,就任何特定的微生物菌羣是否會給人類帶來這些健康風險,研究人員們仍然無法準確預測。
對於一位70歲的艱難梭菌感染患者來説,這個問題可能並不重要,因為艱難梭菌感染患者想要的只是馬上得到治癒。**但是對年輕人來説,**考慮到糞便移植的長遠影響則是更為重要的。
無疑,看起來糞便移植實在是太簡單了,任何人都可以在家裏嘗試。互聯網甚至都能找到相關的教學視頻,還有聚集了DIY移植者的大型線上社區。可以肯定的是,這些資源幫助了許多真正有需要,但又遭到醫生拒絕的病人。但是,這種移植操作容易,也很可能讓獲得錯誤信息的人採取錯誤的行動。在醫療實驗室外,人們難以事先篩查捐贈者的病原體**。**
因此,對於糞便移植來説,當前,更重要的是,規範這種技術,收集捐贈者和受體的系統數據,並創建一個報告意外副作用的系統,而不是讓人們隨意使用彼此的糞便,因為把許多未知物植入患者的腸道,這種行為無異於賭博。
説到底,當前的糞便移植仍只是一種權宜之計,**糞便移植的最終,應該是清楚地分辨出糞便的性質,即****創造一個特定的微生物菌羣,能夠把糞便捐贈者提供的益處複製出來。**也就是説,最終實現的,將是沒有糞便的糞便移植,使用的是糞便替代品。
此前,有研究團隊曾基於此,培養了一名從未服用過抗生素的41歲女性腸道里的細菌,並去除了哪怕顯示出一絲毒性和抗性的任何細菌。最後,一個由33株細菌組成的菌羣留了下來,研究人員把其命名為“RePOOPulate”,並在兩個艱難梭菌患者身上測試了這種混合物,最終使他們在數日內恢復了健康。
研究人員認為,我們可以把這些混合物視為簡化的糞便或複合的益生菌。它們都包含被定性為“好”的菌株,可以根據標準化的配方一次又一次地製造出的相同的東西——這也好過性質不明、高度不可控的糞便中的菌羣。
當然,新的問題是,這些合成菌羣也同樣面臨益生菌所面臨的問題:沒有哪個單一的細菌可以治療所有的疾病,甚至患有某種特定疾病的所有人**,而一個生態系統卻能**。糞便移植的意義就在於腸道微生態結構重建。因此,糞便移植一定是未來的重要技術,但不是現在。