G12C突變難造“藥王”,KRAS靶點需要衝破適應症天花板_風聞
氨基观察-生物医药新时代的商业智库和价值灯塔2022-07-28 12:28
1年前,安進KRAS G12C抑制劑獲批,徹底改寫KRAS靶點不可成藥歷史,讓市場為之振奮。
也正因此,這一領域湧入了眾多國內藥企。除了進度領先的再鼎醫藥、加科思等藥企之外,還包括益方生物、勁方生物、勤浩生物、貝達藥業、君實生物、艾力斯等。
看上去,KRAS G12C抑制劑成了又一個競爭激烈程度不輸PD-1的市場。這是否意味着,KRAS靶點已經沒有看點了嗎?答案顯然並非如此。
作為首個被人類發現的致癌基因,KRAS靶點固然已經告別“不可成藥”歷史,但依然還有很長的路要走。
因為,KRAS G12C突變只是該靶點極為細分的一個種類。對於任何一家藥企來説,僅靠KRAS G12C抑制劑也很難成為“藥王”。
泡沫本身並不可怕。對於任何一個行業來説,泡沫都是利弊共存。泡沫的好處在於,會吸引大量資源投入,助推行業快速發展。
對於需要衝破天花板的KRAS靶點來説同樣如此。在KRAS G12C抑制劑之後,國內藥企開始圍繞KRAS靶點進行廣泛佈局。
較量,才剛剛開始。
/ 01 /
極度分裂的大靶點
作為人類歷史上第一個被發現的致癌基因,RAS基因突變與約20%的腫瘤有關。RAS基因突變,會不斷刺激細胞增殖、遷移,導致腫瘤發生,常見於胰腺癌、結直腸癌、肺癌領域。
RAS基因突變分為多個類型,包括KRAS、NRAS、HARS。其中,KRAS是最為常見的突變種類,佔比約85%。
簡單換算下,KRAS基因突變大概與17%左右的腫瘤相關。單從這一數字來看,KRAS基因突變無疑是一個大靶點。
但事情沒有這麼簡單。KRAS靶點雖大,卻難以聚焦。因為突變位點太多,導致KRAS基因突變被分成了諸多細分子集,包括G12C、G12D、G13D突變等等。
極度分裂的情況下,KRAS靶點細分子集的患者羣體規模並不大。
以美國市場為例。如下圖所示,雖然美國每年新發腫瘤患者中,KRAS突變患者數量超過10萬人。但佔比最高的G12D突變,新發患者人數不過5.1萬人,而像G12V、G12C等則是更少。
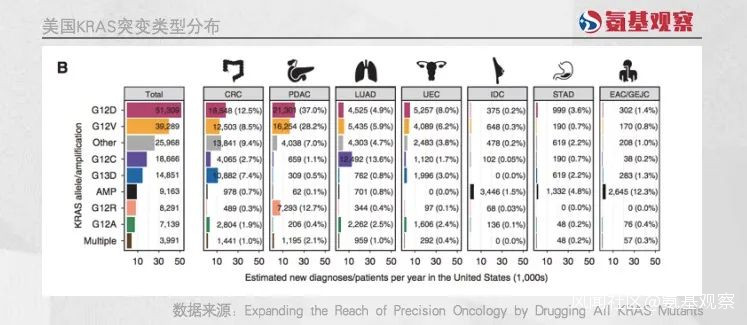 並且,這些突變患者又存在於各個不同的腫瘤裏面,使得市場進一步分散。例如當前開發最為火熱的KRAS G12C抑制劑,主要患者在肺癌領域。這導致藥企開發的難度和成本都大幅增加。
並且,這些突變患者又存在於各個不同的腫瘤裏面,使得市場進一步分散。例如當前開發最為火熱的KRAS G12C抑制劑,主要患者在肺癌領域。這導致藥企開發的難度和成本都大幅增加。
國內也是如此。因為種羣差異,相比於海外國內KRAS G12C突變屬於更為罕見的類型。根據益方生物招股書,目前國內最為常見的突變位點之一KRAS G12C,2020年發病人數只有約為4.3萬人。
而這4.3萬人,又存在於肺癌、結直腸癌和膽管癌等細分市場。發病率方面,肺癌大約是4.3%,結直腸癌大約是2.5%,膽管癌則是2.3%。
很顯然,對於藥企來説,要想在KRAS靶點站穩腳跟,需要滿足更多患者需求,以衝破靶點割裂導致的天花板。當然,要做到這一點並不容易。
/ 02 /
逐個擊破曙光漸顯
目前,儘管針對KRAS G12C突變的非小細胞肺癌患者已經有所突破,但對其它適應症以及其它類型的突變依然需要藥企們不斷探索。
一直以來,針對KRAS基因突變的靶向性成藥之路頗為坎坷,核心原因在於不管是直接“殺死”基因突變的KRAS蛋白,還是抑制其複製功能都很困難。
KRAS蛋白是一種非常小的分子,表面相對光滑,難以找到用於藥物結合的“口袋”,無法直接消滅;KRAS對提供能量的核苷酸GTP具有超強的親和力,因此普通藥物很難與GTP競爭,間接打擊KRAS蛋白。
某種程度上來説,KRAS G12C抑制劑的誕生是幸運的。因為科學家們發現,KRAS G12C突變點是從甘氨酸突變為半胱氨酸,這種突變位點與不可逆抑制劑的結合破壞了switch-I和 switch-II口袋,才讓我們有了可乘之機。
儘管取得了這一成功,但由於其它突變並非半胱氨酸。在欠缺非半胱氨酸以外殘基的低親核性的情況下,靶向KRAS的其他非半胱氨酸熱點突變體的共價藥物仍有待開發。
當然,事在人為。隨着KRAS G12C抑制劑的突破,也給人們帶來更多的靈感。如今,這一成功便有可能複製到KRAS G12S突變體上。
日前,在攻破KRAS“不可成藥”性中做出突破性貢獻的Kevan M. Shokat教授團隊在Nature Chemical Biology上發表最新研究顯示,通過特異性共價抑制的邏輯,將β-內酯的結構成功添加在Mirati公司KRAS G12C抑制劑adagrasib的骨架上。
經過多次優化生成的抑制劑,能夠特異性與KRAS G12S突變體共價結合,顯著降低突變體的活性,同時並不會對野生型KRAS蛋白產生影響。
雖然這一研究聚焦於KRAS G12S突變體,但是他們相信這一策略為靶向絲氨酸增添了一種新工具,可以用於靶向其它攜帶絲氨酸的靶點。至於是否可行,還需要時間來驗證。
相比之下,非共價可能是一條更有前景的道路。實際上,Mirati公司針對KRAS G12D突變已經有所進展。
在Adagrasib基礎上,Mirati公司採用吡啶並嘧啶骨架進一步篩選和優化,最終得到的一款選擇性非共價KRAS G12D抑制劑,目前已進入臨牀階段。
在國內,針對KRAS G12D突變,同樣有包括恆瑞醫藥、艾力斯、益方生物等藥企展開研究,其中恆瑞醫藥KRAS G12D抑制劑已於日前獲批臨牀。
綜合來看,雖然目前我們針對KARS突變已經成藥的還只有KRAS G12C抑制劑,但針對其它突變的藥物,也正在逐漸迎來勝利曙光。
/ 03 /
泛KARS突圍戰已經打響
在逐個擊破之外,也有藥企有着更大的夢想——希望通過泛KARS藥物直接突圍。相比於逐個擊破,泛KARS藥物的開發策略要更多。
目前,最為熱門的方向是通過阻擊KRAS上游通路,來間遏制泛KRAS蛋白活性。也正因此,KRAS上游的SOS1或者SHP2靶點,因為機制明確,且成藥難度更低的特點,成了藥企們的香餑餑。
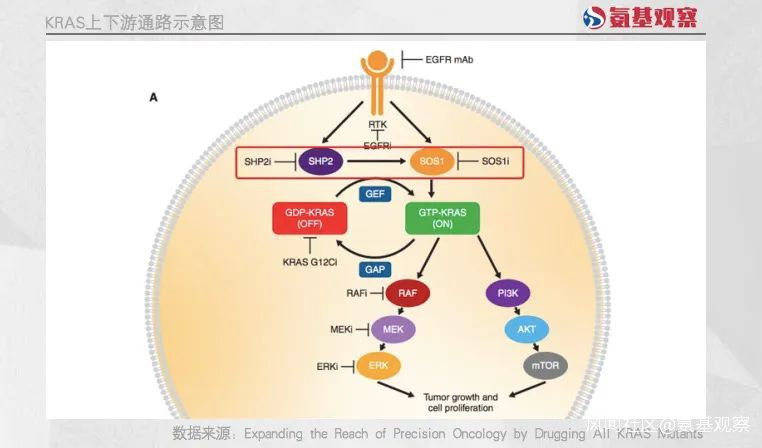 例如SHP2抑制劑,便吸引了眾多國內藥企入局,包括加科思、諾誠健華,聖和藥業,貝達藥業,勤浩醫藥等公司都在開展研究。
例如SHP2抑制劑,便吸引了眾多國內藥企入局,包括加科思、諾誠健華,聖和藥業,貝達藥業,勤浩醫藥等公司都在開展研究。
不過,能否通過上游通路來遏制KARS突變還是一個未知數,畢竟人體機制過於複雜。
雖然KRAS基因突變與上游通路SHP2、SOS1等蛋白息息相關,但除此之外也受到其他細胞蛋白的支持,僅僅遏制上游一個通路或許不足以帶來深刻和持久的臨牀益處。
正如下圖所示,目前所有藥企的臨牀都還處於早期階段,未來還充滿着變數。
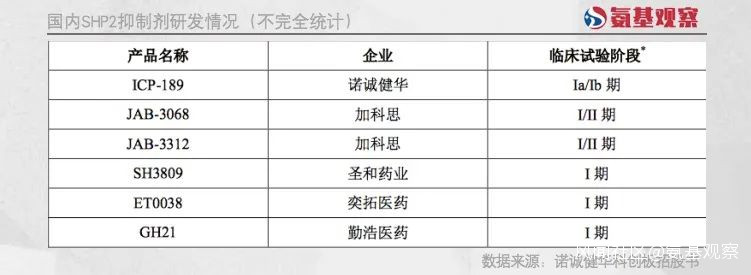 不過,即便間接遏制的之路走不通,直接覆蓋各個類型的KRAS突變的解題思路依然保有希望。
不過,即便間接遏制的之路走不通,直接覆蓋各個類型的KRAS突變的解題思路依然保有希望。
目前,包括勃林格殷格翰和Revolution Medicines等海外藥企,便沿着這一思路尋找答案,邏輯基本一致:通過直接遏制RAS基因,達到同時阻斷RAS異構體的目的。
另外,隨着PROTAC技術的進步也讓我們看到更多可能。因為PROTAC藥物不需要和靶點蛋白長時間高度結合,就能抓住靶點蛋白並將其降解,如此一來,就解決了KRAS靶點不可成藥的難題。
當然,不管是直接遏制RAS基因,還是通過PROTAC技術曲線救國,都如SOS1抑制劑或SHP2抑制劑一樣,還需要通過紮實的臨牀數據來證明自己。
/ 04 /
總結
雖然距離完全攻克KRAS靶點還有困難,但在KRAS G12C突變領域迎來突破之後,針對KRAS突變的藥物研發,已經迎來黃金時代。
未來,相信我們一定可以看到泛KRAS藥物和針對單個突變的兩類藥物同台競技,給全球患者帶來更好的治療選擇。
這並不意味着,哪一種技術路線就是唯一答案。正如Revolution Medicines一樣,其在開發泛KRAS藥物同時,也在針對單個突變的藥物進行廣泛佈局。這正是支撐其超20億美金市值的關鍵。
對於針對KRAS突變的藥物來説,更核心的在於,能夠在明確定義的患者羣體中,具有深度和持久的抑制效果,以及更好的安全性,這些要素才是最為關鍵的。
如何權衡眾多因素,滿足KRAS基因突變患者臨牀未滿足需求,同時建立自身護城河,也是對每一家藥企的考驗。
