Nature子刊:新顯微技術讓“不可見”的生物分子無處遁形_風聞
中国生物技术网-中国生物技术网官方账号-2022-09-13 09:14
瞭解特定蛋白質在細胞和組織中是如何排列的對科學家們來説至關重要。因為,這種精微的結構是機體生物功能和疾病狀態的核心。然而,在活細胞內,一大堆蛋白質和各種生物分子“擠”在了一起,雜亂無章的團簇給試圖觀察它們的科學家帶來了難題。由於蛋白之間的距離太小,傳統方法中用於使它們可見的熒光標記對它們束手無策,從而限制了通過標記獲取生物分子信息的可能。
近日,發表在**《Nature Biomedical Engineering》上的一項新研究中,來自麻省理工學院**(MIT)的研究團隊開發了一種新技術克服了上述困難,使那些擠在一起“不可見”的分子顯露“真容”。該技術不僅可以實現低至幾十納米的超分辨率,而且還可以“剝離”細胞和組織中的生物分子以實現 “去擁擠”化,從而使科學家可以發現以前從未見過的細胞和組織內景觀。

這種名為“擴張顯示(Expansion Revealing,ExR)”的新方法該團隊此前開發的擴張顯微成像技術之升級版本。
通常,對細胞內的特定蛋白質或其他分子進行成像需要用與靶蛋白結合的抗體攜帶熒光標籤對其進行標記。抗體長約10納米,而典型的細胞蛋白直徑只有約2至5納米。因此,如果靶蛋白過於密集,抗體就無法接觸到它們。
這一直是傳統成像技術的障礙,也是該團隊於2015年首次開發擴張顯微成像技術時的障礙。在原始版本的技術中,研究人員在擴張組織之前將熒光標記附着在感興趣的分子上,但他們必須要用一種酶來切碎樣品中的蛋白質,以便組織能被擴張。然而,標記是事先做好的,這意味着,在組織擴張後,標記就成了問題。
為了克服這一障礙,研究人員需要找到一種能在保持蛋白質完整性的同時擴張組織的方法。於是,他們使用了熱處理而不是用酶來軟化組織,這樣可以使組織膨脹約20倍也不會被破壞。然後,分離的蛋白質就可以在擴張後用熒光標籤進行標記。
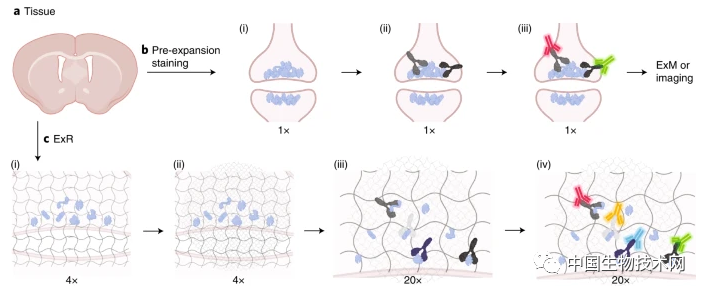
在這項新研究中,該團隊展示了使用共聚焦顯微鏡成像完整腦回路中突觸前鈣通道與突觸後支架蛋白的排列。突觸是密集堆積着蛋白質的神經元之間的連接。
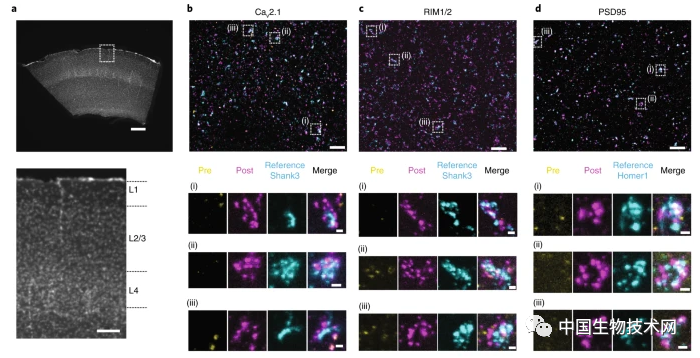
研究人員表示,突觸蛋白與神經退行性疾病密切相關,但此前一直沒有工具可以將其可視化。因此,這項新技術將會進一步發現以前未見的細胞和組織內的納米結構,從而幫助解答許多有關突觸蛋白功能障礙的生物學問題。
他們還從阿爾茨海默症小鼠模型中發現腦組織中含有離子通道蛋白的週期性澱粉樣納米簇。這些都是科學家們以前從未見過的。
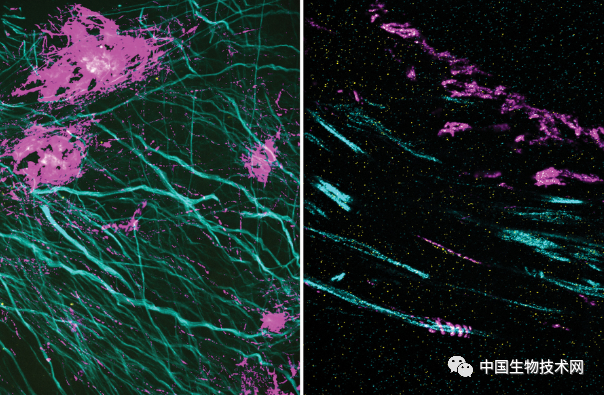
左圖顯示了β澱粉樣蛋白納米簇的線狀結構,右圖顯示了β澱粉樣蛋白的螺旋結構,這是以前的技術無法揭示出的
研究共同通訊作者、MIT的生物工程、大腦和認知科學和神經技術教授Edward Boyden説:“顯然,這個新技術將揭示更多新的生物學發現。如果生物領域研究人員和臨牀醫生一直以常規方式標記並研究大腦或其他生物樣本中的蛋白質,那麼他們會遺漏掉許多現象和可能性。”
目前,該團隊還在對這項技術進行調整,以便他們可以一次成像更多種蛋白質,並最終將其應用於人體組織樣本。
論文鏈接:
https://www.nature.com/articles/s41551-022-00912-3