Cell:斯坦福團隊首次從頭合成微生物組,功能可與天然微生物組媲美_風聞
中国生物技术网-中国生物技术网官方账号-2022-09-19 14:00
腸道微生物組(腸道菌羣)是一個極其複雜的微生態系統。近十幾年來,通過將微生物組移植到無菌小鼠中的實驗不斷在這一領域湧出新的研究成果,證實了這些數以萬億計的小生命對宿主健康具有一系列深遠影響,包括從肥胖、糖尿病、腸道疾病、癌症、神經發育,以及抑鬱症在內的精神類疾病都與它們有關,微生物組甚至還會影響個體對癌症免疫治療的反應。
然而到目前為止,多種宿主表型的微生物組組成,及其與特定疾病相關的確切細胞和分子機制仍然是個謎。
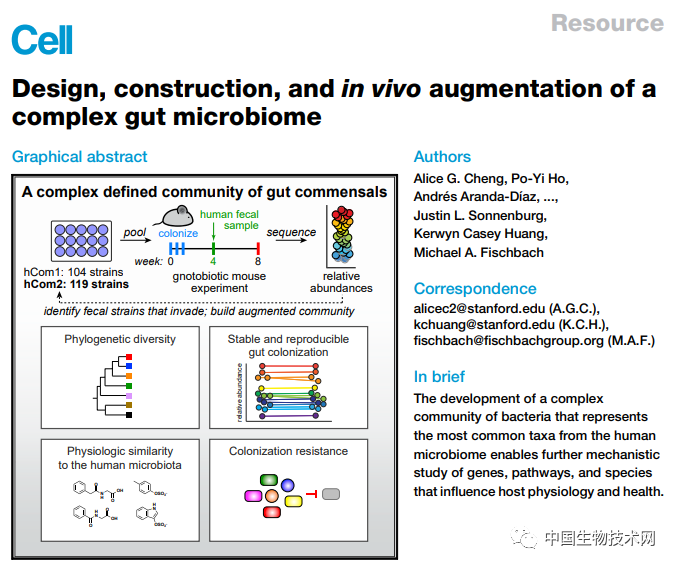
近日,發表在《Cell》上的一項新研究中,來自斯坦福大學微生物組治療計劃(MITI)的研究團隊首次從頭構建了最複雜且定義最明確的合成微生物組,並將其成功移植到小鼠體內,可靠模擬了天然菌羣的功能。這一成果為研究腸道微生物組提供了理想的模型,併為開發基於工程微生物組的治療方法打開了大門。
目前,許多關鍵的微生物組研究都是利用糞菌移植進行的,即將微生物組從一個生物體引入到另一個生物體。雖然科學家通常會在特定細胞甚至整個小鼠中關閉某個基因或敲除某種蛋白質,但在給定的糞便樣本中,還沒有一種工具可以實現在數百種細菌中操縱其中的一種。
在這項新研究中,研究人員提出一個解決方案:通過單獨培養細菌然後與其他細菌混合的方法,從頭合成微生物組。微生物組中的每一個細胞都佔據一個特定的功能生態位,執行分解和構建分子的反應。此外,還必須要確保最終的合成微生物組不僅穩定、保持穩態(不能出現壓倒性菌種),而且還要具有功能性,能夠執行天然微生物組的所有行為。
然而,由於個體間存在的差異,將選擇的細菌菌種加入到“大家庭”中絕非易事,隨機挑選的的兩個個體間共享的微生物基因還不到一半。
為此,研究人員着手設計了一個由人類腸道微生物組中最常見細菌菌種組成的羣落。他們分析了來自人類微生物組計劃(HMP)的宏基因組序列數據,以找到那些幾乎存在於所有個體中的細菌,無論其丰度如何。
他們選擇了大約20%的人類微生物組計劃受試者中存在的細菌菌株,然後在體外構建並表徵了一個由104種細菌組成的特定菌羣,他們稱其為hCom1。
雖然這些細菌菌株可以在培養皿中共存,但真正的考驗是“人工菌羣”能否在腸道中定植。接下來,研究人員將hCom1引入精心設計的無菌小鼠體內。
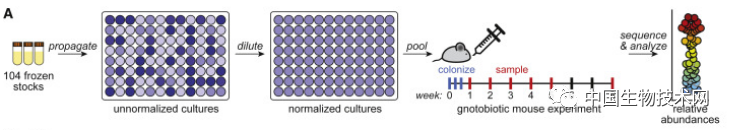
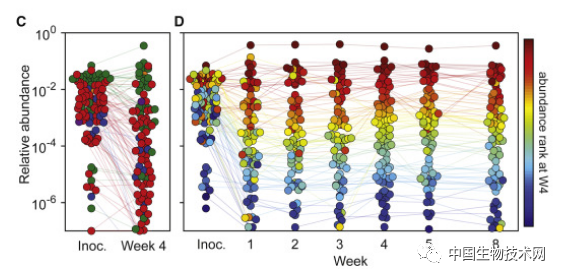
結果令人滿意,98%的菌種定植在無菌小鼠的腸道中,hCom1非常穩定,每個菌羣的相對丰度水平在兩個月內保持不變。
為了使人工菌羣更加完整,並確保所有重要的微生物組功能都能由一種或多種細菌來完成。他們借鑑了“定植抗性”理論——任何被引入現有菌羣的細菌,只有在能填補尚未佔據的生態位時才能存活。
接下來,研究人員將來自人類的糞便微生物組引入到定植hCom1的小鼠中,並跟蹤成功定植的新菌種,試圖建立一個更完整的合成微生物組。
結果顯示,在被糞便樣本挑戰的小鼠中,第8周平均89%的基因組副本來自hCom1,其餘11%代表了從糞便樣本中加入到hCom1的新菌種。儘管有新菌種加入,hCom1的菌羣結構仍然保持不變。因此,hCom1對人類糞便的挑戰具有廣泛但不完全的彈性。
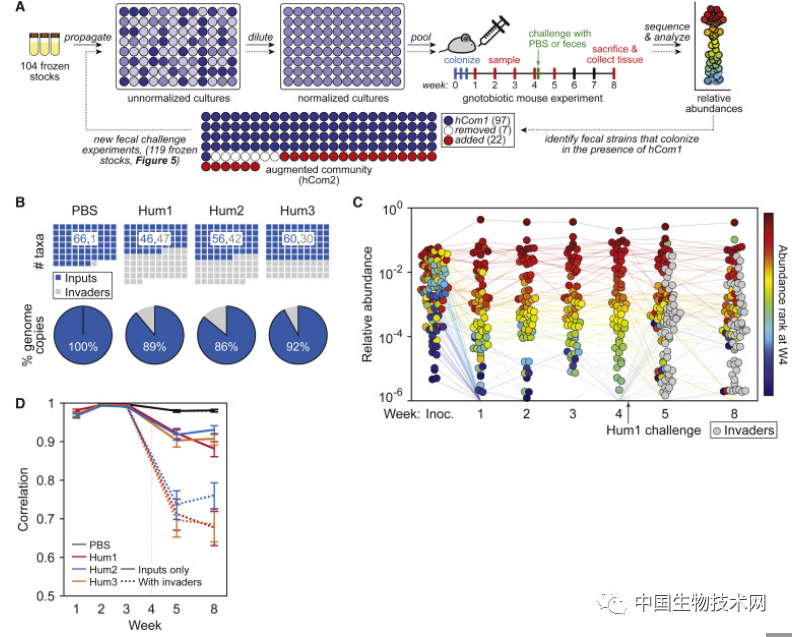
研究人員在三次糞便移植中至少兩次發現了22種新的細菌菌株,主要來自厚壁菌門(Phylum Firmicutes)或另枝菌屬(Alistipes),他們將這些菌株添加到hCom1中,並移除那些未能在小鼠腸道中定植的細菌,然後形成了一個由119種菌株組成的新合成微生物組(hCom2)。第二次迭代仍然是通過單獨培養然後混合的方式。但hCom2比hCom1更類似於糞便微生物組的混合體,並且具有更強的定植抗性。
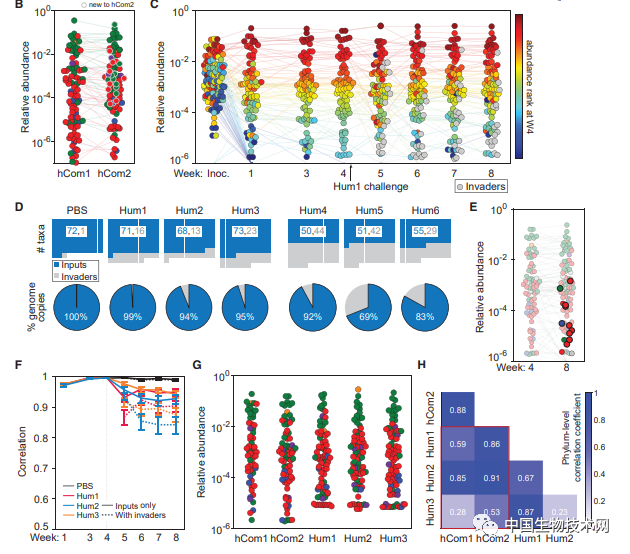
隨後,研究人員在無菌小鼠定殖了hCom2,然後用大腸桿菌感染它們。結果發現,與那些被天然然菌羣定植的小鼠一樣,這些小鼠也能抵抗感染。
總之,hCom2可靠模擬了人源化小鼠的腸道承載能力、免疫細胞譜系和代謝表型。研究人員表示,hCom2可以作為理想的腸道微生物組模型的起點。
研究人員表示,hCom2或其未來版本將使類似的還原論研究成為可能,從而揭示涉及其他領域的細菌製劑,如免疫治療反應。
先前的研究表明,健康的天然微生物組會產生有益的保護作用。在這項研究中,該團隊還通過反覆消除或修改某些菌株來進一步確定哪些菌株具有特別的保護作用,並從中發現了幾種關鍵的細菌。他們計劃將進一步研究,以將這個範圍進一步縮小。
該團隊表示,這種從頭合成微生物組的方法將使基於工程微生物組的療法在未來成為可能。
論文鏈接:
https://dx.doi.org/10.1016/j.cell.2022.08.003