“瘦身版”納米抗體,能庇佑人類走多遠_風聞
返朴-返朴官方账号-关注返朴(ID:fanpu2019),阅读更多!2022-11-18 08:54

撰文 | Hayley Bennett
編譯 | 汪汪
美國藥理學家Aaron LeBeau有個綽號叫“鯊魚小子”。當你聽到這個綽號,大概很難想象這人會是一名致力於研究癌症新療法的科學家。剛剛入職美國威斯康星大學麥迪遜分校(University of Wisconsin–Madison)的頭一年,LeBeau就在與學校達成的協議裏提出,要在他的實驗室裏放一個30立方米的鯊魚鹽水水箱,現在這個水箱已經成為了四條小護士鯊的安居之處。LeBeau喜歡他的綽號,他形容這個暱稱是一個“眾所周知的秘密”,當他第一次見到他的新鄰居時,就被問道:你是那個每天在研究鯊魚的人嗎?
鯊魚小子並不僅僅研究鯊魚。最近,LeBeau又開始研究起了另一種生物:駱駝。在旁人看來,鯊魚和駱駝顯然沒有任何共同之處,但在科學家的眼裏,這兩種風馬牛不相及的生物正被一種在進化過程中的奇特之處聯繫起來,而科學家們正在研究這種奇特之處,試圖利用它解決從新冠病毒到癌症的各種問題。
故事要從上世紀80年代説起,當時,一羣比利時的學者正在研究水牛昏睡症,在測試過程中,他們需要分析水牛的血液樣本。項目中途,一位之前曾在研究組待過的學生提出想用同樣的方法來分析駱駝的血液。項目的負責人,來自布魯塞爾自由大學(Vrije Universiteit Brussel)的 Serge Muyldermans同意了這個請求。學生給研究組送來一些阿拉伯駱駝血液,但研究團隊只取了很少一部分用於測試,剩餘的血液樣本都繼續儲存在冰箱裏。
不久之後,Muyldermans為一些生物學專業的學生設置了課程實踐——對血液樣本中的抗體進行分離。這時,冰箱裏儲存的駱駝血液終於發揮了作用。
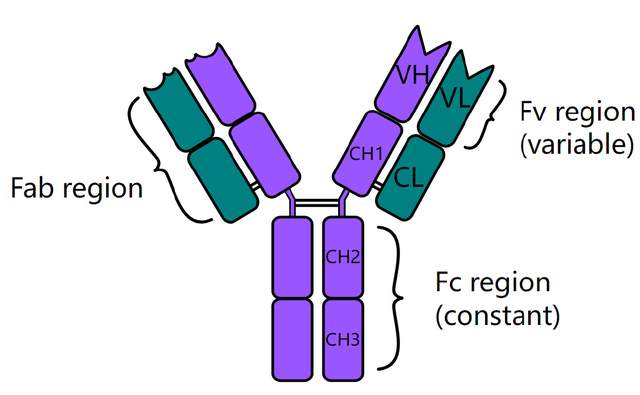
如果我們對免疫學有所瞭解的話,我們會知道,經典抗體分子一般被認為由兩種類型的蛋白質鏈組成:即重鏈(heavy chain, Hc)和輕鏈(light chain, Lc)。兩條重鏈與兩條輕鏈配對形成一個免疫球蛋白分子(immunoglobulin G, IgG)——一種經典的 Y 形抗體(如圖1,紫色為重鏈,綠色為輕鏈)。這個結構是如此的優雅而強大:兩條重鏈構成了 Y 形雙倍厚度的軀幹,在頂部向兩端展開,就像是伸出的雙手;而輕鏈則像裝備在盔甲上的臂板一樣,附着在重鏈伸出的手臂上,和重鏈一起形成“抓手”,即Fab區,可以與抗原相結合。
按照實驗設計,學生們需要首先使用化學還原劑將他們分離得到的 Y 形抗體進行還原拆分,再按分子量對抗體進行分離,就可以得到抗體分子的重鏈和輕鏈。但在對駱駝血液樣本進行實驗時,結果卻並不符合預期。無論學生們如何重複實驗,都只能得到重鏈的分子量,而輕鏈部分卻不知所蹤。這個實驗結果令所有人意外:要麼學生們的操作有錯誤,要麼來自駱駝血液中的抗體不同尋常。
Muyldermans的同事Raymond Hamers(1933-2021)最先反應過來,他認為這可能不是什麼實驗錯誤。也許,駱駝的抗體就是沒有輕鏈?這個猜想讓Muyldermans興奮起來。他在細菌中製造小鼠抗體時,遇到的難題就是細菌無法將重鏈和輕鏈蛋白質正確摺疊並連接在一起。如果駱駝的抗體沒有輕鏈,那這難題不就迎刃而解了嗎?
此後,Muyldermans、Hamers和同事們花了很長時間來證明駱駝的免疫系統確實可以生產這種沒有輕鏈的非典型抗體。1993 年,他們的團隊終於在《自然》雜誌上報導了這一驚人發現。事實證明,在駱駝和美洲駝這樣的動物體內,既存在傳統抗體,也存在這些無輕鏈抗體。後者被稱呼為 “納米抗體”:它們沒有臂板,由重鏈延伸出去的手臂也更為精小,這種結構使得分子更加緊湊,與傳統抗體分子量一般在150kDa左右的大小相比,“納米抗體” 的大小僅僅只有75kDa 。

我們可以用音樂播放列表來打個比方:經典抗體的免疫曲目類似於由兩個音樂合集編制的播放列表,每個音樂合集包含數千首曲目,組合可以千變萬化;而納米抗體則僅由一個合集創建。讓科學家們大開眼界的是,儘管納米抗體的多樣性比傳統抗體要少,但依然可以產生良好的免疫反應。
從進化學的角度來看,這個現象至今仍然無法解釋。為什麼會出現僅有一種鏈的抗體?它又是如何出現的?
美國加州州立大學(California State University)弗雷斯諾分校的結構生物學家Cory Brooks在 2018 年的一篇論文中提出了他的猜想。他認為這是一次在進化過程中發生的巧合:重鏈與輕鏈相互作用的部分發生了變化,使得兩種蛋白質鏈分開。那這種進化巧合是否為駱駝帶來了好處呢?根據Brooks的説法,這類納米抗體似乎比普通抗體“更擅長中和病毒”:在駱駝體內有很高的病毒載量,而這些病毒並沒有對駱駝產生影響。但如果其他反芻動物感染了同樣的病毒,就會出現各種症狀。科學家們猜測,也許在駱駝進化的漫長曆史中,出現過一些致命病毒,而這些較小的抗體有助於抵抗這些病毒,從而被保留了下來。
無獨有偶,這種神秘的抗體不僅僅出現在駝類生物中,也出現在鯊魚體內。1995年,美國邁阿密大學的 Andrew Greenberg 及其同事在論文中揭示,鯊魚使用一種單鏈抗體,稱為“新型免疫球蛋白抗原受體”(immunoglobulin new antigen receptors ,IgNARs)。這類新型抗體常在鯊魚、鰩魚和其他軟骨魚類中出現,比駱駝的無輕鏈抗體更小、更穩定。
這不會是單純的偶然,新型抗體一定有獨到之處,才能在進化過程中被保留下來。Brooks的工作表明,分子量更小的抗體相較於傳統抗體來説更加穩定,在惡劣的環境中也能為機體提供保護。比如説,駱駝的體温很高,而鯊魚及其親近魚類為了平衡海水中的高鹽濃度,在體內保留了較高濃度的尿素——這兩種情況下,新型抗體都能提供更好的穩定性和更高的保護效力。
現在回到鯊魚小子LeBeau。過去,他研究的正是駱駝抗體,利用這種抗體的特性來尋找癌症靶標,研究抗癌療法和腫瘤成像技術。這些研究持續了好幾年,也得到了不錯的成果,因此他的團隊希望接下來可以試試鯊魚的抗體版本。很可惜,LeBeau不確定自己要如何弄到鯊魚血液,因為他們的實驗室位於美國中部,這裏的鯊魚數量為零。無奈之下,他們求助於當地的一家水族館,水族館很樂意提供幫助,但每條鯊魚300公斤的體重使他們望而卻步。看來,養鯊魚還不如養駱駝靠譜。
法國製藥公司賽諾菲(Sanofi)正是這麼幹的。它們建設了一個駱駝牧場,再利用駱駝血液中的特殊抗體發展新的療法。賽諾菲大獲成功:其中一個基於納米抗體的療法已經開始進入市場。2018年,賽諾菲還以 39 億歐元(34 億英鎊)的價格收購了初創公司 Ablynx,這是一家專注於研發納米抗體療法的新公司。他們的研發的一般步驟是:用目標病原體感染駱駝,使駱駝產生免疫,等待 6-12 周後抽出駱駝血,再使用相同的病原體來對血中的抗體進行篩選,從而得到最佳抗體。
這種策略並不是賽諾菲獨有的秘訣。實際上,它已經被很廣泛地使用,業內人員形象地稱之為“淘金”。在尋找能結合乳腺癌靶點的駱駝抗體時,研究人員使用的就是這種策略。利用駱駝和鯊魚活體篩選抗體,是因為人們認為使用活體動物可以減少篩選出最佳抗體的時間——動物的免疫系統在遇到目標分子之後,會做一些額外的分子工作,來優化它們的結合結構。但每種方法都有挑戰,照顧一個滿是駱駝的農場並不是一個簡單的選擇。
賽諾菲近些年來針對納米抗體的研發做出了非常多的成果。2018年,由其研發的針對罕見血液疾病的納米抗體 caplacizumab 在歐盟獲批上市,並於次年獲得美國FDA批准。賽諾菲還在針對其他靶點開發療法,例如類風濕性關節炎和紅斑狼瘡等一些自身免疫疾病。另一種由Ablynx和賽諾菲聯合研發的藥物ozoralizumab在日本開展了針對類風濕性關節炎的臨牀試驗,並於今年6月宣佈了臨牀二/三期試驗的積極結果。
納米抗體具有靈活的小身材和更加穩定的性質,而且可以格式化加以設計,這些獨特的優勢令它們備受科學家們的青睞。正如Muyldermans所期待的那樣,當不再需要傳統抗體的輕鏈結構以後,生產過程中遇到的難題迎刃而解,這些納米抗體可以在細菌、酵母或哺乳動物細胞中大規模克隆和生產。
不過,提高產能僅僅是優勢之一。納米抗體還有一個絕對的優勢——它們可以到達傳統抗體無法到達的目標分子部分。這是一個非常大的突破,這意味着在傳統抗體之外,我們可以使用納米抗體來尋找其他疾病靶標。顯然,更小的體積使它們可以適應更小的間隙;不過,除了體積,獨特的結構也功不可沒:在傳統抗體伸出的Y型手臂末端有手指狀突起,作用是與分子靶標接觸,但在納米抗體中,這種抓手並不對稱,其中一邊突起比傳統抗體更長,科學家們認為這使它們能夠進一步進入目標分子表面的縫隙中,從而觸及一些從未到達過的隱藏結合區域。
加州州立大學的Cory Brooks是一名結構生物學家,主要工作是使用晶體學來研究抗體與靶標結合過程中所涉及的分子結構。他的研究結果可以為納米抗體的獨到之處提供證明:當目標是病毒時(如HIV 和SARS-Cov-2),比較常規抗體和納米抗體與相同靶標的結合情況,可見納米抗體確實能與目標分子的隱藏部位接觸。在Brooks看來,納米抗體在治療 Covid-19 等傳染病、甚至在所有疾病領域都具有很大潛力。病毒所致的傳染病可能是使用納米抗體治療的最佳靶標之一,特別是考慮到納米抗體在駱駝科動物進化中可能扮演着“病毒中和劑”的角色。
怎樣才能獲得抗體?也許對一個大公司(比如賽諾菲)來説,建立一個駱駝農場的主意不錯。但對於Lebeau這麼一個一直把“免疫學無聊”掛在嘴邊的人來説,鯊魚是一種更有趣的選擇。在新冠大流行暴發前不久,他已經在與蘇格蘭Elasmogen 公司的首席執行官 Caroline Barelle 接洽,該公司一直致力於收集鯊魚的血液樣本,以建立一個包含數十億鯊魚抗體的合成庫,並正在尋找學術合作者,基於這個巨大合成庫來研究癌症治療。
兩人第一次聊天后,LeBeau 就立即開始尋找鯊魚缸;疫情出現後,他們一拍即合,開始了 Covid-19 中和抗體的研究。在檢索了Elasmogen公司的合成文庫後,他們發現了一些 Covid-19 刺突蛋白的結合劑,然後在明尼蘇達州進行晶體學分析,探索它們的精細結合模式。正如 LeBeau 回憶的那樣,這些基於結構的工作顯示了微小的鯊魚抗體正在做“瘋狂的分子瑜伽”,以進入即使是美洲駝抗體也無法到達的刺突蛋白區域。在針對活病毒的測試中,他們的研究表明,這些來自鯊魚的抗體在中和病毒方面可以與人類抗體的效果一樣好,並且優於駱駝抗體。
隨着病毒的迅速發展,抗體研究很重要的方向之一是考察抗體對病毒變異株的抵抗力。在後續研究中,他們發現這些鯊魚抗體對 Omicron 這類更具傳染性的新冠病毒變異株非常有效!Omicron在去年11 月首現南非,它的刺突蛋白中包含至少30處突變。分子建模表明,即使刺突蛋白突變程度達95%,他們所研發的一種鯊魚抗體仍然可以發揮作用。
與人類體內笨重的 Covid-19 抗體相比,這些小身材的納米抗體似乎具有優勢。人類抗體直接識別病毒與人類細胞接觸的刺突蛋白區域,該區域始終處於適應和變異的壓力之下。而鯊魚抗體會深入刺突蛋白的更下方,進入 LeBeau 認為“從不變異”的區域——如果確實如此,那麼這個區域就是高度保守的,這種保守性甚至可以追溯到2003年引起非典的SARS病毒。不僅如此,這個區域的保守性還可以延伸到其他來自野生動物的冠狀病毒,也就是説,如果有朝一日那些不同於新冠病毒的其他病毒再次蔓延到人類身上,這類納米抗體仍然可以發揮作用。目前他們正在對動物進行實驗以驗證這個猜想,希望在人類遭遇下一次疫情之前,他們已經做好充足的準備。
在這些驚人的進展發生之時,鯊魚小子LeBeau仍在盯着鯊魚缸。作為一名癌症研究人員,LeBeau似乎更加迷戀鯊魚以及它們身上的奇妙抗體。用他的話説,“這些抗體看起來只是一些精巧的奇妙的蛋白質,但背後藴藏的潛力卻似乎無窮無盡。”2021年他來到威斯康星州,現在他正用癌症靶標對活鯊魚進行免疫接種。他的同事們正在研究冠狀病毒,而 Elasmogen 公司正在利用納米抗體尋找針對關節炎和炎症性腸病的靶標。從治療出血熱到研發疫苗,這張由納米抗體繪製成的宏偉畫卷,正徐徐對我們展開。
編譯來源
https://www.chemistryworld.com/features/the-incredible-antibodies-of-sharks-llamas-and-camels/4015629.article?adredir=1
特 別 提 示
1. 進入『返樸』微信公眾號底部菜單“精品專欄“,可查閲不同主題系列科普文章。
2. 『返樸』提供按月檢索文章功能。關注公眾號,回覆四位數組成的年份+月份,如“1903”,可獲取2019年3月的文章索引,以此類推。
版權説明:歡迎個人轉發,任何形式的媒體或機構未經授權,不得轉載和摘編。轉載授權請在「返樸」微信公眾號內聯繫後台。