PNAS:突破血腦屏障,靶向致病RNA,治療漸凍症和痴呆_風聞
葆力医学观察-专注生物科研领域,趣味科普与行业干货齐飞2022-11-25 09:22
肌萎縮側索硬化(ALS),又稱漸凍症,是世界衞生組織(WHO)認定的五大絕症之一,是一種累及上/下運動神經元及其支配的軀幹、四肢和頭面部肌肉的慢性、進行性變性疾病,患者會逐漸失去控制肌肉的神經元,導致肌肉萎縮,最終死亡。
C9orf72基因突變是遺傳性漸凍症的主要原因,C9orf72基因中六核苷酸重複序列(GGGGCC,G4C2)異常擴增,重複65次到數萬次,這種異常擴增,既影響了C9orf72基因的正常表達,還會產生一種名為二肽重複蛋白(Dipeptide Repat Proteins,DRP)的神經毒蛋白。
C9orf72基因這種異常擴增突變,除了會導致漸凍症,還是額顳葉痴呆的重要致病因素,約佔額顳葉痴呆的25%,額顳葉痴呆會導致大腦額葉和顳葉萎縮,引起性格、行為和語言的改變,最終導致死亡。
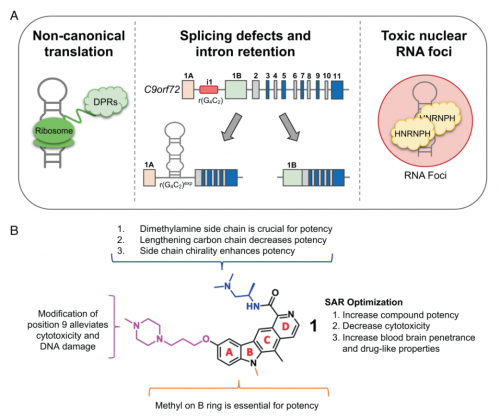
2022年11月21日,斯克里普斯研究所的研究人員在 PNAS 發表了題為:A blood–brain penetrant RNA-targeted small molecule triggers elimination of r(G4C2)exp in c9ALS/FTD via the nuclear RNA exosome 的研究論文。該研究發現了一種候選小分子藥物,能夠突破血腦屏障,選擇性消除導致漸凍症和額顳葉痴呆的C9orf72基因的G4C2異常擴增的RNA片段,並恢復漸凍症神經元和小鼠模型的健康。

論文通訊作者 Matthew Disney 教授表示,這種化合物通過結合並利用細胞的自然過程來消除致病RNA(G4C2異常擴增引起的內含子保留),讓這些被釋放的內含子RNA通過外泌體被作為廢物清理掉。可以想象,這種方法還可以用於其他目前無藥可醫的因為毒性RNA作用的神經系統疾病。

論文第一作者Jessica Bush(左),通訊作者Matthew Disney(右)研究的首先從斯克里普斯研究所的包含11000個類藥性分子中進行篩選,首先確定了69種可抑制毒性C9orf72突變翻譯的化合物。然後,研究團隊進一步細化了這些化合物,根據分子大小、結構等因素提出了那些無法通過血腦屏障的化合物,進一步篩選到了16種候選化合物,其中一種化合物(化合物1)最具潛力,被用來進一步研究。研究團隊對來自約翰·霍普金斯大學醫學院神經退行性研究實驗室的由漸凍症患者捐獻的皮膚細胞樣本進行測試,他們將這些患者的皮膚細胞誘導為幹細胞,再使其分化為神經元。對4名漸凍症患者來源的皮膚細胞誘導的神經元進行測試,化合物1都能使漸凍症標誌物劑量依賴性降低,且沒有脱靶效應。
研究團隊還在攜帶C9orf72基因突變的漸凍症小鼠模型身上測試了這種化合物,這種小鼠模型顯示出典型的漸凍症行為和血液學標誌。治療後兩週,漸凍症小鼠模型的疾病標誌物顯著減少,健康狀況得到改善。Matthew Disney 教授表示,迄今為止的證據表明,這種方法代表着RNA藥物發現領域的一個顯著進步。這項研究首次證明,你可以開發穿越血腦屏障的分子,消除毒性的基因產物,並在漸凍症中證明了這一點。這可以成為治療包括漸凍症、額顳葉痴呆、亨廷頓舞蹈症、肌肉萎縮症等神經系統疾病的通用方法。論文鏈接:https://www.pnas.org/doi/10.1073/pnas.2210532119