5家中國藥企免費獲得默沙東新冠口服藥仿製授權

據日內瓦藥品專利池(MPP)網站20日消息,該組織已與27家仿製藥公司簽署協議,授權其生產默沙東口服新冠藥莫努匹韋(molnupiravir)。其中包括5家中國企業:復星醫藥、朗華製藥、龍澤製藥、博瑞醫藥、迪賽諾醫藥。
根據MPP此前與默沙東的協議,包括中國企業在內的27家仿製藥公司無需支付專利費用。

藥品專利池網站截圖
綜合公開資料,莫努匹韋由默沙東和Ridgeback聯合開發,它是全球首款獲批的口服抗新冠病毒藥物。莫努匹韋3期臨牀試驗的研究結果顯示,早期治療服用莫努匹韋,可顯著降低未接種疫苗的新冠肺炎高危成年患者的住院或死亡風險。
2021年11月,莫努匹韋獲得英國藥品和健康產品管理局(MHRA)附條件批准上市。隨後獲得美國食品藥品監督管理局(FDA)緊急使用授權,以及日本厚生勞動省緊急特例批准。
綜合Harvard T.H. Chan公共衞生學院2021年10月的信息等公開資料,莫努匹韋1個療程的藥物,其生產成本約為17美元左右,正常售價可高達700美元,藥價是成本價的40多倍。
在獲批前,默沙東與聯合國支持下的公共衞生組織MPP簽署了莫努匹韋的許可協議。MMP通過默沙東授予的許可,可向製造商授予“MPP分許可”,用以增加莫努匹韋的生產基地,提高藥物的供應數量和覆蓋範圍,供應105箇中低收入國家(LMIC)。

2021年進博會上的默沙東展台 圖源澎湃新聞
據路透社20日消息,參與談判的MPP官員對其透露,預計在較貧窮國家,莫努匹韋為期5天共40粒(每日服用兩次,每次4 粒)的單療程花費約20美元。不過,想要交付莫努匹韋,還需獲得各國監管部門的進一步批准。
莫努匹韋的效果依然受到質疑。路透社提到,雖然莫努匹韋在印度獲得緊急授權,可以上市銷售。“但由於存在安全風險,目前不建議使用。”

路透社報道截圖
MMP本月20日新聞稿表示,根據協議,只要新冠肺炎仍被世界衞生組織列為國際關注的公共衞生突發事件,默沙東及其合作伙伴Ridgeback Biotherapeutics,以及發明該藥物的美國埃默裏大學都不會從“MPP分許可”持有人的莫努匹韋銷售中收取特許權使用費。
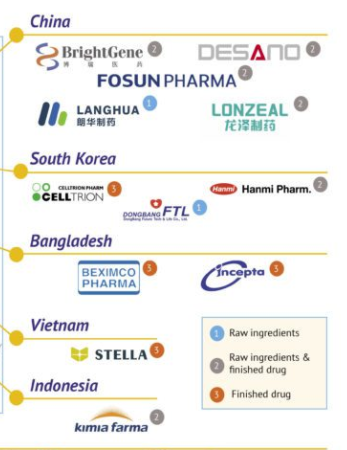
MMP稱,經機構獨立評審,本次獲得許可的企業證明了他們有能力滿足藥品專利池組織對產能和監管合規的要求,能夠生產符合國際質量標準的藥品。全球共有13家獲許可同時生產莫努匹韋原料藥和成品藥,另有5家藥企獲授權生產原料藥,9家藥企獲授權生產成品藥。
其中,來自中國的復星醫藥、博瑞醫藥、(石家莊)龍澤製藥與(上海)迪賽諾獲許可同時生產莫努匹韋的原料藥和成品藥,維亞生物旗下的朗華製藥則獲許生產莫努匹韋的原料藥。
藥品專利池網站截圖
莫努匹韋不是世界上唯一的口服新冠藥物。
由中國科學院上海藥物研究所、中國科學院武漢病毒研究所、中國科學院新疆理化技術研究所、中國科學院中亞藥物研發中心等共同研發的VV116,與獲批上市的默沙東莫努匹韋和輝瑞帕昔洛韋同屬新冠治療小分子藥物。
VV116已經在國內獲批進入臨牀試驗。此外,當地時間2021年12月30日,VV116在烏茲別克斯坦獲得緊急使用授權。據澎湃新聞消息,在年內通過臨牀試驗後,VV116將第一時間啓動上市(NDA)申請。

本文系觀察者網獨家稿件,未經授權,不得轉載。