全球使用最廣的流腦疫苗,納入新版專家共識_風聞
疫苗与科学-疫苗与科学官方账号-03-07 15:34
陶醫生早就預言過,隨着國產流腦4價結合疫苗(康希諾公司的曼海欣)於2021年底上市,中國流腦疫苗專家共識一定會因此而更新。
説曹操,曹操到。2023版中國流腦疫苗專家共識於2月網絡首發,上一版本為2019版。
 2023版的正文篇幅是9頁,參考文獻116篇;2019版正文篇幅4頁,參考文獻49篇。新版擴容了一倍多,主要擴展內容為流腦的流行病學和疫苗研發進展。
2023版的正文篇幅是9頁,參考文獻116篇;2019版正文篇幅4頁,參考文獻49篇。新版擴容了一倍多,主要擴展內容為流腦的流行病學和疫苗研發進展。
在最重要的【流腦疫苗接種專家共識】一節中,2019版分不同類型的流腦疫苗進行建議,顯得凌亂。2023版則根據免費流腦疫苗的接種程序,分為<2歲和≥2歲這兩個年齡段分別給予建議,條理感更清晰。
然而,新舊共識的接種建議實質沒有區別,一句話就是:自費流腦疫苗可以替代免費流腦疫苗。
新版共識裏,可以用於替代免費流腦疫苗的自費流腦疫苗,由舊版的三種——AC結合疫苗、4價多糖疫苗和AC結合-Hib疫苗,擴大為四種,即新增了4價結合疫苗。
由此,流腦4價結合疫苗正式登上中國流腦預防的舞台。在此之前,中國的流腦預防水平與國際主流水平之間相差了兩個台階,曼海欣讓中國踏上了其中一個台階,另一個台階是流腦B羣疫苗(陶醫生預計,中國踏上這個台階至少還需要5年,甚至是10年)。
 國外有接種流腦B羣疫苗
國外有接種流腦B羣疫苗
2021年12月,國產首款流腦4價結合疫苗——曼海欣,獲批上市。
曼海欣的Ⅲ期臨牀試驗,完全按國家要求採用隨機、盲法、同類疫苗對照設計的原則,即在同一個臨牀試驗方案設計下、同一個研究現場、同一時間內,同一實驗室檢測條件下,由統一的研究者進行臨牀試驗的實施,在科學的前提下進行實驗疫苗與對照疫苗的比較。
曼海欣的Ⅲ期臨牀試驗選取國內已上市的各種工藝流腦疫苗進行對照,<2歲與A羣多糖疫苗和AC結合疫苗,≥2歲與4價多糖疫苗在同等條件下進行頭對頭PK。
曼海欣Ⅲ期臨牀研究結果顯示:
在安全性方面,曼海欣的總體不良反應發生率試驗組低於對照組,各年齡組均未發生4級不良反應,相比於同類疫苗有更好的安全性,耐受性良好。
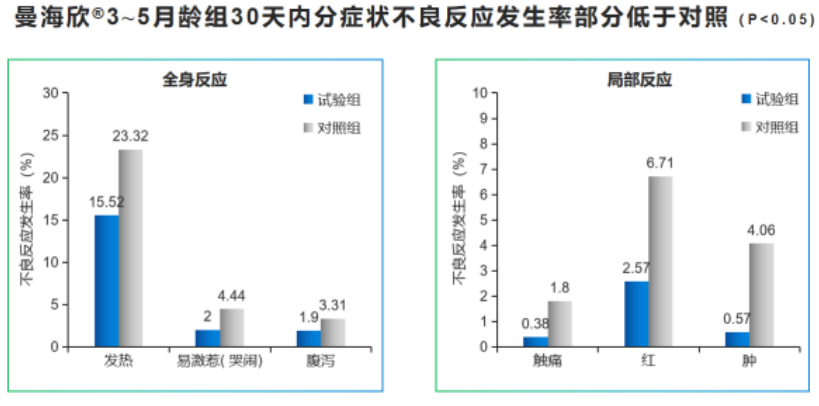
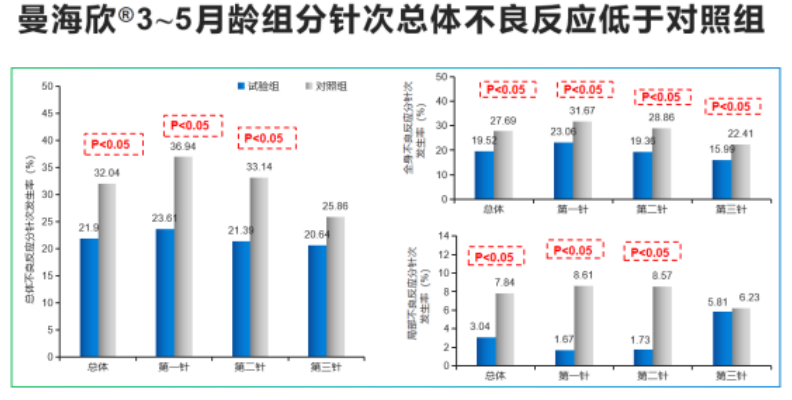
尤其3~5月齡與AC結合疫苗進行對照,其中全身反應發熱、哭鬧及腹瀉,局部不良反應發生觸痛、紅、腫等症狀發生率均低於對照組,並且分劑次不良反應發生率均低於對照組,安全性顯著性優於對照疫苗,其餘組與對照疫苗安全性結果相當,無統計學差異。
3~5月齡,對照為AC結合疫苗,總體不良反應發生率為曼海欣21.9% Vs 對照32.0%(P<0.05,曼海欣優於對照疫苗);
6~23月齡,對照分別為AC結合和A羣多糖疫苗,總體不良反應發生率分別為曼海欣21.5% Vs 對照25.1%,曼海欣20.4% Vs 對照20.1%(無統計學差異,安全性無差異);
2~3歲,對照為4價多糖疫苗,總體不良反應發生率為曼海欣22.6% Vs 對照22.5%(無統計學差異,安全性無差異)。
 在免疫效果方面,曼海欣各年齡組都顯示出良好的免疫效果,是國內唯一可以用於<2歲人羣的流腦4價疫苗。
在免疫效果方面,曼海欣各年齡組都顯示出良好的免疫效果,是國內唯一可以用於<2歲人羣的流腦4價疫苗。
在≥2歲人羣中用4價多糖疫苗做對照的臨牀研究中,曼海欣也顯示出了出色的免疫效果,填補了國內流腦疫苗市場的空白。
國內上市的4價多糖疫苗僅用於≥2歲人羣,在曼海欣Ⅲ期臨牀試驗中只能安排2~3歲(47月齡)組與4價多糖疫苗進行對照,其餘年齡組與AC結合疫苗進行對照。
在2~3歲人羣與4價多糖疫苗的頭對頭比較中,曼海欣除了顯示出良好的安全性,免疫效果優勢尤為突出,在抗體陽轉率、抗體幾何滴度及高抗體(>1:128)比例這三項主要評價指標上均表現優異。
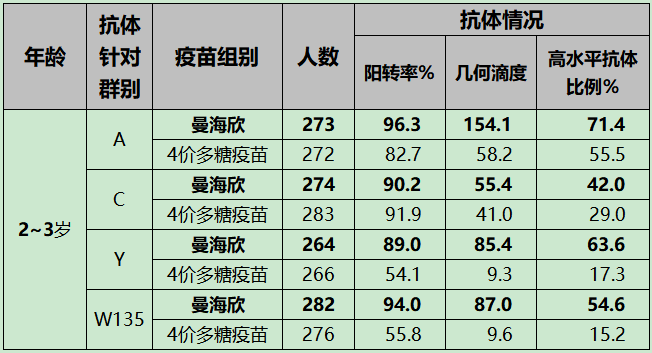 由上表可以看出,接種曼海欣後,兒童針對4個羣別腦膜炎球菌產生的抗體,在陽性率、幾何滴度和高水平抗體比例上均明顯高於對照疫苗,尤其是Y羣和W135羣。
由上表可以看出,接種曼海欣後,兒童針對4個羣別腦膜炎球菌產生的抗體,在陽性率、幾何滴度和高水平抗體比例上均明顯高於對照疫苗,尤其是Y羣和W135羣。
根據2023版專家共識,因流腦結合疫苗具有更好的免疫效果、免疫持久性和免疫記憶,在全球76個將流腦疫苗納入國家免疫規劃的國家中 ,有68個將結合疫苗納入國家免疫規劃,流腦結合疫苗才是全球防控流腦使用最廣泛的疫苗。
流腦4價結合疫苗更因其更廣的菌羣覆蓋,在全球40個國家被納入國家免疫規劃,同時還有更多的國家受種者能夠自費選擇(包括我國),為孩子提供更全面持久的保護。