GSTP1介導的Pik3r1的S-谷胱甘肽化調控破骨細胞形成_風聞
源井生物-让基因编辑更简单!04-11 10:28
骨質疏鬆症是一種與年齡有關的代謝疾病,與骨密度有直接關係,GSTP1是一種谷胱甘肽S-轉移酶P1,其在多種疾病中的治療潛力已被發現。該研究通過孟德爾隨機化遺傳關聯及單細胞測序分析發現GSTP1可能與骨密度存在一定的關聯性。通過氧化還原質譜、免疫共沉澱、非變性非還原免疫印跡、流式細胞術、質譜分析、CRISPR-CAS9基因編輯等關鍵實驗探究GSTP1對骨密度影響的具體機制,發現GSTP1可以通過Pik3r1的Cys498和Cys670上調S-谷胱甘肽化水平,從而抑制其磷酸化,進而通過Pik3r1-AKT-mTOR軸調控自噬通量的變化,影響體外破骨細胞的分化,最後在體外調控破骨細胞的形成。
浙江大學附屬醫院骨科研究中心嚴世貴課題組在氧化還原領域權威期刊,中科院一區TOP雜誌《REDOX BIOLOGY》上發表了題為“GSTP1-mediated S-glutathionylation of Pik3r1 is a redox hub that inhibits osteoclastogenesis through regulating autophagic flux”(IF2022:10.787)。

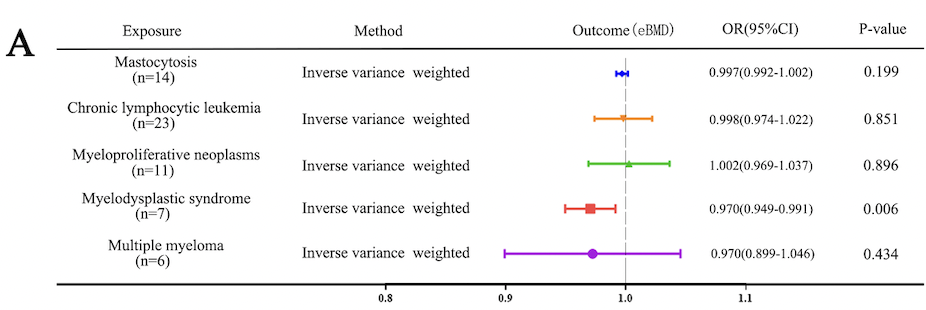
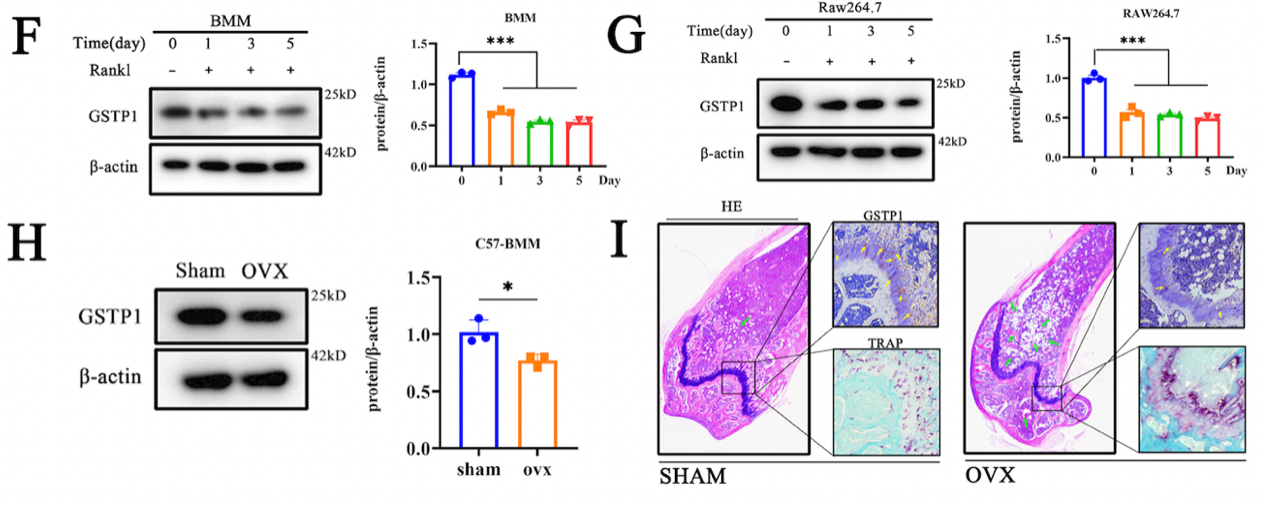
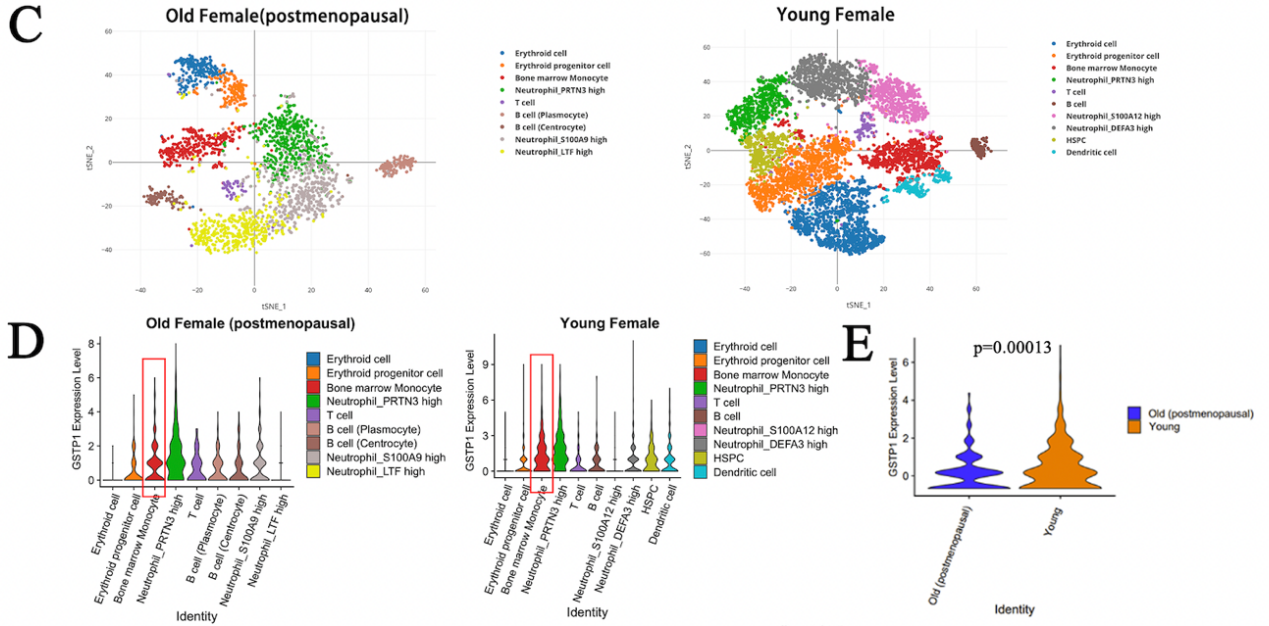
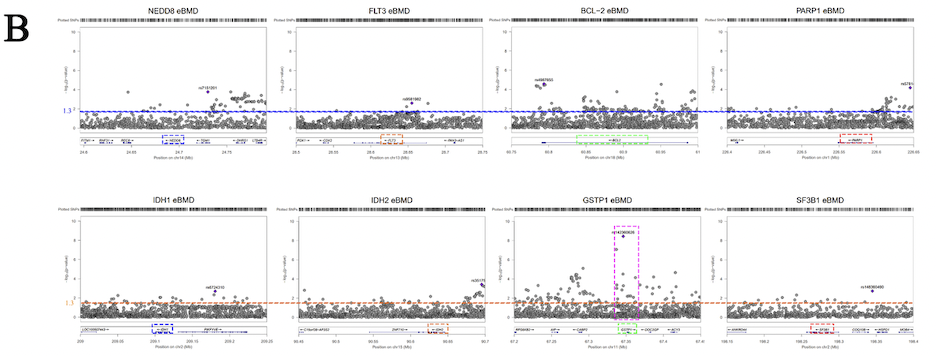
該研究首先通過孟德爾隨機化分析以證明 MDS與骨礦物質密度(BMD)之間存在的的潛在因果聯繫。總結了已經報道的MDS信號轉導蛋白和可能作用的靶位,發現GSTP1可能影響BMD,利用RT-qPCR檢測成骨細胞特異性基因RUNX2的表達量、敲低或過表達GSTP1發現GSTP1與成骨細胞分化關係不大,結合骨髓單細胞分析和Western Blot發現GSTP1在骨髓單核細胞中高度表達,且在老年女性和年輕女性中出現差異,發現GSTP1對BMD的影響更可能通過破骨細胞發生。
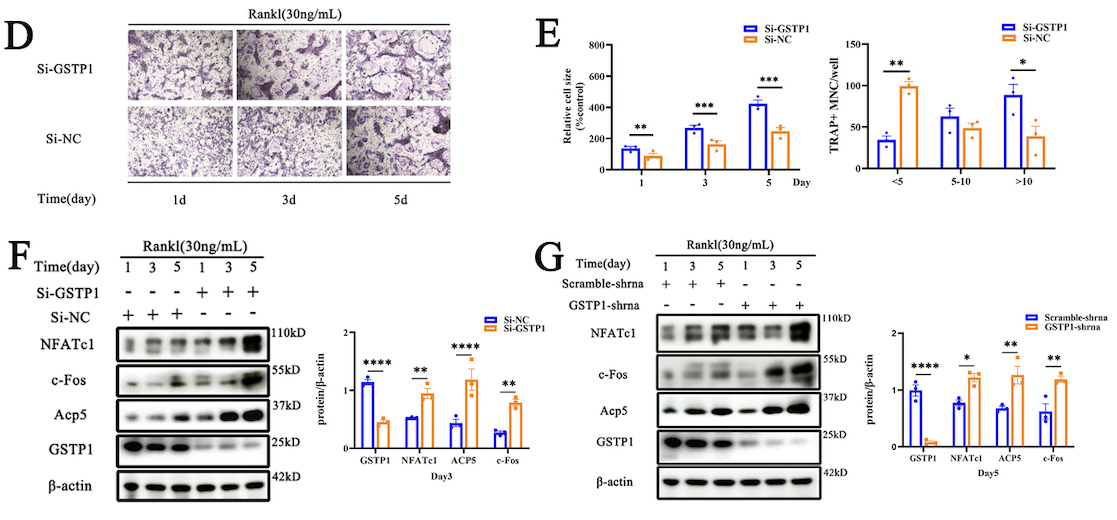
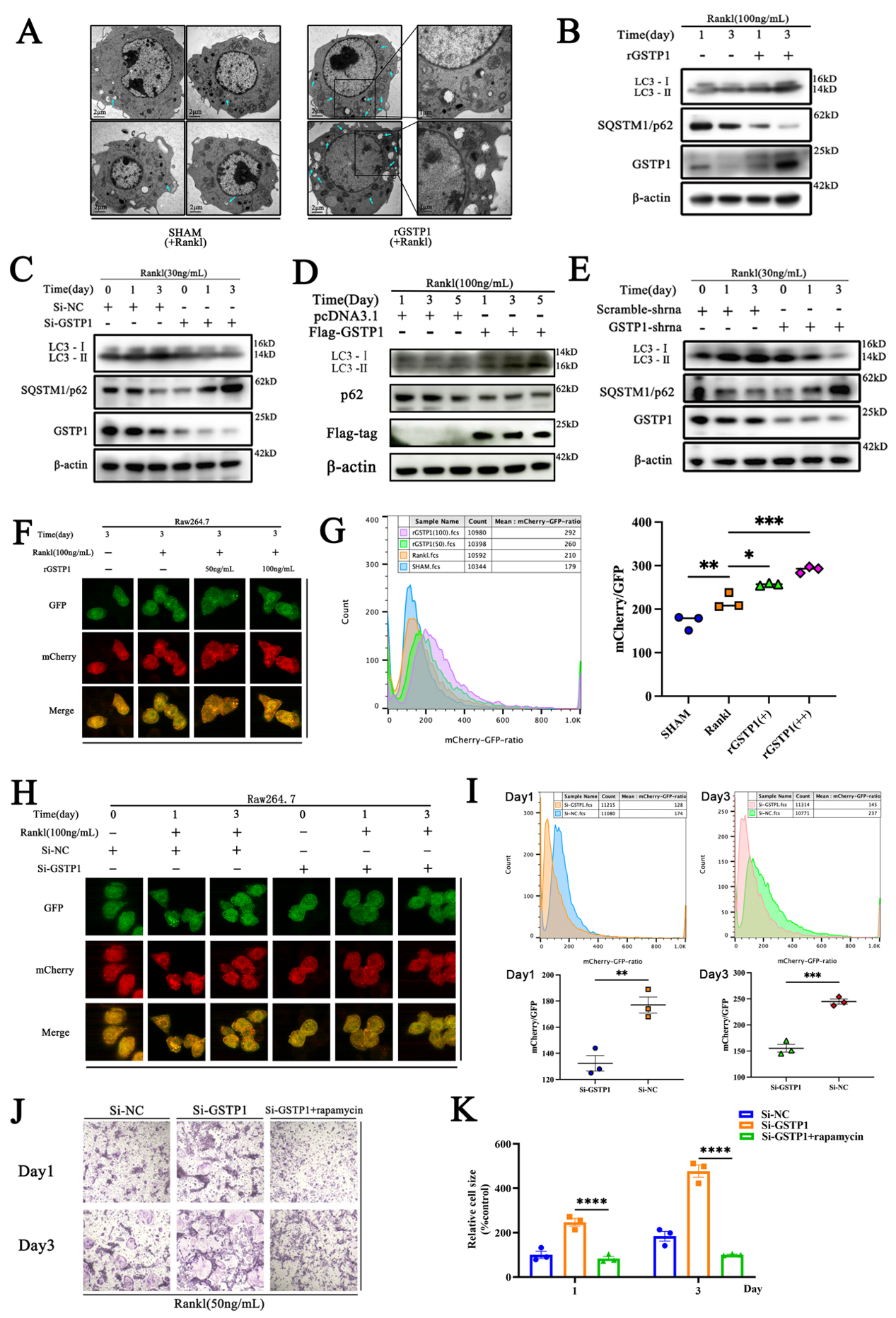
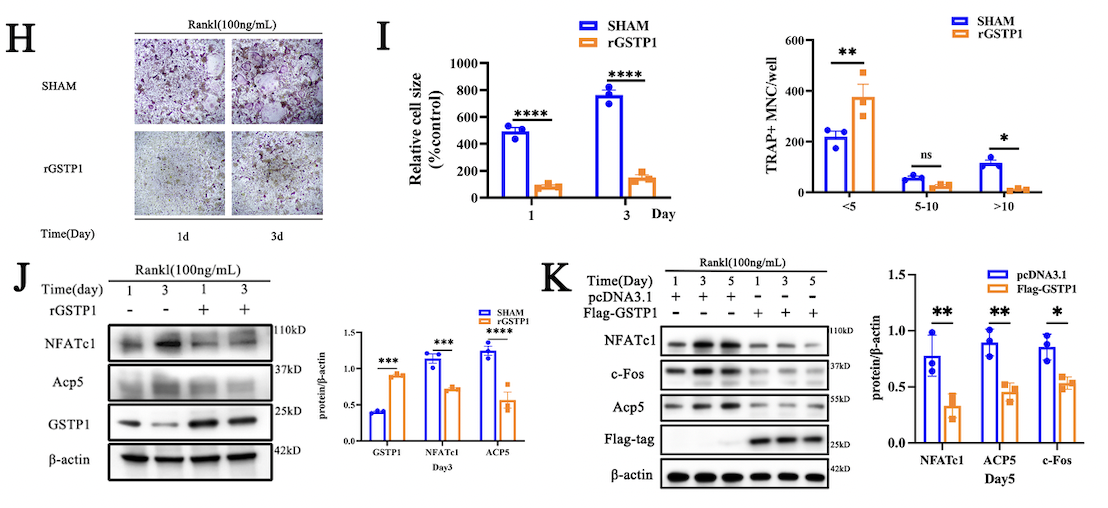
自噬對破骨細胞分化有廣泛的影響,本文從自噬角度繼續探究GSTP1如何影響破骨細胞。細胞經rGSTP1刺激後出現了更多的自噬囊泡和吞噬囊泡,選擇哺乳動物自噬蛋白LC3的作為自噬通量標記物,作者通過比率流式法和自噬雙標慢病毒檢測過表達或敲低GSTP1時不同細胞系在破骨細胞形成過程中的自噬通量改變。而自噬激活劑雷帕黴素通過激活自噬通量逆轉了低水平GSTP1促進的破骨細胞形成。上述結果證明GSTP1可以通過調節破骨細胞分化過程中的自噬通量來調節破骨細胞的發生。
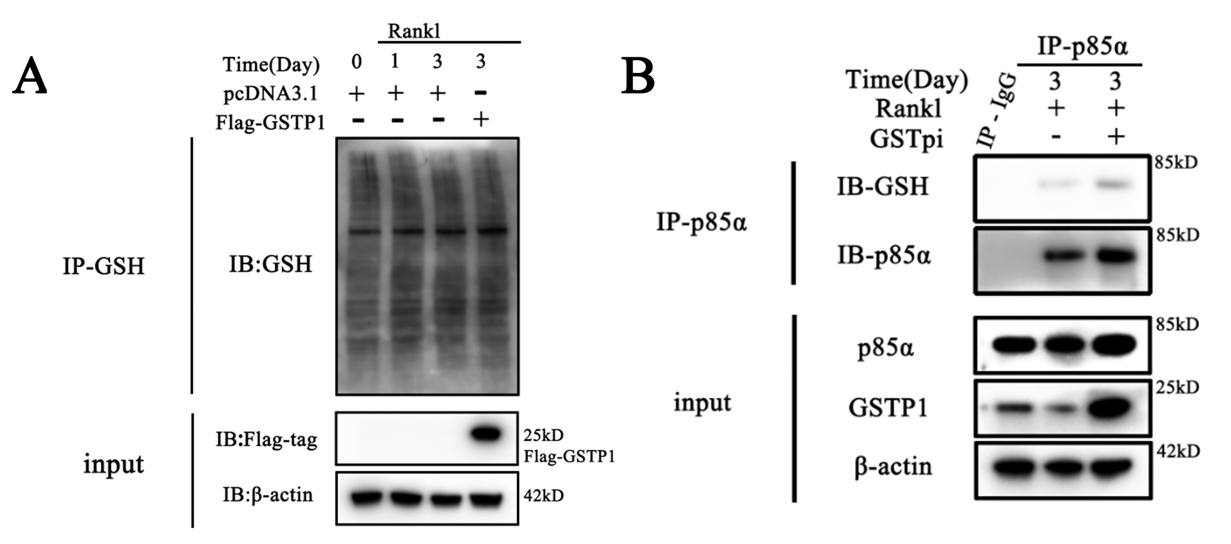
雷帕黴素以mTOR為靶點,mTOR參與哺乳動物自噬主要通過ERK或PI3K-AKT通路激活,為了確定GSTP1在破骨細胞分化過程中對自噬的調控是否通過mTOR完成,刺激下分化 5天BMMs,在磷酸化水平上與對照組沒有差異,利用敲低和轉染,探究GSTP1和磷酸化 Pik3r1、AKT水平之間的關係,結果表明GSTP1調控的自噬通量是通過Pik3r1-AKT-mTOR信號級聯來完成的。
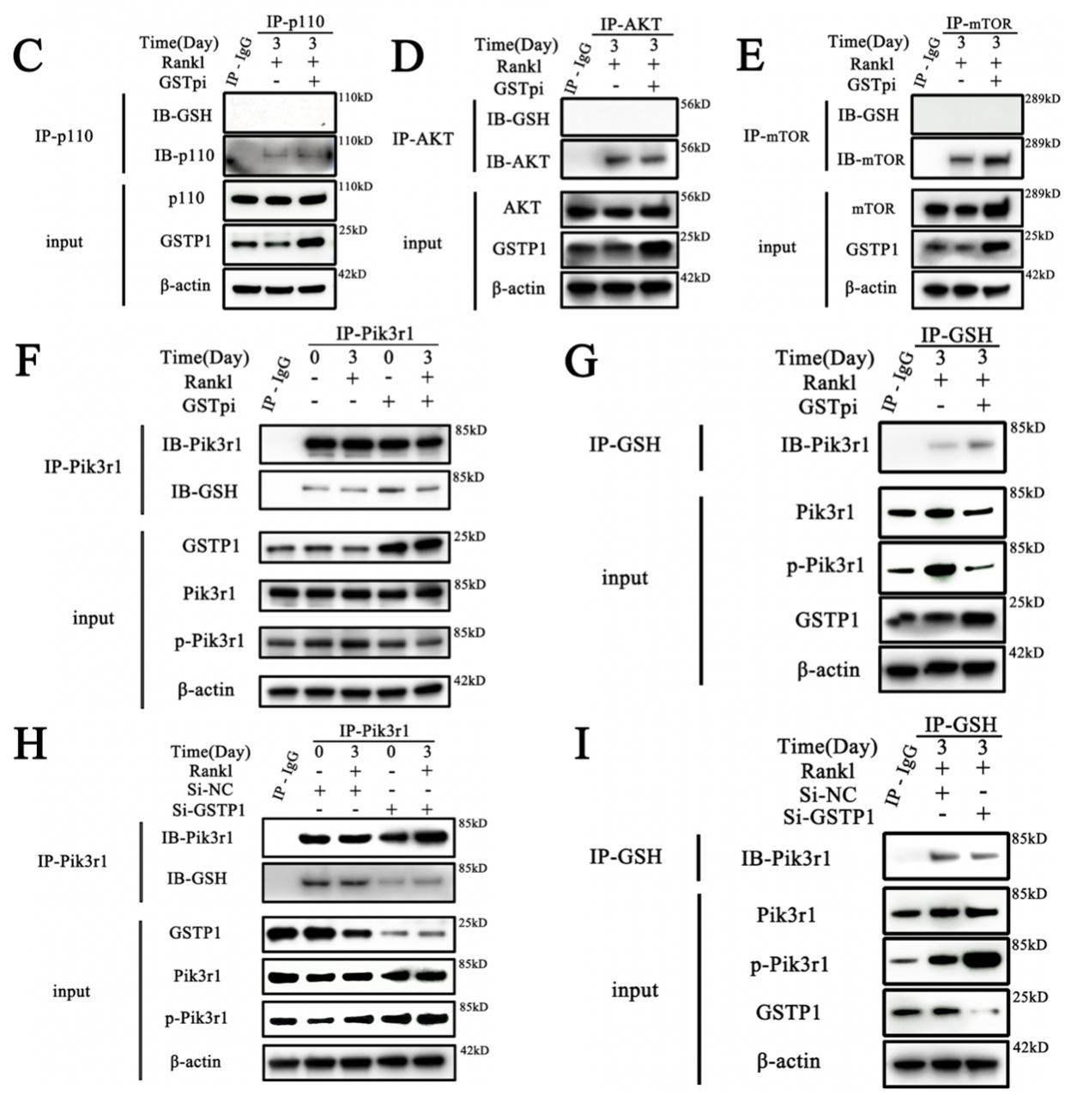
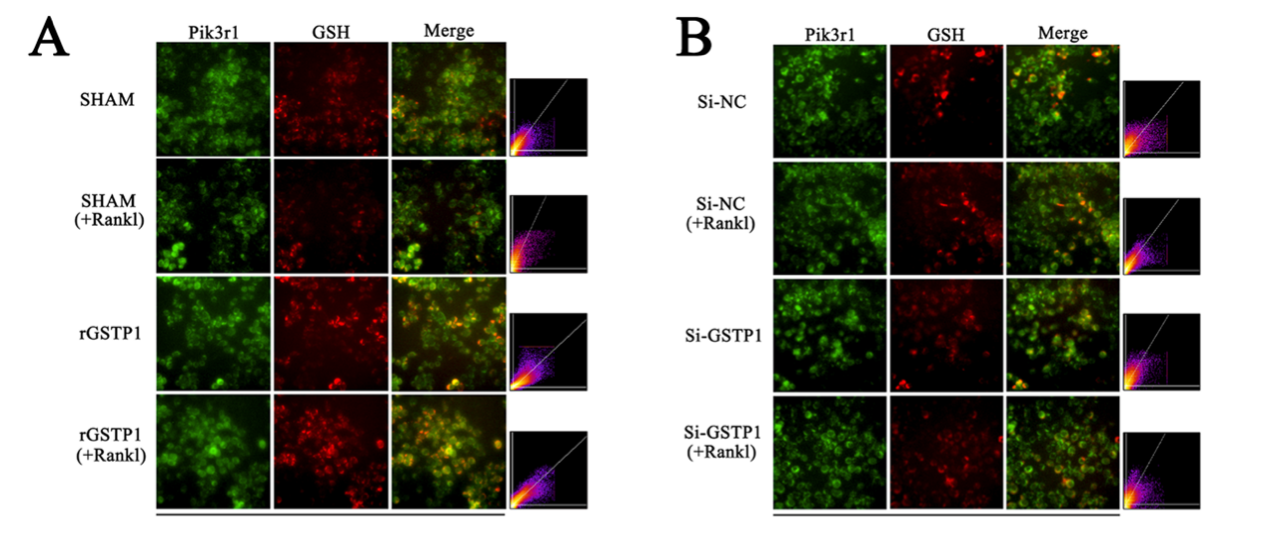
進一步驗證GSTP1下游激酶活性的調控是否與S-谷胱甘肽有關,作者探索了Pik3r1更微觀的蛋白質分子結構,首先,不同物種的初步序列比對顯示Pik3r1中的4個半胱氨酸(Cys498,Cys656,Cys659,Cys670)在進化上是保守的,表明半胱氨酸殘基在Pik3r1功能的調控中發揮着重要作用。免疫共沉澱結果顯示過表達和敲低GSTP1在破骨細胞形成過程中改變了Pik3r1的S-谷胱甘肽化水平,進而下調了Pik3r1作為激酶的磷酸化水平。
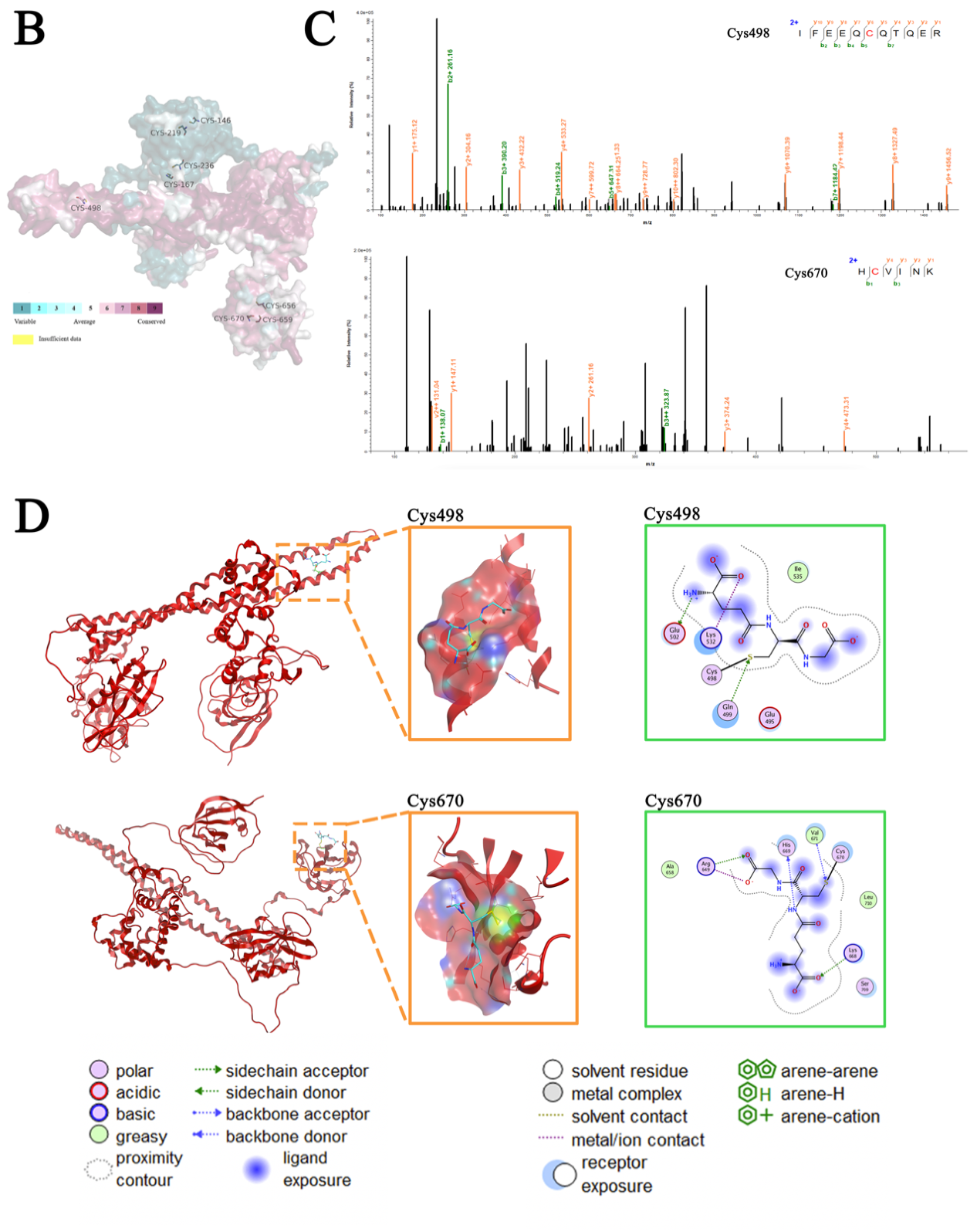
接着,通過非還原非變性免疫共沉澱以及氧化還原相關修飾質譜堅定到Cys498和Cys670可以發生S-谷胱甘肽化。此外,分子蛋白對接的結果也表明,Cys498和Cys670更容易與GSH發生相互作用。二維圖像清楚地顯示谷胱甘肽與蛋白質Pik3r1-CYS498共價對接後,谷胱甘肽與GLN499和GLU502形成氫鍵,與LYS532和GLU502發生靜電相互作用;同樣地,Pik3r1-CYS670與配體GSH對接的二維圖譜顯示,小分子GSH與HIS669、HIS668、ARG649、VAL671形成氫鍵,與ARG649存在靜電相互作用。
綜上,作者確定了Cys498和Cys670是Pik3r1發生S-谷胱甘肽化的兩個半胱氨酸殘基位點。
為了闡明GSTP1介導的Pik3r1的S-谷胱甘肽化在破骨細胞生成中的作用,作者先用CRISPR/Cas9基因編輯技術敲除RAW264.7細胞中的Pik3r1,排除內源Pik3r的影響,然後用丙氨酸替代其中可能發生S-谷胱甘肽化半胱氨酸位點,構建了3個單位點突變質粒和1個雙位點突變質粒。最後,將這些突變質粒和野生型myc-Pik3r1質粒轉染到Pik3r1-KO的RAW細胞中完成後續實驗。源井基因編輯提供了CRISPR/CAS9基因編輯技術,成功構建了Pik3r1的敲除RAW264.7細胞系(如下圖),為後續的突變回補驗證奠定了重要基石。
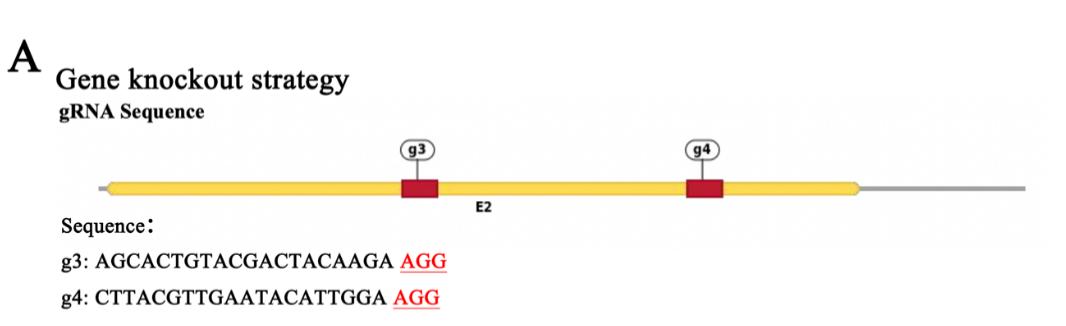
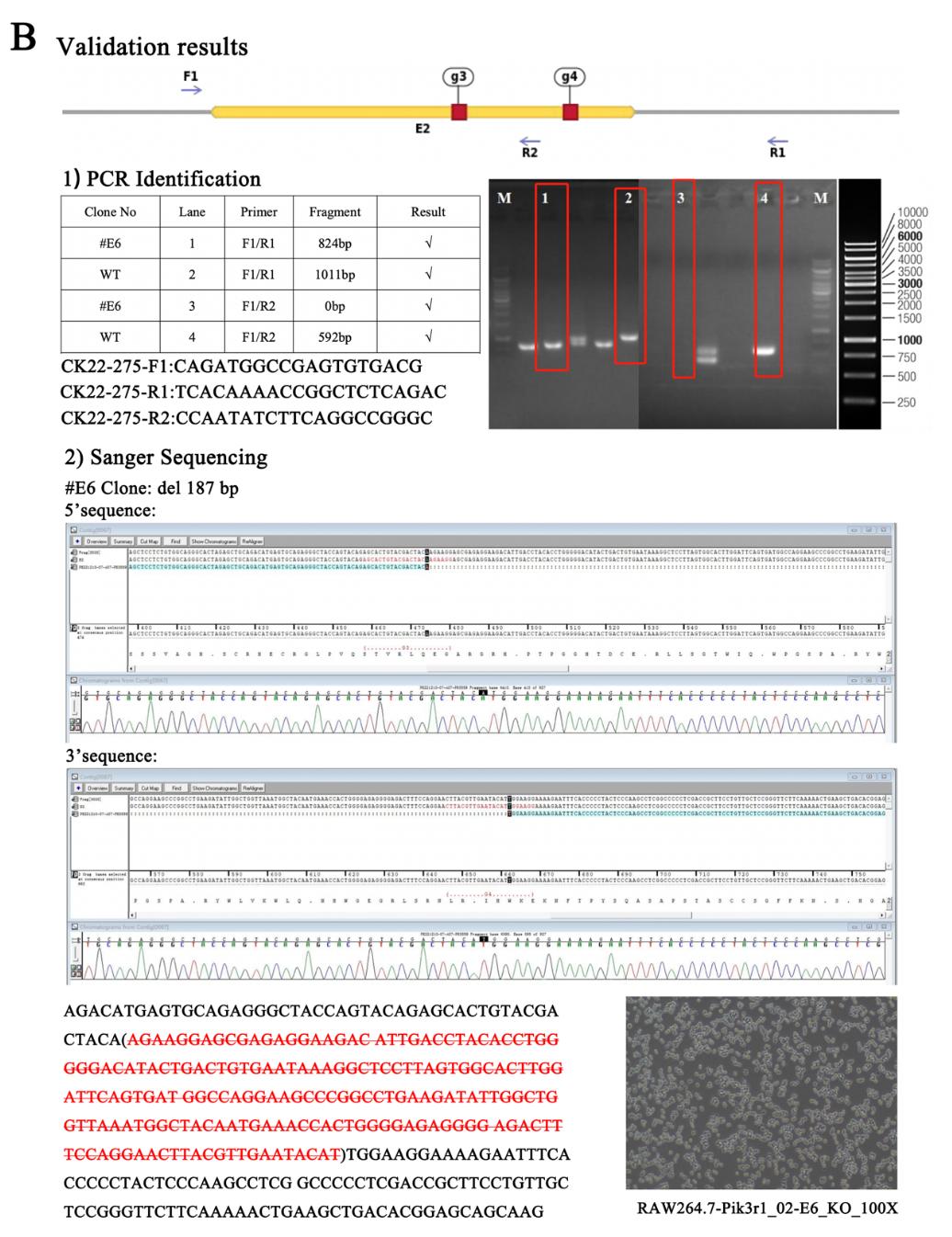
補充圖11:
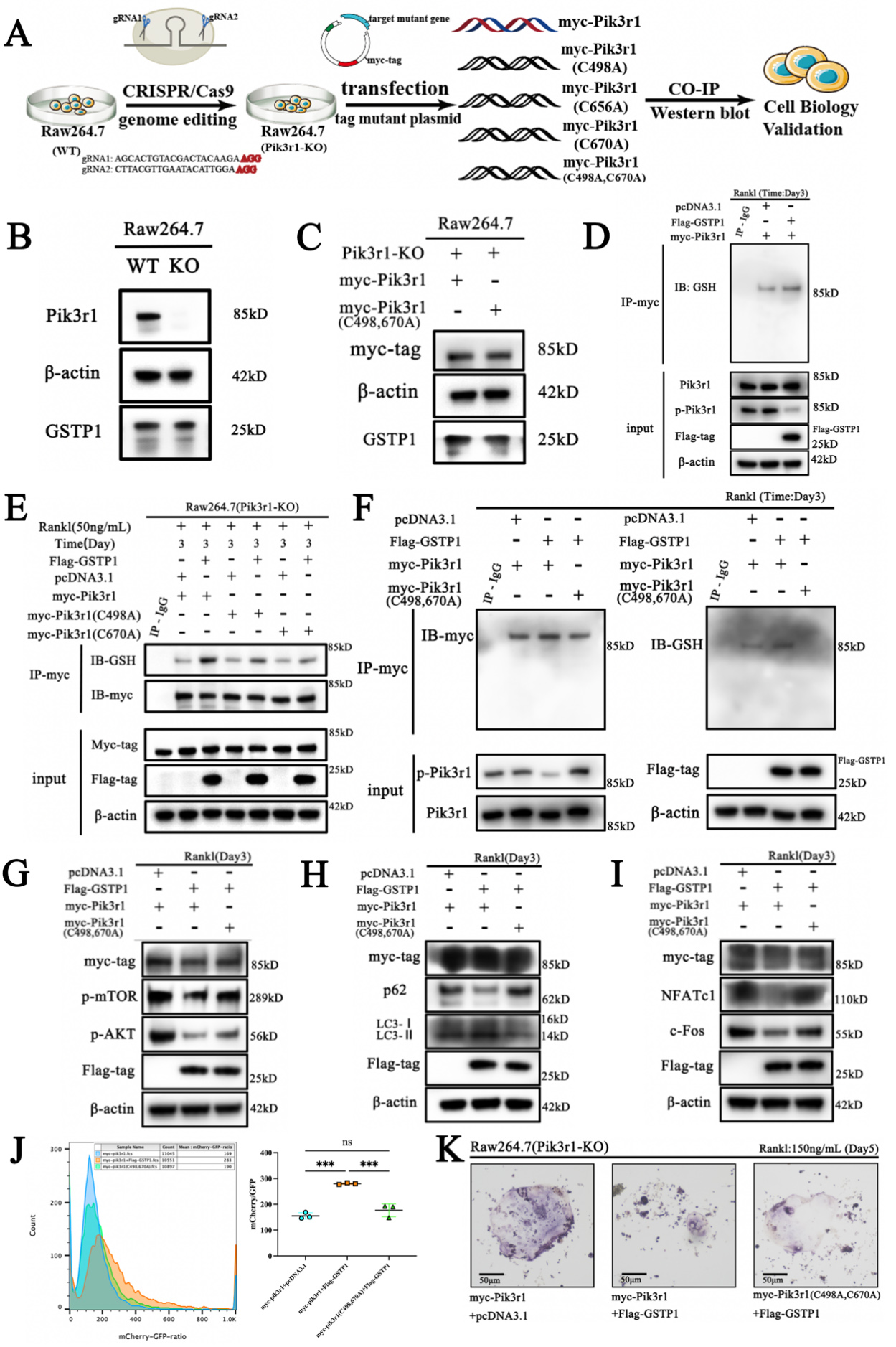
圖 7 GSTP1 介導的 Pik3r1 的S-谷胱甘肽化調節破骨細胞生成
在破骨細胞形成過程中,共免疫沉澱的結果表明,在轉染了C498A和C670A 突變質粒的細胞中,GSTP1介導的Pik3r1 S-谷胱甘肽化水平低於轉染了野生型質粒的細胞。但在轉染了C656A突變質粒轉染的細胞中Pik3r1的S-谷胱甘肽化水平沒有顯著差異。此外,作者同時突變Cys498和Cys670,並將雙突變質粒轉染到Pik3r1-KO的Raw264.7細胞中。在相同條件下,免疫共沉澱結果顯示GSTP1介導的S-谷胱甘肽化水平被完全消除(圖7F),這有力地證明了破骨細胞生成過程中GSTP1介導的Pik3r1的S-谷胱甘肽化是通過Cys498和Cys670實現的。
至此,作者通過詳盡的體外實驗證明Cys498和Cys670是GSTP1介導的Pik3r1發生S-谷胱甘肽化的兩個半胱氨酸位點,並且這種氧化還原相關的修飾可以通過Pik3r1-AKT-mTOR級聯通路調節自噬通量並最終抑制破骨細胞生成。
該研究通過大量的體內外實驗探索了GSTP1重塑破骨細胞相關骨穩態的一種全新機制,第一次詮釋了破骨細胞的細胞命運是由GSTP1介導的氧化還原相關的翻譯後修飾-自噬流級聯軸來決定的。