中國原研創新藥出海最後一塊拼圖,為什麼是“價格保護”_風聞
氨基观察-生物医药新时代的商业智库和价值灯塔10-19 10:53
當出海成為必答題,所有人都在看着,中國原研創新藥的國際化征途走到了哪一步?
過去幾年,從BTK抑制劑澤布替尼、CAR-T療法西達基奧侖賽,再到PD-1替雷利珠單抗,一個個選手的成功突圍,意味着中國原研創新藥開始與世界接軌。不過,嚴格來説,當前還只是出海的上半場。
替雷利珠單抗們的出現,論證了中國藥企能夠做出兼具品質、創新的好藥;然而,未摘掉的“低價”標籤,仍是掣肘中國藥企海外定價和商業化的重要因素。
換句話説,中國原研創新藥行業還需更進一步,才能開啓出海下半場。
藥企的成長與生態環境相輔相成。中國原研創新藥要想撕掉“低價”標籤,需要更多企業走出內卷怪圈,也需要政策層面給予更多支持,例如在“價格保護”方面做得更好。
實際上,藥企出海的意義不僅僅是與全球接軌,也是整個行業真正形成良性的創新循環、惠及更多患者的關鍵。説白了,這也是我國生物醫藥產業實現“從大到強”的必經之路。
如今,原研創新藥出海浪潮越來越猛烈,這些問題的解決顯得愈發迫切。
/ 01 / 出海答卷日漸清晰
過去創新藥出海之所以進展較少,是客觀原因造成的。不同的監管、商業化環境,導致出海對所有中國藥企都是一個全新、複雜的考驗。**如今,隨着先行者們的逐步探索,出海答卷已經日漸清晰:**過硬的產品質量、世界級研究數據、全球佈局的臨牀註冊能力。
**過硬的產品質量是根本。**在全球性3期頭對頭研究中,澤布替尼對比第一代BTK抑制劑伊布替尼,取得顯著的優效性結果,這使得澤布替尼備受認可成為Best in class;西達基奧侖賽的臨牀數據,也預示着其擁有更好的療效和安全性數據,最終在與Abecma的對壘中可以不佔劣勢地位。而首個出海的PD-1替雷利珠單抗也具有差異化競爭優勢,其分子設計旨在最大限度地減少與巨噬細胞中的 Fcγ受體結合,具有顯著增強抗腫瘤活性的特點。
**世界級研究數據則是必選項。**這要求藥企從立項一開始就高標準、嚴要求,以國際化視角去設計實驗方案並貫徹執行。這也是替雷利珠單抗成為首個順利出海的國產PD-1的核心原因。
可以看到,此次替雷利珠單抗歐洲上市的依據RATIONALE 302研究,入組了來自歐洲、亞洲和北美洲11個國家和地區共132個研究中心的513例患者。實際上,除了提供RATIONALE 302研究的臨牀數據,百濟神州共提供了7項臨牀試驗中,1972例接受替雷利珠單抗單藥治療患者的安全性數據。
**全球臨牀註冊能力,決定着出海的效率與進度。**國際多中心臨牀入組地點較多,對藥企的研發團隊及運營團隊有着極高的要求,不僅要嚴格把握國際準則、入組患者的入排標準、試驗質量控制,還要非常熟悉海外臨牀註冊法規的各項要求。
替雷利珠單抗能夠後來居上,正是因為百濟神州全球臨牀註冊羽翼已豐。從2015年起就開始和全球監管打交道,百濟神州積累了豐富的全球臨牀註冊經驗。澤布替尼已累計在全球超過65個國家及地區獲批,在歐美等主流發達國家實現廣泛覆蓋的同時,也已在多個新興市場上市。
這些能力最終在替雷利珠單抗的身上也得到了延續。替雷利珠單抗的全球臨牀開發絕大部分都由百濟神州推進。除了疫情因素,百濟神州的出海很少遇到“延遲”的情況。
某種程度上,越來越多的成功出海案例傳遞出的積極信號是,面對一個全然陌生的市場,中國藥企已然能夠走得越來越穩妥。這也意味着,中國原研創新藥的出海大潮正加速來襲。
/ 02 / 加速良性創新循環
對於以傳奇生物、百濟神州為代表的創新藥企而言,一旦進入全球市場,將會加速形成良性創新循環,有能力惠及更多患者。
一方面,出海能為藥企帶來穩定的現金流回報,畢竟歐美市場在政策、供給、價格及支付體系方面,都營造了良好的環境。
不管是澤布替尼還是西達基奧侖賽,都已證明海外商業化環境能夠創造相當可觀的收益。今年上半年,澤布替尼美國收入高達25.19億元,帶動百濟神州收入大幅增長72%,達到72.5億元;西達基奧侖賽海外收入也達到了1.89億美元,上半年銷售額已超去年全年。接下來,替雷利珠單抗大概率也是如此。
**更重要的是,出海能夠獲得更高的利潤空間。**根據百濟神州總裁、首席運營官吳曉濱透露,替雷利珠單抗未來在海外的定價和國內不會一樣,將參考海外支付能力。目前,K藥在美國年治療費用超過17萬美元,而替雷利珠單抗在國內年治療費用不足1萬美元。
很顯然,如果成功撬動海外市場,處於“卷王”賽道的替雷利珠單抗,仍將為百濟神州帶來極為顯著的業績增量,加速公司走向盈利節點,也有能力投入更多資源在創新研發層面。
另一方面,出海能為藥企獲取海量真實世界患者數據,讓藥企洞見更為真實的臨牀需求,從而滿足更多臨牀未滿足的需求。
因為真實世界的情況複雜程度遠超註冊試驗入選的患者。只有通過真實世界數據的積累、研究,才能更充分了解不同治療方案對病人的治療效果,為藥企帶來更多研發思路,從而為患者帶來更多獲益。
顯而易見的一點是,隨着中國藥企海外商業化的推進,穩定的現金流回報和大量的真實世界患者數據,能夠進一步反哺創新研發,加速蜕變,最終實現良性循環發展。這也將進一步助力我國醫藥產業的升級。
不過,在此之前仍有一些關鍵問題需要得到解決,整個行業也需要一場務實主義的勝利。
/ 03 / 亟需撕掉“低價”標籤
何為務實主義?對於中國原研創新藥來説,實現商業化變現,形成閉環是整個行業良性發展的基礎,也是屬於創新藥的務實主義。
從跟隨、反超,再到希望引領發展,中國創新藥行業已經進入關鍵階段。在這一背景下,要想獲得突破性發展,就必須解決一些問題,比如亟需撕掉的“低價”標籤。
“低價”標籤在PD-1領域體現的最為明顯。如下圖所示,PD-1在國內市場的定價,中國藥企的原研藥價格均不足K藥、O藥的50%。
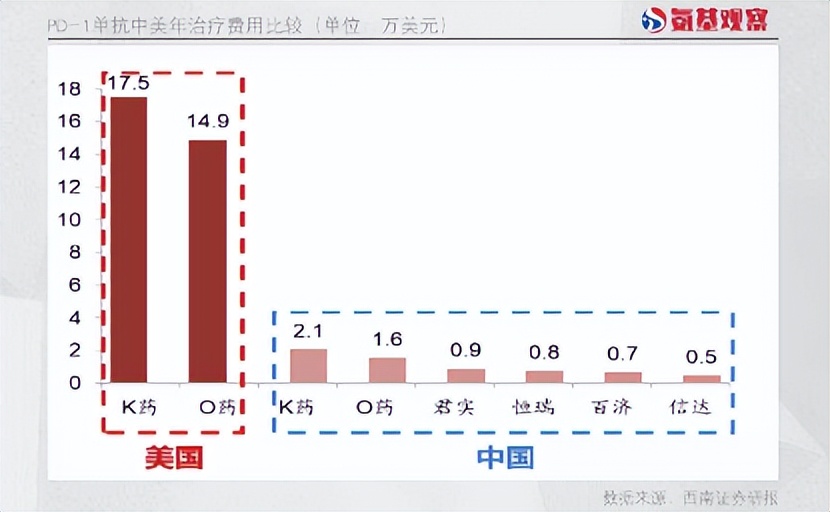 而如果與K藥、O藥在海外的定價相比,差距則更為明顯,價差甚至超過90%。固然,低價很大程度上能夠惠及更多患者,但創新藥行業並不能“唯低價論”。過低的藥價反而會反噬創新生態,影響出海等戰略的順利推進。
而如果與K藥、O藥在海外的定價相比,差距則更為明顯,價差甚至超過90%。固然,低價很大程度上能夠惠及更多患者,但創新藥行業並不能“唯低價論”。過低的藥價反而會反噬創新生態,影響出海等戰略的順利推進。
畢竟,中國作為原創國,藥品的國內價格往往被視為海外市場的價格基礎,國內過低的價格一定程度上導致,創新藥品在海外市場失去定價主動權,影響了本土創新藥出海的定價和市場拓展。
從長遠角度來看,“低價”標籤的存在,實際上影響着整個行業良性發展閉環的達成。
沿着舊地圖,找不到新大陸。只是,撕掉“低價”標籤的過程不是一蹴而就的,而是需要多方的共同努力。
**一方面,需要企業走出內卷怪圈,**真正做到以臨牀未滿足需求為導向進行創新藥的開發,從源頭上避免內卷,減少價格戰的可能;
**另一方面,也需要監管的持續探索。**只有真正做到了“價格保護”,才能最大程度上促進出海等創新生態的繁榮,造福更多患者。這一點,在海外創新藥發展過程中已經得到了充分驗證。
**包括美國、日本、歐洲等國家地區,對於高臨牀價值創新藥都有着符合其國情的價格保護政策。**比如日本,創新藥的利潤可根據創新性、療效、安全性等調整,這使得小野製藥在日本對納武利尤單抗的定價,超過百時美施貴寶在美國定價的兩倍。也正是這些激勵政策,讓日本藥企在免疫療法、ADC等諸多創新領域,在全球都具有極高的競爭力。
即使是在嚴格控制藥價的法國,為了推動創新、促進投資和出口,兩年前法國也對部分藥價管控條款進行了大幅修改。比如,在滿足公共健康需求的同時,推動某些改良型藥品(ASMR 4級)接軌歐盟價格;由於生產費用可能會造成一定的供應問題,允許某個治療領域整體或部分藥品可以維持較高價格;在ASMR5級藥品上市的前三年中,固定其價格等等。
**回到國內來説,探索符合國情的價格保護機制也必然非常關鍵。**例如在支付環節,除了老生常談的商保,也可以探索支付創新試點,建立基於臨牀價值(療效)的創新藥支付新機制;探索建立多方共付新機制,給予創新藥企更自主的定價空間。
**甚至,還包括更多政策的探索,比如醫保支付標準的“保密”做法。**在美國保險公司與代表支付方的藥品福利管理公司(PBM)與藥品生產企業進行價格談判後,支付價格通常作為商業機密不對外公佈。
在不少人眼中,中國創新藥行業仍有許多不足,但成長是顯而易見的。如今,站在產業崛起的時代背景下,行業各方需要努力,加速下半場的到來。
