《華爾街日報》:個性化幹細胞有望未來治療帕金森病、心力衰竭和黃斑變性
Nidhi Subbaraman
將實驗室培養的、由患者自身細胞製成的腦細胞注入體內,能否逆轉帕金森病的症狀?這是總部位於聖地亞哥的初創公司Aspen Neuroscience Inc.計劃在今年晚些時候進行人體試驗的想法。
在帕金森病患者中,神經元死亡並失去製造化學物質多巴胺的能力,導致不規律、無法控制的運動。Aspen Neuroscience將測試新注入的細胞是否能成熟為多巴胺生產者,從而阻止這種無法治癒的疾病的衰弱症狀,該公司首席執行官Damien McDevitt表示。公司表示,動物試驗已取得積極結果。
Aspen Neuroscience是幾個計劃進行人體試驗的團隊之一,這些試驗使用通過逆向工程將患者自身細胞還原為幹細胞狀態製成的幹細胞進行治療。這些“誘導多能幹細胞”或iPS細胞的行為類似於胚胎細胞,可以發育成任何類型的細胞。
研究人員希望他們可以將患者的iPS細胞培養成一系列健康細胞,以治療目前無法治癒的疾病。其中,美國國立衞生研究院的一個團隊正在領導一項始於2019年的試驗,使用從患者血液樣本中培養的眼組織來治療黃斑變性,這是導致視力喪失的主要原因。今年晚些時候,梅奧診所的一項試驗將通過手術植入從患者皮膚細胞培養的心臟組織,以治療先天性心臟病。
這些早期臨牀試驗將是幹細胞生物學家長期追求的理念的“原理驗證”測試,Whitehead研究所和麻省理工學院的幹細胞生物學家Rudolf Jaenisch表示,他在1980年代和90年代在遺傳學領域做出了開創性工作。Jaenisch博士表示,由於涉及的時間和成本,使用患者產生的iPS細胞作為治療手段尚不實際,但最初的試驗是有價值的。“我們必須弄清楚:這到底有效嗎?”
這種新穎的方法與使用幹細胞胚胎的類似試驗不同,它從患者體內提取血液或皮膚細胞開始,通過實驗室過程將其轉變為幹細胞。然後這些幹細胞被培養成特定類型的細胞,如眼組織、心臟細胞或神經元。雖然以這種方式培養修復組織既昂貴又耗時,但科學家希望這將降低組織被人體免疫系統排斥的幾率,因為它源自患者自身。
研究人員承認,植入源自幹細胞的組織存在風險。非目標細胞類型或可能形成腫瘤的細胞可能會在目標組織的位置生長。此外,患者的身體仍有小概率會排斥植入的組織。
多年來,幹細胞研究使用的是在生育診所通過體外受精創造並由夫婦捐贈用於研究的胚胎,或從流產中獲得的胎兒組織。然而,這些細胞的來源材料有限,並且美國政府對資金的使用存在法律限制。
再生醫學領域在2006年得到了推動,當時在日本京都大學工作的幹細胞生物學家山中伸彌發現了一組似乎能讓成年小鼠細胞“時光倒流”的基因,將它們轉變為胚胎狀態。
如今,幹細胞科學的進步使研究人員能夠精確可靠地轉化成年細胞。他們找到了生長因子、蛋白質和分子的正確組合,模擬細胞在胎兒中發育的環境,並將其傳遞給細胞。他們還改進了方案——對細胞基因組進行測序,或分析細胞產生的蛋白質——以確定他們實驗室培養的組織是否是正確的類型且無錯誤。
 珍妮·洛林(Jeanne Loring)是加州拉霍亞斯克裏普斯研究所的幹細胞生物學家,也是阿斯彭神經科學公司的聯合創始人。照片:斯克裏普斯研究所“我們已掌握了所有必要的技術環節,”加州拉霍亞斯克裏普斯研究所幹細胞生物學家、阿斯彭神經科學公司聯合創始人珍妮·洛林表示,“關鍵在於反覆不斷地實踐。”
珍妮·洛林(Jeanne Loring)是加州拉霍亞斯克裏普斯研究所的幹細胞生物學家,也是阿斯彭神經科學公司的聯合創始人。照片:斯克裏普斯研究所“我們已掌握了所有必要的技術環節,”加州拉霍亞斯克裏普斯研究所幹細胞生物學家、阿斯彭神經科學公司聯合創始人珍妮·洛林表示,“關鍵在於反覆不斷地實踐。”
然而進展依然緩慢。使用患者來源iPS細胞(又稱自體細胞)的研究團隊表示,按照現有方法為單個患者製備並測試治療組織需耗時數月。“當iPS細胞首次被報道時,我曾預測‘十年內將進入臨牀’,”加州大學戴維斯分校幹細胞生物學家保羅·克內普夫勒坦言,“但顯然這個過程要漫長得多。”
山中伸彌博士因發明iPS細胞獲得2012年諾貝爾獎,現同時任職於舊金山格拉德斯通研究所。他表示,利用患者自身細胞培育定製化組織本是這項技術的理想應用場景,但高昂成本與漫長週期促使他轉向了略有不同的研究方向。
 幹細胞生物學家山中伸彌(攝於2019年)因發明iPS細胞獲得2012年諾貝爾獎。照片:Yoshio Tsunoda/AFLO/Zuma Press自體iPS細胞的早期試驗之一涉及日本一名患有年齡相關性黃斑變性的老年女性。2014年,她接受了由自身皮膚細胞培養的視網膜細胞移植。根據《新英格蘭醫學雜誌》發表的報告,一年後她的視力既未改善也未惡化,且未出現嚴重副作用。
幹細胞生物學家山中伸彌(攝於2019年)因發明iPS細胞獲得2012年諾貝爾獎。照片:Yoshio Tsunoda/AFLO/Zuma Press自體iPS細胞的早期試驗之一涉及日本一名患有年齡相關性黃斑變性的老年女性。2014年,她接受了由自身皮膚細胞培養的視網膜細胞移植。根據《新英格蘭醫學雜誌》發表的報告,一年後她的視力既未改善也未惡化,且未出現嚴重副作用。
參與該研究的山中伸彌博士表示,團隊在針對該眼疾患者的更大規模後續試驗中選擇了使用供體細胞。他擔任理事的日本CiRA基金會已建立了一個由捐贈者iPS細胞組成的細胞庫,供研究和臨牀試驗使用。這縮短了獲取組織的時間,但接受這些細胞的患者通常需要服用抗排斥藥物。
iPS細胞治療費用高昂,每名患者預估費用約10萬至近100萬美元。研究人員表示,若治療成功並廣泛應用,成本將會下降。
今年,梅奧診所的醫學與分子實驗藥理學副教授蒂姆·尼爾森將帶領團隊開展試驗,通過手術向先天性心臟病患者注射源自患者皮膚細胞的實驗室培養心肌組織。尼爾森博士(同時是非營利研究組織HeartWorks的聯合創始人)表示,這項試驗旨在驗證新組織是否能強化衰弱的心肌——這種病症通常需要進行心臟移植。
“我們將在未來十年進入這一階段,真正見證這一領域、這項技術蓬勃發展,成為現實應用,”尼爾森博士表示。
美國國立衞生研究院下屬的一個團隊去年為一名晚期“乾性”年齡相關性黃斑變性患者手術植入了工程化視網膜組織。該疾病會導致患者視網膜細胞衰竭,引發視力模糊乃至失明。
該研究負責人、馬里蘭州貝塞斯達市美國國立眼科研究所幹細胞生物學家卡皮爾·巴蒂表示,NIH團隊培育的視網膜組織始於一次抽血。
巴蒂博士稱,其團隊通過按特定順序添加精確配比的試劑組合,開發出一種能穩定從幹細胞培育視網膜細胞的方法。團隊希望今年招募更多患者,在12人身上測試該手術的安全性。巴蒂博士表示,從抽血到手術的整個過程約需六個月。
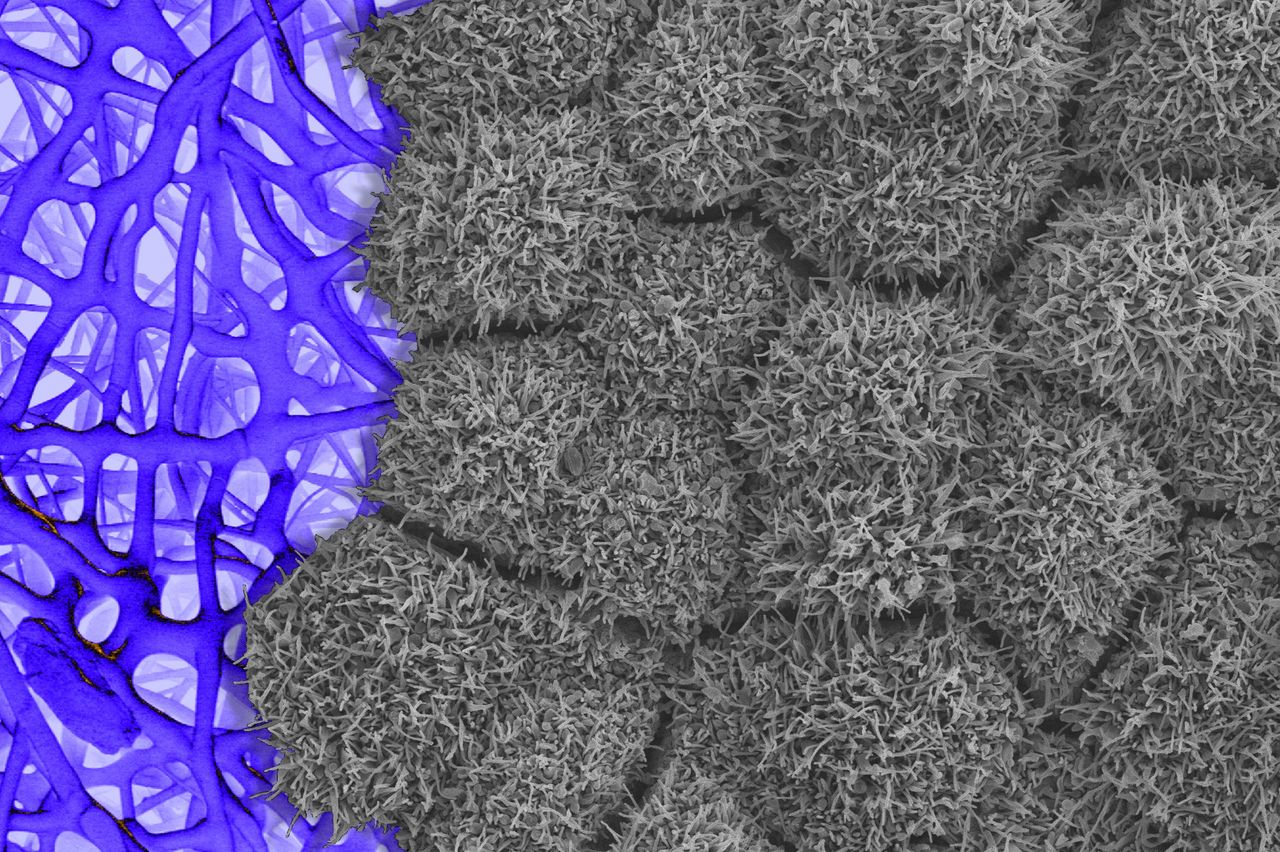 由幹細胞製造的視網膜組織在支架上生長(左圖所示)。通過掃描電子顯微鏡可見,視網膜細胞上的毛髮狀結構表明它們已完全成熟且功能正常。圖片來源:巴蒂實驗室/美國國立眼科研究所/NIH巴蒂博士指出,過去指導幹細胞生長為組織的方案存在缺陷是一大挑戰。細胞系會失控生長為不需要的細胞類型,或形成腫瘤。NIH團隊表示已在其視網膜組織工程中優化了這些步驟。“該方案的成功率超過95%,”巴蒂博士説。
由幹細胞製造的視網膜組織在支架上生長(左圖所示)。通過掃描電子顯微鏡可見,視網膜細胞上的毛髮狀結構表明它們已完全成熟且功能正常。圖片來源:巴蒂實驗室/美國國立眼科研究所/NIH巴蒂博士指出,過去指導幹細胞生長為組織的方案存在缺陷是一大挑戰。細胞系會失控生長為不需要的細胞類型,或形成腫瘤。NIH團隊表示已在其視網膜組織工程中優化了這些步驟。“該方案的成功率超過95%,”巴蒂博士説。
他表示,在更多患者接受該療法前,不會對現有患者的療效發表評論。
阿斯彭神經科學公司的定製腦細胞最初來源於皮膚細胞。該公司研發高級副總裁兼聯合創始人安德烈斯·布拉特-利爾介紹,先從患者肩部取下一塊橡皮大小的皮膚組織,溶解於溶液中後在培養皿中培育。通過每日添加特定試劑組合,這些細胞被轉化為幹細胞。隨後精選出純淨的幹細胞羣落,再經過新一輪試劑誘導,使其分化為神經元前體細胞。
這家公司正在冷凍儲存其培育的腦細胞,其技術突破在於設計了DNA和RNA測序步驟,可對培養皿中的細胞進行基因突變抽檢(這些突變可能導致腫瘤),從而避免了將iPS細胞培育的組織植入齧齒動物體內這種更耗時的檢測方法。
麥克德維特博士透露,阿斯彭神經科學已從10名帕金森患者體內培育並冷凍了細胞。在等待美國食品藥品監督管理局批准的同時,公司計劃今年內對部分受試者展開臨牀試驗,預計三年左右可獲得結果。
聯繫記者尼迪·蘇巴拉曼請致信[email protected]
本文發表於2023年3月24日印刷版,標題為《科學家測試個性化幹細胞療法》。