印度工廠質量問題導致藥品短缺——《華爾街日報》
Dominique Mosbergen and Brianna Abbott
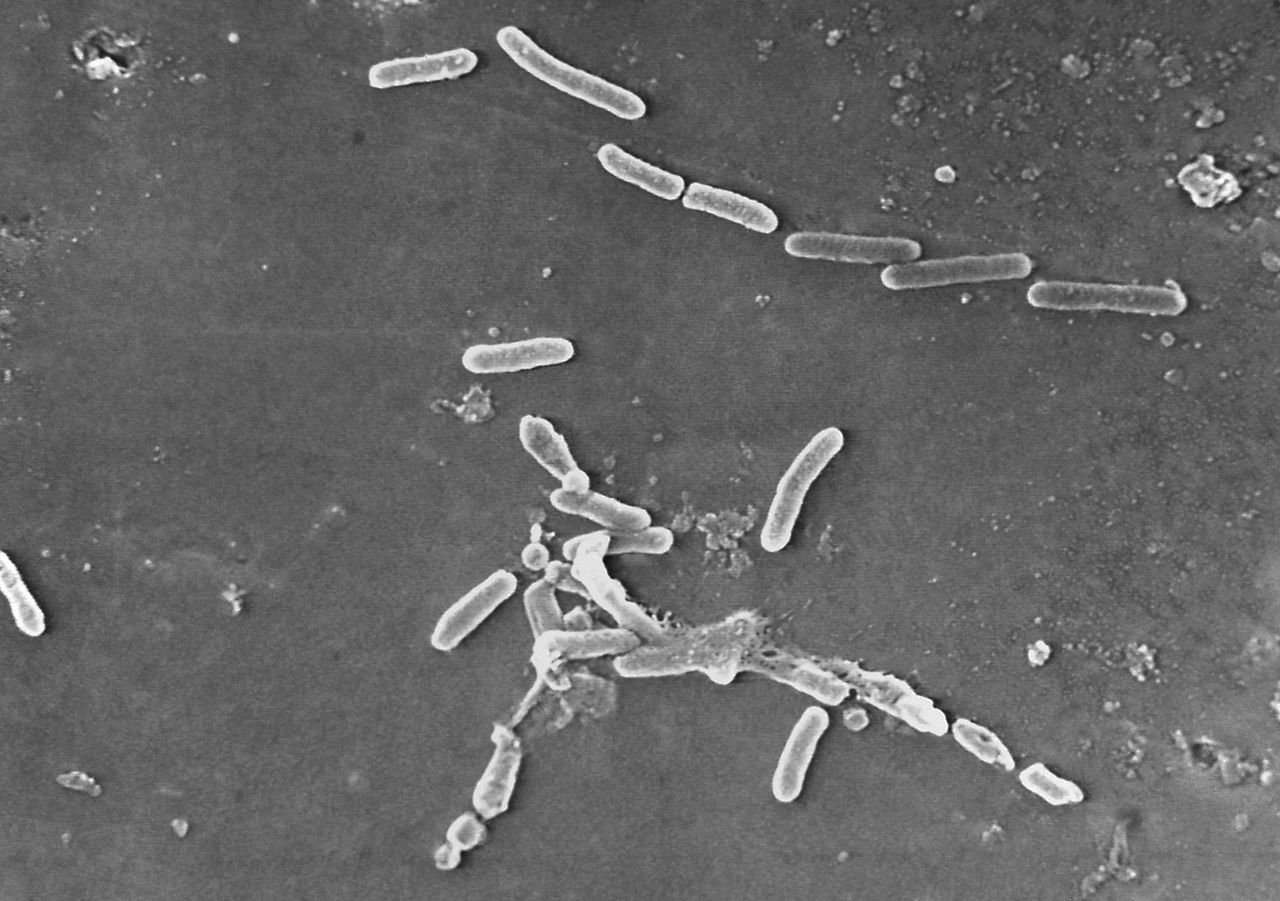 銅綠假單胞菌的顯微鏡圖像,這種病原體與被污染的眼藥水產品以及美國視力喪失病例和死亡有關。圖片來源:Janice Haney Carr/美國疾病控制與預防中心/美聯社印度工廠的惡劣條件使美國人生病,並加劇了癌症患者化療藥物的短缺,這引發了要求提高仿製藥供應韌性的呼聲。
銅綠假單胞菌的顯微鏡圖像,這種病原體與被污染的眼藥水產品以及美國視力喪失病例和死亡有關。圖片來源:Janice Haney Carr/美國疾病控制與預防中心/美聯社印度工廠的惡劣條件使美國人生病,並加劇了癌症患者化療藥物的短缺,這引發了要求提高仿製藥供應韌性的呼聲。
美國疾病控制與預防中心表示,18個州有80多人感染,至少4人死亡,這是一起與印度Global Pharma Healthcare公司生產的受污染眼藥水有關的細菌爆發。
印度古吉拉特邦Intas製藥工廠的質量控制問題引發了美國癌症藥物順鉑和卡鉑的短缺。紐約大學朗格尼醫學中心Perlmutter癌症中心胸部腫瘤項目主任Vamsi Velcheti博士表示,這些用於治療肺癌、乳腺癌和前列腺癌等癌症的化療藥物沒有完美的替代品。
醫院正在延長藥物供應,一些患者接受的劑量減少,治療間隔時間延長,或改用副作用更大的其他藥物。Velcheti説:“這是全國範圍內的重大危機。”
印度500億美元的製藥業安全記錄堪憂。美國食品藥品監督管理局(FDA)2019年向國會報告稱,在約90個國家中,印度製藥商的合規檢查通過率最低。FDA表示,印度約83%的工廠符合安全與質量標準,而中國和美國分別為90%和93%。
“這對美國民眾安全和生命的威脅是真實存在的,“FDA前副局長、現任美以教育協會高級研究員的彼得·皮茨表示。
77歲的密歇根州居民貝弗利·詹寧斯去年4月使用在亞馬遜購買的EzriCare人工淚液後右眼失明。“我原以為這種眼藥水是安全的,“住在密歇根州奧托納貢的詹寧斯説。
 美國疾控中心表示,Global Pharma Healthcare公司生產、EzriCare經銷並於2月召回的人工淚液潤滑眼藥水,與導致美國80多人感染的細菌爆發有關。圖片來源:/Global Pharma Healthcare/美聯社她於5月在新澤西州聯邦法院對Global Pharma和亞馬遜公司提起訴訟。詹寧斯還起訴了經銷該眼藥水的新澤西州公司EzriCare,以及紐約進口商Aru Pharma。
美國疾控中心表示,Global Pharma Healthcare公司生產、EzriCare經銷並於2月召回的人工淚液潤滑眼藥水,與導致美國80多人感染的細菌爆發有關。圖片來源:/Global Pharma Healthcare/美聯社她於5月在新澤西州聯邦法院對Global Pharma和亞馬遜公司提起訴訟。詹寧斯還起訴了經銷該眼藥水的新澤西州公司EzriCare,以及紐約進口商Aru Pharma。
亞馬遜和環球製藥未予置評。阿魯製藥和EzriCare未回應置評請求。美國食品藥品監督管理局(FDA)表示,其對處方藥製造商至少會進行一次檢查,但無需對非處方產品生產廠家進行常規檢查。FDA稱會根據潛在風險對這類設施進行抽查。印度衞生部未回應置評請求。
眼藥水等仿製藥和部分化療藥物主要產自海外,因其售價過低難以吸引美國製造商。印度和中國等國家憑藉較低的勞動力成本建立起龐大產業,為包括美國在內的全球市場大規模生產這些藥品。
印度官員稱該國是全球最大仿製藥供應國,佔全球供應量的五分之一,美國市場銷售的仿製藥40%來自印度。貿易數據顯示,2022年印度是美國第三大藥品進口來源國,僅次於中國和墨西哥。
對少數廉價藥品來源的過度依賴可能導致供應鏈中斷,一旦出現問題將使患者面臨風險。FDA指出,約60%的藥品短缺與質量問題有關。
“我們需要實現多元化,“與以色列、阿聯酋等國製藥商合作倡導的皮茨表示。
FDA去年對古吉拉特邦Intas製藥廠(生產多種抗癌藥物)的檢查發現"系統性失效”,包括數據缺失、防污染程序不完善,以及卡車裝載着多袋碎紙文件。Intas未回應置評請求。
該公司停止了用於治療全美癌症患者的順鉑和卡鉑生產,導致藥品短缺。美國食品藥品監督管理局(FDA)本月禁止從該工廠進口Intas公司藥品,但對包括供應短缺的卡鉑和順鉑在內的部分藥物予以豁免。
美國衞生系統藥劑師協會高級主任邁克爾·加尼奧表示,化療藥物等部分藥品必須在成本高昂的無菌環境下生產,但採購方無法直接比較不同藥廠的藥品質量,往往選擇最便宜的選項。
“這會導致惡性競爭,最終你根本不清楚自己買什麼,“加尼奧説。
2019年,FDA檢查了約半數在美註冊的印度製藥廠。2022年該機構僅檢查了其中約10%。
明尼蘇達大學藥物經濟學教授斯蒂芬·雄德爾邁爾指出:“當人們知道無人監管時,就會做出許多不該做的事。”
FDA表示正在加強疫情期間縮減的檢查力度。
直到EzriCare眼藥水生產商Global Pharma在今年2月主動召回產品後,FDA才首次檢查其工廠。3月的檢查報告指出,該廠缺乏確保無菌的規範操作,檢查人員目睹員工在應保持無污染的區域穿着褪色工作服和破損鞋套。
部分組織建議建立藥品儲備以應對未來短缺,行業機構與非營利組織正在開發醫療產品評級體系,幫助採購方判斷質量。
美國食品藥品監督管理局(FDA)表示,已於2月訪問印度,與監管機構和製藥商討論藥品質量問題,並建議國會要求製藥商提高產品成分透明度。
約翰霍普金斯大學運營管理與商業分析教授戴廷龍指出,國會應授權FDA定期對海外藥企進行突擊檢查,並強制仿製藥製造商提高供應鏈透明度。
“購買這些產品需自行承擔風險,“他表示。
——本文由Vibhuti Agarwal參與撰寫。
聯繫記者:Dominique Mosbergen,郵箱[email protected];Brianna Abbott,郵箱[email protected]