不再需要注射:類似Ozempic的口服藥物即將問世 - 《華爾街日報》
Peter Loftus
針對人們蜂擁使用Ozempic以大幅減重的情況:口服減肥藥正在研發中。
諸如Ozempic這類因減肥效果而人氣飆升的藥物必須注射使用。然而許多人厭惡針頭,這促使製藥商探索可吞嚥的劑型。
化學合成並不簡單。但如果研究人員能成功,藥片將吸引大量恐針人羣,同時成本比注射劑低數百美元。
將注射型減肥藥轉化為口服版本是當前最熱門的藥物研究領域之一,吸引了禮來、諾和諾德和輝瑞等行業巨頭,背後是潛在價值數十億美元的市場驅動。
進展最快的是諾和諾德開發的司美格魯肽片劑——該成分正是注射劑的主要活性物質。
 Ozempic因其顯著的潛在減重效果而廣受歡迎。圖片來源:Carolina Andrade/華爾街日報諾和諾德5月表示,在一項持續68周的每日服藥研究中,這種實驗性藥片幫助受試者最高減重17.4%,與Ozempic的姊妹藥物Wegovy的測試結果相當。
Ozempic因其顯著的潛在減重效果而廣受歡迎。圖片來源:Carolina Andrade/華爾街日報諾和諾德5月表示,在一項持續68周的每日服藥研究中,這種實驗性藥片幫助受試者最高減重17.4%,與Ozempic的姊妹藥物Wegovy的測試結果相當。
今年晚些時候,諾和諾德計劃向美國和歐洲藥品監管機構申請批准該片劑。諾和諾德已銷售治療2型糖尿病的口服司美格魯肽片劑Rybelsus,儘管有些人會超適應症使用它來減肥。
諾和諾德的Ozempic和Wegovy療法以及禮來的Mounjaro已成為風靡一時的藥物,受到名人吹捧並在Facebook和TikTok上討論,因為它們有可能幫助人們顯著減重。
這類藥物最初被批准用於治療糖尿病,其作用機制是模擬腸道激素,這些激素在調節血糖和食慾方面發揮作用。一種關鍵的腸道激素被稱為胰高血糖素樣肽-1,即GLP-1。
 諾和諾德正在開發司美格魯肽片劑,這是注射減肥藥的主要成分。 圖片來源:Jacob Gronholt-Pedersen/REUTERS肽是大分子,更容易以注射形式包裝和遞送**。製藥商還將他們的GLP-1藥物製成注射劑,以避免藥片因被吞服而經過消化道的旅程。**消化道可能會降解肽,從而降低其益處。
諾和諾德正在開發司美格魯肽片劑,這是注射減肥藥的主要成分。 圖片來源:Jacob Gronholt-Pedersen/REUTERS肽是大分子,更容易以注射形式包裝和遞送**。製藥商還將他們的GLP-1藥物製成注射劑,以避免藥片因被吞服而經過消化道的旅程。**消化道可能會降解肽,從而降低其益處。
但製造肽和注射它們的裝置(稱為筆)既昂貴又複雜。注射藥物必須在特定(通常是低温)温度下儲存。而且它們會讓一小部分但數量可觀的人羣感到恐懼。
“有些人就是害怕打針,”BMO資本市場分析師埃文·大衞·西格曼表示。
分析師預測,抗肥胖藥物市場將非常龐大,以至於製藥公司已開始努力開發適合不願注射人羣的口服藥物。
西格曼估計,口服減肥藥可能佔據約15%的市場份額,他預測未來幾年全球年銷售額將達到1000億美元。
製藥商通過提高劑量或採用非肽類腸道激素形式,設計出口服版腸道激素藥物以克服消化道降解問題。
醫生和分析師指出,由於化學特性限制,口服藥不太可能超越當前每週注射劑的減重效果,某些藥片效果甚至可能更差。部分患者或許仍傾向於選擇每週注射的便捷性而非每日服藥。
“我猜人們會説’每週一次聽起來簡單多了’,”西北大學範伯格醫學院肥胖治療專家羅伯特·庫什納博士表示。
但分析師和醫生認為,若定價更低,這類藥片對部分患者仍具吸引力。
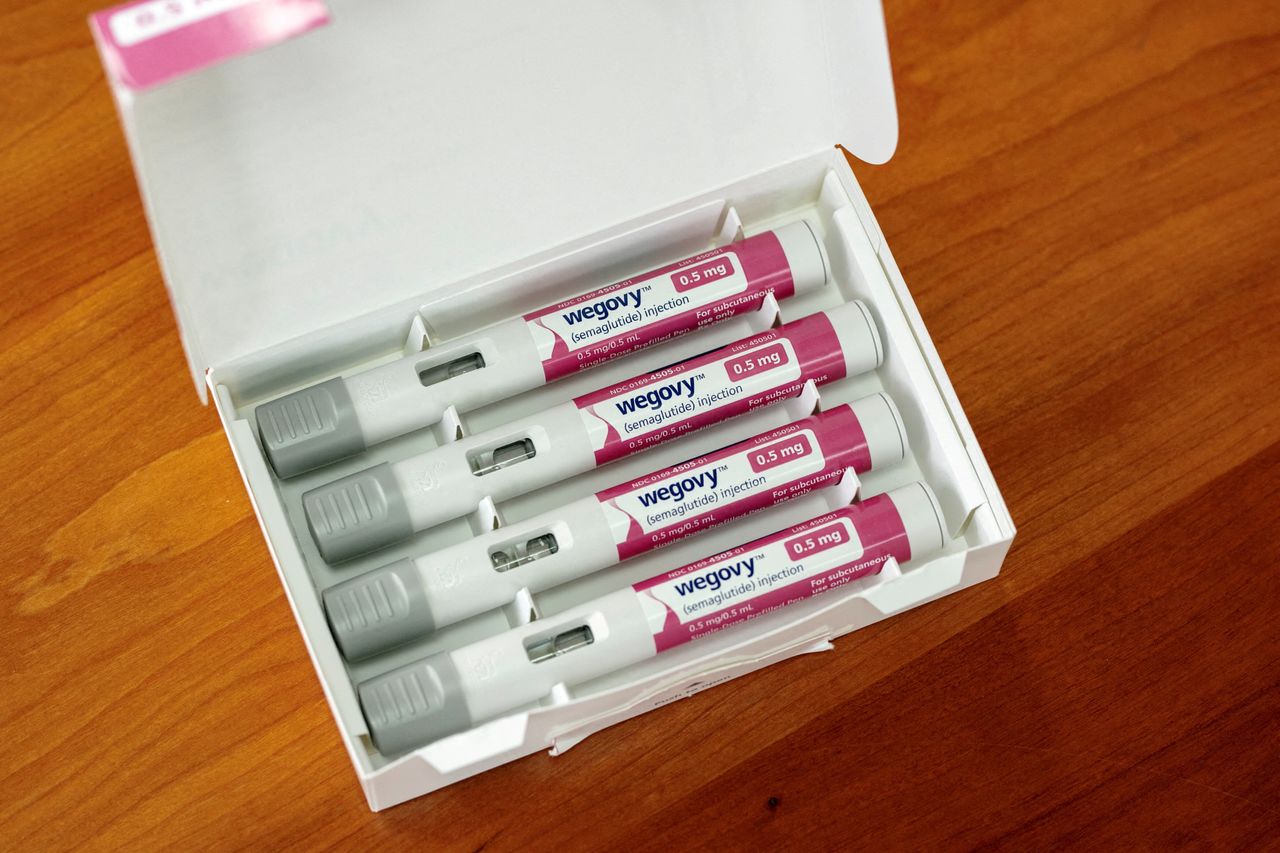 Wegovy注射筆圖片來源:JIM VONDRUSKA/REUTERS西格曼預估,若研發成功並通過審批,Structure Therapeutics開發的口服藥月定價約500美元,約為注射藥物成本的一半。該公司CEO雷蒙德·史蒂文斯表示討論具體價格為時尚早,但定價目標是讓患者能夠負擔。
Wegovy注射筆圖片來源:JIM VONDRUSKA/REUTERS西格曼預估,若研發成功並通過審批,Structure Therapeutics開發的口服藥月定價約500美元,約為注射藥物成本的一半。該公司CEO雷蒙德·史蒂文斯表示討論具體價格為時尚早,但定價目標是讓患者能夠負擔。
“如果這些口服藥物更經濟實惠或更易於獲取,它們或許能填補這一空白,”康涅狄格州紐黑文市耶魯大學肥胖研究中心主任Ania Jastreboff博士表示。
禮來公司正在研發一種名為orforglipron的非肽類GLP-1口服藥。研究人員週五在聖地亞哥舉行的美國糖尿病協會年會上報告稱,在一項針對270多名肥胖患者的中期臨牀試驗中,每日服用一次的該藥物在36周內幫助受試者減重最高達14.7%。
對於研究中平均起始體重為240磅(約109公斤)的受試者而言,這相當於減重約35磅(約16公斤)。
禮來近期已啓動更大規模的後期臨牀試驗,以期收集足夠證據獲得批准。
該公司表示,其GLP-1口服藥的減重效果可能不及其注射藥物Mounjaro——後者在GLP-1基礎上增加了第二種腸道激素GIP。
一項研究中,使用Mounjaro的患者減重最高達約22.5%。不過,若實驗性口服藥能達到純GLP-1注射藥物的效果,對部分患者而言仍不失為一種選擇。
輝瑞正在開發包括danuglipron在內的抗肥胖口服藥,今年早些時候報告的中期研究顯示其前景良好。
測試顯示,這類口服減肥藥與注射劑一樣會引發噁心等胃腸道副作用。製藥公司表示這些反應通常為輕至中度,且多發生在劑量增加階段。
更正與補充羅伯特·庫什納博士是西北大學範伯格醫學院的肥胖治療專家。本文早期版本錯誤地將他的名字寫為威廉。(已於6月25日更正)
聯繫彼得·洛夫特斯,郵箱:[email protected]
刊登於2023年6月26日印刷版,標題為《類似Ozempic的口服藥物正在研發中》。