全球首例!透析7年後,他移植了一顆豬腎_風聞
医学界-医学界官方账号-为你提供可靠、有价值的内容是我们的存在方式。44分钟前
“截至目前,異種器官移植的諸多關鍵性科學問題,還沒有得到完全解答。”
撰文丨凌駿、燕小六
當地時間3月21日,美國哈佛大學麻省總醫院醫療團隊宣佈,他們成功完成人類歷史上首例基因編輯豬腎的人類活體移植。
手術非常成功,根據報道,新的腎臟在移植後不久就可以產生尿液。醫生預計患者很快就可以出院,“為器官衰竭患者提供更容易獲得的移植器官,此次手術標誌着一個重要的里程碑。”麻省總醫院在一份聲明中表示。
據世界衞生組織統計,全球大約有120萬人需要腎臟移植,但每年僅有不到1/3的患者能等到合適的供體器官,其餘人只能接受腎臟透析等治療度過餘生。“我們希望這種新的移植方法,能夠給全球數百萬腎衰竭患者帶來新生。”麻省總醫院移植外科醫生Tatsuo Kawai博士表示。
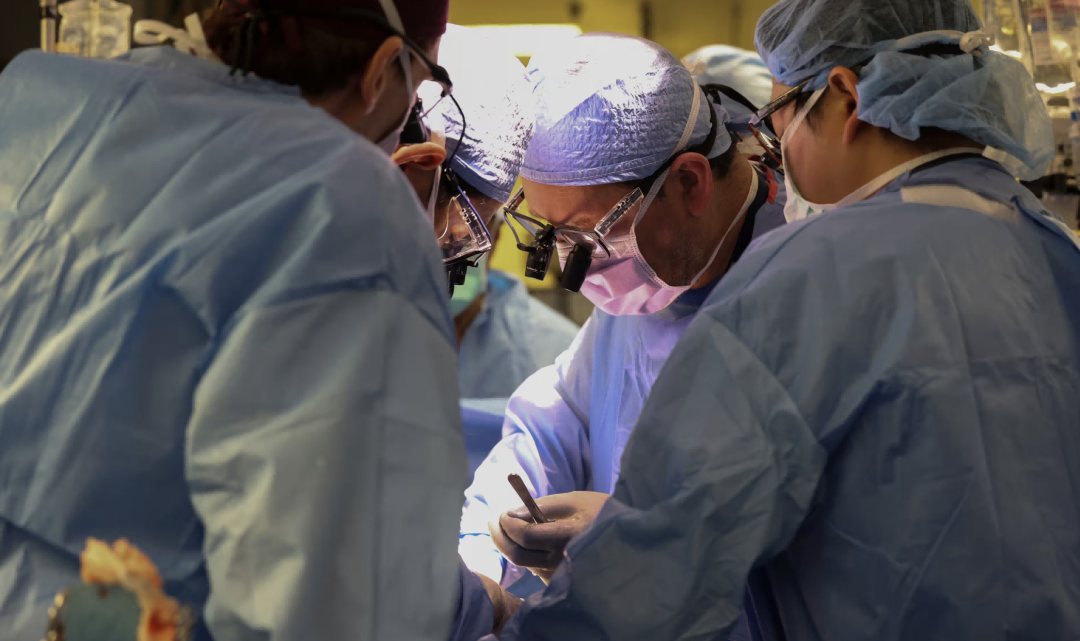
美國麻省總醫院,人類歷史上首例轉基因豬腎移植術
“最美麗的腎臟”
接受本次豬腎移植術的是62歲的Richard Slayman,一名來自美國馬薩諸塞州的腎病患者。
早在2010年左右,Slayman的腎臟就已經無法正常工作,由於沒有合適的腎移植機會,他不得不接受了長達7年的透析治療。一直到2018年,他終於等到了合適的供體和手術時機,成功接受了標準的腎移植流程。
好景不長,2023年,移植到他體內的新腎臟也出現了衰竭,當年5月Slayman又恢復了透析治療。但此時的他合併有高血壓、糖尿病等基礎疾病,透析過程中反覆出現血栓等嚴重併發症,需要每兩週去醫院進行一次解凝和手術修復。
在這樣的情況下,麻省總醫院的醫生團隊向Slayman提出了“豬腎移植”的方案。雖然有着諸多疑慮和擔心,但常年被疾病纏身的Slayman早已疲憊,他渴望迴歸正常生活,最終決定接受“豬腎移植”。
手術方案也順利通過了美國食品藥品監督管理局(FDA)“同情使用條款”的批准,這一條款允許對患有危及生命疾病的患者,提供可能獲益卻未經批准的治療方式。
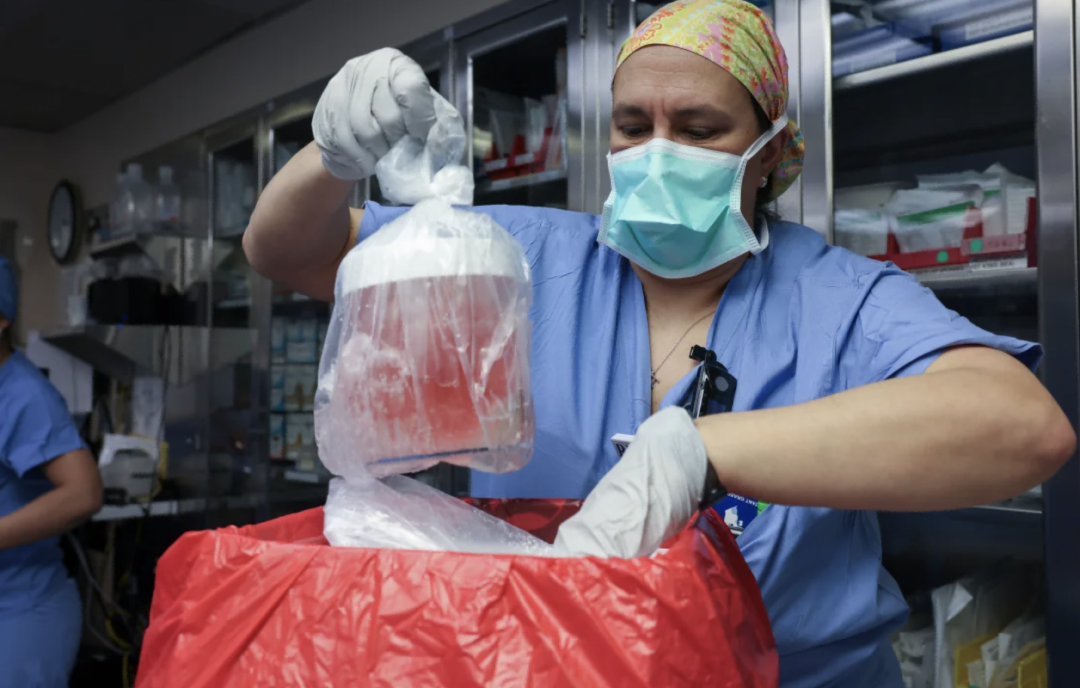
醫護團隊取出豬腎,準備開展移植手術
3月16日手術當天,麻省總醫院的外科醫生團隊將一個經多處基因編輯豬的腎,一點點地接入Slayman的循環系統。這並不是一件容易的事,由於有基礎疾病,Slayman的血管狀況並不理想。
“可當豬腎的血管和Slayman的血管完全吻合後,豬腎立即‘變成了粉紅色’,並開始產生尿液。”主刀醫生Tatsuo Kawai博士在本週四的新聞發佈會上稱,“這是我見過最美麗的腎臟,當時手術室中的15名移植團隊成員爆發出熱烈掌聲。”
相關的製藥公司也為Slayman提供了專門定製的抗排斥藥物,以防止豬器官導致的排斥反應。根據團隊介紹,Slayman在術後幾天就可以下地行走,截至目前免疫系統並未出現排斥狀況,血壓等指標和生命跡象穩定。“這一顆豬腎可以持續運作數年。”醫生團隊在新聞發佈會上大膽預測。
“我們希望有一天,腎透析將被淘汰。”麻省總醫院腎移植醫學科主任Leonardo Riella博士稱,“腎透析就像是呼吸衰竭患者的呼吸機。你可以使用它一段時間,但如果希望患者能迴歸正常生活,應該有一個更永久的解決方案,可能是人體移植或者異種移植。”
一顆基因編輯豬腎
“這位患者非常了不起,他具有‘科學奉獻精神’,我非常地尊敬他”。復旦大學上海醫學院副院長、上海市器官移植重點實驗室主任朱同玉教授告訴“醫學界”。
目前在全球異種大器官移植領域,進展最快的是豬心和豬腎移植。和心臟移植不同的是,儘管會導致生活不便,但腎透析是一種極為成熟的治療方式,可以延續腎衰竭患者的生命。對於Slayman來説,同意接受豬腎移植需要莫大的勇氣。
“他此前已經做過了一次腎移植,一側的血管通道用掉了。另一側用於本次異種器官移植,如果失敗,後續再做人源腎移植的機會渺茫。這個人應該被歷史記住。”朱同玉説。
這也不是科學家第一次嘗試在人體中進行豬腎移植,只是此前均是在腦死亡患者體內進行。過去幾年內,美國紐約大學已接連完成了3例腦死亡患者的豬腎移植,一例在最長61天的觀察期內,肌酐水平處於最佳範圍,豬腎具備一定的清除和藥物代謝能力,驗證了豬腎人體移植的可行性。
可腦死亡人體和“活人”終歸不同。朱同玉告訴“醫學界”,腦死亡人體和活體對異種器官的反應存在差別,大腦會分泌很多神經遞質、激素,對免疫系統形成壓制。在Slayman的手術中,科學家可以瞭解活體對異種器官的反應,獲得一系列真實世界數據,這為未來移植方案的進一步優化、改造奠定了基礎。
“但目前來看,Slayman後續的健康狀況還無法預估。”朱同玉稱,還需要評估一系列免疫學、微生物病毒學指標,監測移植豬腎的生理指標,觀察它能否滿足人體的生理需求。
“討論異種器官移植是否成功,標誌性節點是手術後的半年。這是一個非常關鍵的時間節點。”朱同玉説,“此時患者已度過超急性和急性排異期高發期,可以觀察到慢性排異等。其次在半年後,也基本能觀察到動物攜帶的病毒或基因序列,在人體內有沒有被激活,甚至導致發病。”
朱同玉所説的“動物病毒”,包括豬內源性逆轉錄病毒(PERV)、豬鉅細胞病毒以及我們一些未知的病毒等。
據瞭解,本次移植所用的豬經過了69處基因編輯,“其中的10處編輯是標準方案之一,包括敲除排斥反應相關基因,加入人補體抑制基因、抗凝基因等,目的是提高豬器官與人體的兼容性。”成都中科奧格生物創始人潘登科教授告訴“醫學界”,“其他的幾十處編輯,是為了消滅供體豬體內的豬內源性逆轉錄病毒等。”
“無內源性逆轉錄病毒PERV-C亞型豬種,目前國際上認為是相對安全的。”潘登科表示,他和團隊培育的基因工程醫用豬,是從源頭上篩選了無PERV-C的巴馬小型豬,並通過嚴格的無菌繁育、監測,目前已在國內完成了數十例異種器官移植動物實驗驗證,並於今年3月14日與西京醫院合作,完成了全球首例腦死亡患者的豬肝移植。
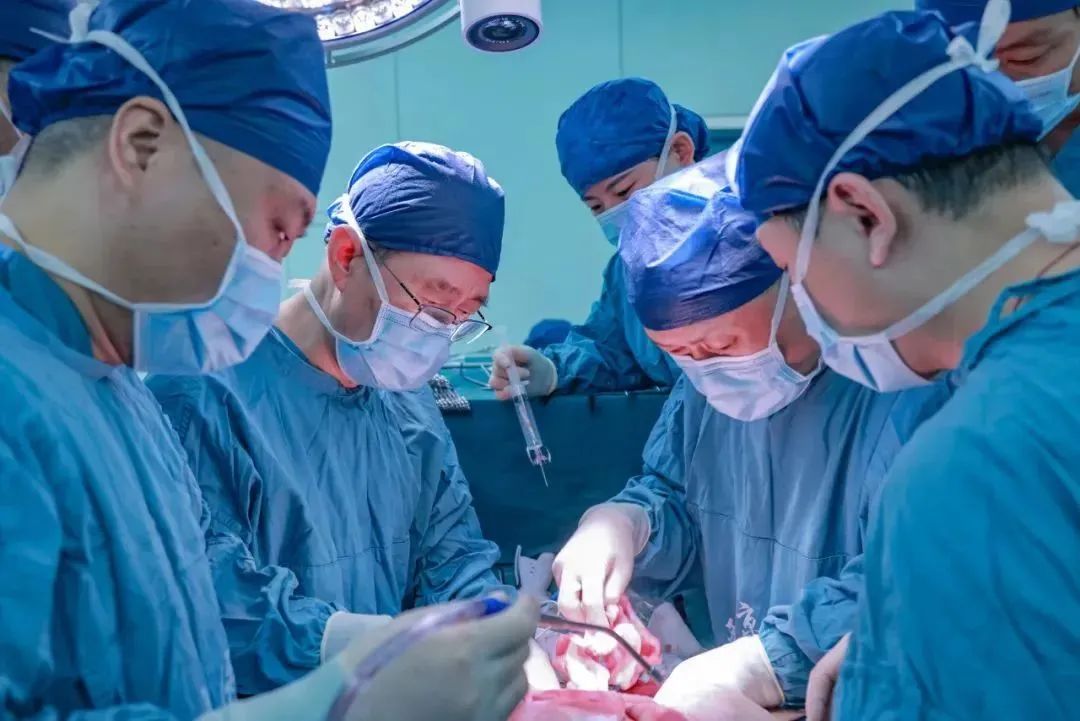
今年3月14日,西京醫院竇科峯院士團隊完成了全球首例腦死亡患者的豬肝移植
針對此次豬腎移植,朱同玉認為,嚴格意義上還未達到“突破”的程度,而是異種器官移植的又一進步和進展。“所謂‘突破’,是要從理論上解決重大問題。但截至目前,異種器官移植的諸多關鍵性科學問題,還沒有得到完全解答。”
麻省總醫院醫生團隊同樣在週四的發佈會上表示,儘管最新的進展很重要,但還需要更多的研究,最好是在不同醫院進行的大型研究,才能更好地瞭解豬腎移植的效果。
堪比“登月計劃”,
異種大器官移植即將開展臨牀試驗
此次的豬腎移植,是人類歷史上第三次嘗試在活人體內移植豬的器官。此前同樣基於“同情使用條款”,2022年1月7日和2023年9月20日,美國馬里蘭大學率先對兩名終末期心衰患者完成豬心臟移植,術後生存時間分別為2個月和6周。
目前,全球尚未有正式獲批臨牀試驗的異種大器官移植項目。根據美國監管機構的相關標準,正式獲批臨牀試驗,需要至少在連續6例的動物實驗中,4例存活時間達半年或一年以上。潘登科告訴“醫學界”,根據最新披露的信息,至少有2個達標的美國科研團隊或將於今年進行申報,有望在明年年底前正式獲批開展臨牀試驗。
朱同玉表示,雖然已經有3例活體移植,但距離異種移植真正走上臨牀,後續還有很多研究要推進。
在跨物種病毒傳播方面,此前在全球首例豬心移植患者的屍檢中,科學家發現了豬鉅細胞病毒存在的跡象。研究團隊推測,該病毒可能最早處於“潛伏”狀態,躲避了檢測,在患者減少抗病毒治療方案後被重新激活,引發了細胞損傷的炎症反應。不過,沒有確定證據表明該病毒感染了患者,或擴散到心臟以外的器官。

2022年1月,美國馬里蘭大學醫學中心宣佈,成功實施全球首例人移植轉基因豬心手術
朱同玉表示,“雖然科學家對於前期豬的培育、手術前的病毒檢測篩查等,目前已有很成熟的技術手段。但豬體內的病毒有很多種,是否還存在未知的病毒,移植後又會不會在人體內不同環境下被激活,目前還不清楚。”
另一方面,“供體豬需要經過基因編輯,但它和人的基因組差異畢竟不在一個數量級上,仍有可能存在排斥。過多的基因編輯也會使得豬本身難以存活。最終到底需要編輯豬的多少基因?編輯哪些基因?還要進一步的臨牀研究。”朱同玉説。
但無論如何,異種大器官移植研究已經進入了加速期,它為全球移植器官的短缺提供了一種極具想象力的解決方案:有一天,經過基因編輯的豬器官可能成為一種商品,讓無數在等待中的患者延續生命。
2022年6月,《新英格蘭醫學雜誌》在首例豬心移植病例報告的評論文章中寫道,無論這次異種移植是否開啓了新未來,研究都提供了一種新的觀察——研究人員利用基因生物工程和細胞發育生物學,迅速而深刻地解決醫學問題。
同時,隨着近年來新型免疫抑制劑的出現,異種移植免疫基礎研究的不斷深入,異種移植的免疫治療方案也越來越完善。“異種器官移植的臨牀轉化研究是一個系統工程,堪比‘登月計劃’,需要器官移植、基因工程、畜牧學、免疫學、倫理等各方面專家配合完成,已有的案例為我們提供了很好的借鑑。”潘登科説。
朱同玉表示,在正式開啓臨牀試驗前,醫學試驗不可能做到萬事俱備,答案還得在真實世界研究中尋找。“從近年來醫學科研領域的相關進展看出,一旦通過倫理學等嚴格審批程序,人類已經具備了探索的條件。”