藏在財報裏的秘密,君實生物的三張明牌_風聞
氨基观察-生物医药新时代的商业智库和价值灯塔1小时前
創新藥行業的寒冬並未過去,但變化在悄然發生。
2024年開年以來,國產創新藥license out進入新高潮。在這背後,是藥企新一代研發成果開始出現,創新藥新鮮血液的加速湧現。
而在財報季,我們更能看到,部分創新藥企研發、商業化環節已經打通,自我造血能力在不斷增強。不管是研發能力還是商業化能力,國內創新藥企都在持續證明自己。
可以預見,一些頭部創新藥企,接下來將會進入發展新階段。
一方面,這些藥企已經打開全球市場大門,國際化佈局預期兑現;另一方面,他們此前的研發積累,會隨着藥物獲批、新適應症上市,持續貢獻不菲的收入。
這些藥企往往又是國內創新實力最強的選手,隨着自我造血能力的大幅增強,他們將能夠擺脱週期的束縛,進入“現金流-創新”飛輪加速的階段。
日前公佈財報的君實生物,就在展示這樣的發展軌跡。
/ 01 / 國際敍事開啓
從模仿到創新,從國內走向世界舞台,每一步都佈滿了挑戰。然而,正是這些挑戰塑造了今天中國創新藥企的實力。
如今,談及中國創新藥企,我們不再將其視為“追隨者”,而是作為“並跑者”,甚至“先行者”和“探索者”,在某些領域取得突破,為全球患者帶來了新的治療方案。這正是君實生物所講述的故事。
作為首個登陸美國市場的國產PD-1,君實生物的特瑞普利單抗,快速放量已經是一張明牌。
首先,是獨家適應症帶來的明確預期。
去年,FDA批准特瑞普利單抗用於復發/轉移性鼻咽癌的全線(一、二線)治療,成為美國首個獲批鼻咽癌治療的免疫療法,填補美國市場空白。
除了適應症獨家外,特瑞普利單抗還具備極大臨牀優勢:其兩項臨牀研究POLARIS-02和JUPITER-02以極高的試驗標準取得了優異的數據結果,患者生存獲益顯著,獲得美國國家綜合癌症網絡(NCCN)指南的首選推薦。
這使得特瑞普利單抗在鼻咽癌治療領域具備獲得廣泛認可的基礎。在美國,醫生極其重視基於“數據”和“證據”的治療選擇。君實生物的合作方Coherus正在嘗試推動,讓特瑞普利單抗跨越患者的所有治療線。比如,剛剛接受二線化療的患者,也能夠立即獲得特瑞普利單抗。據Coherus透露,其在美國與主流醫生超50次會議的廣泛交流中,這一策略獲得了超過90%專家的支持。
按照Coherus預期,特瑞普利單抗在鼻咽癌全線治療的年銷售峯值大約會在2億美金左右。
其次,Coheurs對特瑞普利單抗的高度重視,增強了這一預期實現的確定性。
在年初,Coheurs完成了戰略轉型,將眼科產品出售,專注於腫瘤領域。在Coherus的新戰略中,特瑞普利單抗佔據了核心位置。根據Coherus表述:
其計劃專注於腫瘤微環境及與PD-1通路互補的高潛力產品線,特瑞普利單抗是與新型藥物聯合研究的支柱。
這意味着,Coherus將投入更多資源以發掘特瑞普利單抗的潛力。實際情況也證明了這一點。目前,Coherus已經在鼻咽癌領域找到了有效的市場策略——精準營銷。
具體來説,Coheurs部署了與鼻咽癌ICD-10(疾病分類)代碼相關的實時理賠系統和電子病歷數據源。藉助這些工具,一旦腫瘤醫生接觸到鼻咽癌患者,就會立即提醒公司的團隊進行跟進,隨後觸發兩個步驟:針對性地聯繫醫生/專家進行電話營銷,向該醫生投放高度針對性的品牌數字廣告。這種精準營銷策略已證明非常有效,貢獻了超過60%的新增訂購賬户。
據Coherus統計,自上市以來,已有59個診所和醫院賬户訂購了特瑞普利單抗。在NCCN指定的33個癌症中心中,55%已經將特瑞普利單抗加入其處方列表,其餘則在進行P&T(藥學和治療)審查。
 照這個勢頭,特瑞普利單抗在鼻咽癌適應症上達到銷售峯值的時間預計不會太長。根據Coheurs的預測,實現這一目標可能只需大約2-3年。
照這個勢頭,特瑞普利單抗在鼻咽癌適應症上達到銷售峯值的時間預計不會太長。根據Coheurs的預測,實現這一目標可能只需大約2-3年。
當然,特瑞普利單抗在美國市場的潛力,遠不止於鼻咽癌適應症。
上文提及,Coheurs將特瑞普利單抗視為戰略重心。根據財報,Coherus圍繞特瑞普利單抗的聯合療法探索,具有兩個特點:
一方面,適應症覆蓋範圍廣,包括肝癌、肺癌,甚至是PD-1耐藥的腫瘤患者;另一方面,則是探索範圍廣,聯用組合包括DNA疫苗等前沿療法,意味着後續的競爭力可能更強。
特瑞普利單抗聯合療法的推進大概率也會超預期。在電話會議中,Coheurs表示在今年就會啓動特瑞普利單抗和貝伐珠單抗、IL-27拮抗劑casdozokitug開展肝癌一線療法的研究。
從策略來看,Coheurs追求的不僅是藥物的協同,還包括癌種的協同。日前,Coheurs與INOVIO達成的合作,就是這樣一個例子。雙方將開展INO-3112(靶向HPV 16/18的DNA癌症疫苗)與特瑞普利單抗聯合療法的探索,適應症是局部晚期頭頸部鱗狀細胞癌,與鼻咽癌具有顯著的協同效應,因為兩者都屬於“頭頸部腫瘤”大類範疇,在科室層面不分家。
總體而言,特瑞普利單抗美國市場的發展邏輯極為清晰:從鼻咽癌快速出圈,再到覆蓋更多適應症的聯合療法不斷突圍。
這意味着,美國市場能為君實生物帶來不菲收入。按照Coheursu預期,到2032年特瑞普利單抗銷售額有望逼近20億美金。根據合作條款,君實生物能夠享有美國市場銷售淨利潤的兩位數分成。
而實際上,美國市場只是特瑞普利單抗國際佈局的一個起點。君實生物還在同步加速進軍東南亞、中東、北非、歐洲等海外市場。
目前,與合作伙伴一同,君實生物已在50多個國家或地區鋪建商業化網絡,並陸續啓動了上市註冊工作。目前,特瑞普利單抗已在歐盟、英國、澳大利亞、新加坡、印度、南非、智利、約旦等國家和地區提交了多項適應症的上市申請,其中歐盟已完成對生產現場的GMP核查。
特瑞普利單抗獲FDA批准後,後續在海外其他國家和地區的註冊進程加快是大概率事件。
一方面,可以通過一些合作框架走特殊通道。比如,特瑞普利單抗作為第一個加入奧比斯項目(Project Orbis)的國產創新藥,有望在澳大利亞、新加坡等多個國家加速上市進程;另一方面,FDA批准之後,在一些非ICH國家(比如中南亞、中東等)也可以簡化流程,只做行政審評。
不難預見,未來兩年,特瑞普利單抗海外里程碑將會密集到來。
隨着這一系列戰略佈局陸續落地,君實生物在國際市場上的競爭力和影響力會逐漸展露。
除特瑞普利單抗外,君實生物還有另一張“隱藏王牌”,BTLA單抗tifcemalimab。
目前,tifcemalimab已啓動兩項III期註冊臨牀:一項是tifcemalimab聯合特瑞普利單抗用於治療侷限期小細胞肺癌(LS-SCLC),正在開展國際多中心III期臨牀,已完成中、美、歐三地的首例患者入組及給藥;另一項是tifcemalimab聯合特瑞普利單抗用於治療經典型霍奇金淋巴瘤(cHL),即覆蓋了實體瘤和血液瘤。
另外還有多項tifcemalimab聯合特瑞普利單抗的Ib/II期臨牀研究正在中國和美國同步開展中。特瑞普利單抗和BTLA單抗這對王牌組合,未來有望聯合解鎖更多瘤種的應用,為國際業務的擴展奠定基礎。
/ 02 / 商業化增長預期兑現
先研發後變現的發展模式,決定了創新藥企在豐收之前,可能要面對長時間的孤獨和等待;但一旦戰略佈局成熟,步入收穫季節,便是連綿不絕的爆發之時。
君實生物的崛起印證了這一點。
作為國內創新藥行業的先行者,君實生物在靶點、疾病適應症的佈局上始終保持着前瞻性,靜默耕耘織就了一張增長之網。
截至目前,君實生物在國內已經有3款創新藥進入商業化階段,分別為:特瑞普利單抗、新冠口服藥民得維、阿達木單抗類似藥君邁康。3款商業化產品驅動君實生物收入持續增長。2023年,君實生物來自藥品的收入同比增長58%。其中,特瑞普利單抗銷售收入9.19億元,同比增長25%。
在腫瘤和自免領域之外,君實生物在心腦血管領域的佈局也即將迎來首個商業化產品:昂戈瑞西單抗(PCSK9)預計在2024年上市。
未來新藥物、新適應症的持續獲批,保證了君實生物未來業績增長的可持續性。
以PD-1特瑞普利單抗為例。截至目前,特瑞普利單抗在全球開展了超過40多項由公司發起的臨牀研究。接下來,特瑞普利單抗將會進入有節奏的收穫階段:每年有新適應症逐步上市、進入醫保。
2023年,特瑞普利單抗3項適應症(1LnsqNSCLC、NPC、ESCC)入圍醫保;2024年,仍是特瑞普利單抗的密集收穫期,特瑞普利單抗聯合化療用於可手術NSCLC圍手術期治療的適應症已獲NMPA批准,另外還有用於晚期三陰性乳腺癌、晚期腎細胞癌一線治療、廣泛期小細胞肺癌一線治療等新適應症的上市申請已獲NMPA受理。
由於君實生物在以上多個適應症均進度領先,且此類適應症用藥週期較長,未來其在市場推廣中有望取得先發優勢。例如,圍手術期NSCLC適應症具有覆蓋範圍廣,“首個+唯一”的特點。
圍手術期指術前新輔助和術後輔助階段,覆蓋癌症II期或III期癌症患者。太平洋研報數據顯示,在NSCLC領域,大約40%患者在確診時,處於上述階段。II期或III期患者通常可以手術切除,但30-55%患者面臨復發,傳統的術前新輔助或術後輔助化療僅提升5年OS率約5%,免疫治療的加入帶來了治療革新。目前,國內圍手術NSCLC領域,獲批的僅有特瑞普利單抗。
實際上,不僅是圍手術期NSCLC,今年特瑞普利單抗還有望獲批的適應症中,包括一線TNBC、一線RCC都具有“獨家”特點。
並不意外。**一直以來,在管線佈局方面,君實生物追求的不僅是數量上的增加,更注重的是深度。**例如,特瑞普利單抗除了圍繞一線療法展開佈局外,還前瞻預判了免疫2.0時代的發展趨勢,順勢完成卡位。
一方面,在輔助/新輔助治療領域,君實生物處於全球第一梯隊、國內遙遙領先的位置。
上文提及,特瑞普利單抗聯合化療用於可手術NSCLC圍手術期治療的適應症已獲NMPA批准,是率先突破該適應症的國產PD-1。
這只是開始。在術後輔助和圍手術期領域,特瑞普利單抗還覆蓋了胃癌、肝癌、食管癌等國內高發癌種,公司預計食管鱗癌圍術期研究將會在2024年讀出數據。
另一方面,在與免疫療法、ADC、抗血管生成藥物等諸多前沿領域的聯合療法探索中,君實生物同樣基於差異化理念,通過自有搭建的管線和廣泛合作具備全球競爭力。
 因此,隨着這些新藥物、新適應症的持續上市,君實生物的收入將會持續增厚。
因此,隨着這些新藥物、新適應症的持續上市,君實生物的收入將會持續增厚。
/ 03 / “現金流-創新”飛輪加速
一家創新藥企的崛起,並非源於某種神秘力量,而是源自不懈的努力和持續的積累。説白了,成功是努力的積累,不是偶然。
君實生物的成長故事也是如此。我們能夠看到,君實生物發展提速背後,在於其各個環節能力的持續提升。
隨着鄒建軍博士等行業頂尖好手的加入,君實生物的執行效率在大幅提升。2023年,君實生物在全球範圍內,有6項NDA獲得監管機構受理,是數量最多的創新藥企之一。
在商業化方面,君實生物也是繼續加速度。截至報告期末,特瑞普利單抗已累計在全國超過五千家醫療機構及約兩千家專業藥房及社會藥房銷售。
可以預見的是,君實生物銷售效率將會持續改善。畢竟,銷售團隊的擴張規模是可控的,隨着銷售額的攀升,人均產能將會顯著增加,推動君實生物更快走向盈虧平衡點。
而隨着君實生物具備更強的造血能力,也將進入“現金流-創新”飛輪加速的發展新週期。
在研發儲備方面,君實生物已經成功打造了7個技術平台,包括單抗、雙抗、ADC、siRNA等。由於這些這些平台均具有一定特色,未來君實有能力依託這些平台在多個前沿領域構築具有全球競爭力的管線。
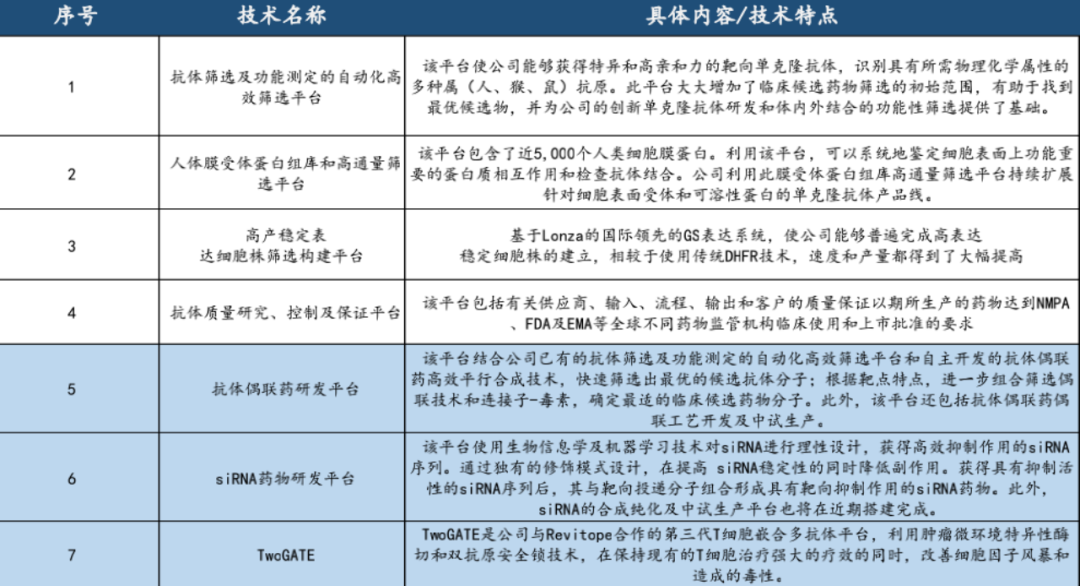 例如,在siRNA領域,君實生物的技術平台具備提高siRNA穩定性、降低副作用以及高效等特點。因此,其ANGPTL3靶點能夠快速展露頭角。JS401是基於公司siRNA平台開發的 ANGPTL3 siRNA 藥物,目前已經進入臨牀1期階段。在同靶點、同機制領域,JS401的進度處於國內第一,全球前三。
例如,在siRNA領域,君實生物的技術平台具備提高siRNA穩定性、降低副作用以及高效等特點。因此,其ANGPTL3靶點能夠快速展露頭角。JS401是基於公司siRNA平台開發的 ANGPTL3 siRNA 藥物,目前已經進入臨牀1期階段。在同靶點、同機制領域,JS401的進度處於國內第一,全球前三。
當然,對於創新藥企來説,能否快速推動核心管線向前,除了能力之外,資金等資源也不可或缺。自我造血能力不斷增強的君實生物將加速走入正循環:“特瑞普利單抗等商業化管線帶來豐厚的現金流反哺創新,創新成果增厚現金流,現金流繼續加速創新成果兑現”的飛輪加速的過程。
