久坐可能影響免疫力?美國國立衞生研究院:健康老年人和病人差不多!_風聞
时光派-时光派官方账号-聚集全球前沿、全面、专业抗衰资讯2小时前

“身體感覺xxx,可能是得了這種病。”
如果要問起現代人最關心的話題,除了名人八卦,當居前列的肯定非上面這類**“健康危機”**莫屬。我們幾乎每天都在經受着各種各樣的疾病威脅,導致長壽之路上關隘重重,如果想要安然度過,健康、良好的免疫功能必不可少。

圖注:隨便一搜,連續三條都是類似的熱點
這也使得一套能夠準確評估機體免疫功能水平的工具成為了必要,為此,科學家們前仆後繼,期望能夠找到“完美答案”。而現在,希望落到了美國國立衞生研究院終身高級研究員、現任耶魯大學免疫生物學教授John S. Tsang身上。
在近期發表於nature雜誌子刊nature medicine的論文中,他的研究團隊提出了一款免疫健康指標(IHM)。利用這款全新的指標,他們不僅發現了健康老年人羣潛在的免疫力下降危機,還成功對多個疾病的治療預後進行了預測,甚至大膽將其稱作“免疫健康的統一指標” [1]。

圖注:這篇文章的標題“人類免疫健康的統一指標”屬實抓人
這究竟是在吹牛,還是強者從不作偽,果真如他號稱得那般🐂🍺?一起往下看。

事實上,科學家們此前已經推出了多款用於評估免疫功能的指標,諸如C反應蛋白(CRP)、紅細胞沉降率(ESR)、自然殺傷(NK)細胞活性等,但它們均存在一個普遍問題:它們在處於病理狀態的機體內檢測效果比較好,卻無法反映健康人體的免疫功能差異,此外它們都只和免疫狀態的某一方面改變有關,無法反映整體。
當然,其中也有佼佼者。此前發佈的一篇推文中,派派報道了由德克薩斯大學的Sunil K. Ahuja教授提出的一項概念:免疫彈性(immune resilience,IR)。
簡單來説,在面對疾病、感染等健康威脅時,**免疫彈性更好的人能夠更快激活免疫系統,識別並消除威脅,並在威脅消除後快速恢復到正常狀態,**避免形成慢性炎症,引發衰老 [2]。

圖注:免疫彈性的發現當時被髮表在了nature雜誌的另一本子刊上 [2]
推薦閲讀:免疫就像橡皮筋,彈性越好越強勁。Nature子刊:免疫彈性與生存率及壽命高度相關!
雖然誕生才不到一年,免疫彈性這一概念已經收穫了科學家們的青睞,被多篇發表於《柳葉刀》等高影響因子雜誌的論文引用,並被提議作為評估免疫健康的指標之一 [3, 4]。

當然,免疫彈性也並非白玉無瑕,其目前也存在一些不足。本文的作者John S. Tsang就指出,**目前仍然沒有一項特定的分子途徑(例如mTOR和AMPK)可以用於對免疫彈性進行直接定義,**因而也無法研究其如何受到遺傳、環境和生活方式等因素的影響。
打個比方,王叔叔和王阿姨現在都是健健康康的狀態,從以上指標來看似乎並沒有什麼差異,但當一陣流感襲來,王阿姨流了幾天鼻涕就恢復如初,出門跳廣場舞去了,王叔叔卻一病不起,咳啊咳咳了一個月沒好,這種差異到底是出於什麼原因呢?

圖注:到底是啥導致王阿姨(左)和王叔叔在同一場流感之後出現這麼大的差異呢?
免疫彈性或許會説是他們的彈性不同,但為什麼彈性不同呢?我們還是不知道。
為了把這些問題理清楚,John S. Tsang教授和他的研究團隊開啓了他們的探索。
圖注:John S. Tsang教授的社交媒體首頁
**(**有關免疫功能的檢測一直都是一大研究熱點,除了免疫彈性外,還有許多其他指標粉墨登場,點擊下方卡片,關注時光派並後台回覆免疫指標,了****解更多免疫功能檢測手段)

研究團隊一共納入了228名單基因免疫疾病患者(涵蓋了22種單基因免疫疾病)。通過分析這些患者的單個基因突變與他們表現出來的免疫功能差異,並綜合考慮突變基因調控的下游通路,研究團隊能夠快速篩選出一批**與免疫能力直接關聯的參數,**這也為後續的深入探索打下了堅實的基礎 [5-7]。
在機器學習技術的幫助下,研究團隊很快就根據這些數據得到了一套新的模型:jPC1,它可以捕捉免疫和健康相關功能的狀態變化,例如健康受試者的jPC1評分就明顯高於單基因免疫疾病的患者。
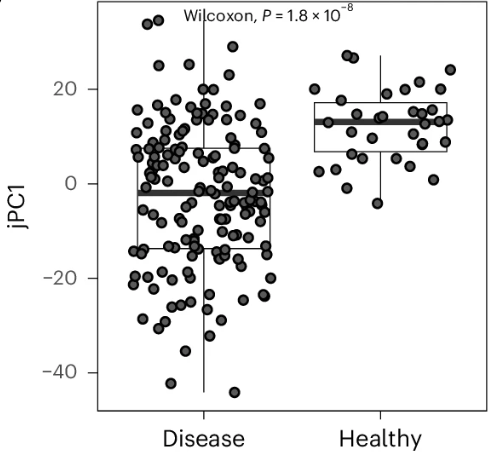
圖注:事實上,不管是健康組(右)還是疾病組,組內個體間的jPC1差異都很大,但總體來看健康組的jPC1得分要更高
jPC1是在研究團隊沒有對數據做任何額外處理的情況下由AI自動挖掘出的模型,就能有如此明顯的區分效果,那如果再加上人類的指導呢?
在接下來的實驗中,研究團隊首先將來自不同人羣的受試者數據進行了分組標註,然後讓AI去分析每個參數與免疫系統健康水平的聯繫,最終建立了一個新的模型,這個模型能夠直接計算每個人免疫系統健康的概率,而這個概率就是他們的免疫健康指標(IHM)分數。
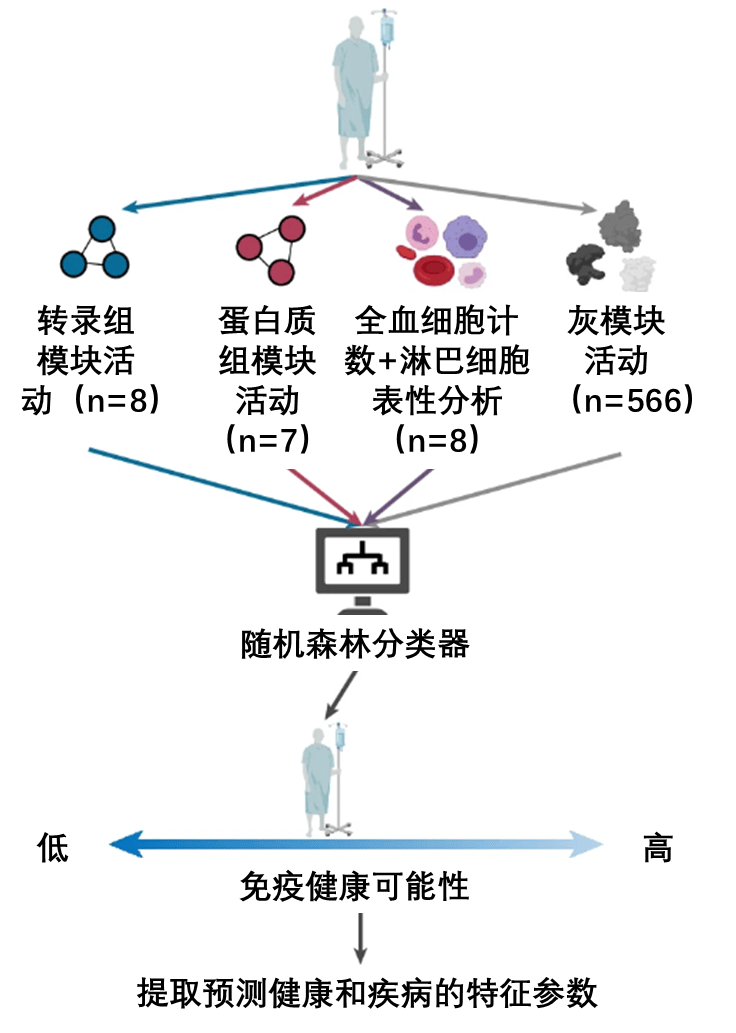
圖注:IHM的大致設計思路
舉個例子,假設你的IHM分數是80,那可能你的免疫系統功能目前感覺不錯,但仍然有20%的概率在未來出現問題,而這個概率在傳統的醫學檢查中可能是無法發現,這也正是IHM的領先之處。
IHM最主要的預測參數包含以下幾個:
1)紅細胞分佈寬度 (RDW)
研究表明,炎症會影響紅細胞的生成和成熟,導致出現大小和形狀千奇百怪的“畸形”紅細胞,紅細胞分佈寬度上升,因此RDW的快速升高可能預示着炎症的出現 [8, 9]。
圖注:一般來説紅細胞的體積和形狀都差不多,而病理狀態下就會變得千奇百怪
2)炎症相關參數(唾液酸粘附素、C 反應蛋白 (CRP))
唾液酸黏附素在機體中負責抑制免疫細胞的過度活化和炎症反應,維持免疫穩態,因此唾液黏附素水平升高意味着炎症反應的出現或加劇。
而C反應蛋白則是炎症反應的經典標誌物之一,在慢性炎症患者中,也能觀察到持續升高的C反應蛋白水平 [10]。
3)髓細胞/巨噬細胞信號 (MIP-1α、LD78β)
MIP-1α和LD78β都是由激活的巨噬細胞等免疫細胞分泌的因子,在體內主要負責吸引免疫細胞向炎症部位遷移,加速炎症消除,其水平升高與急性和慢性炎症狀態有關。此外,這兩種物質也和病毒等感染的免疫防護有關 [11]。
4)循環自然殺傷(NK)細胞水平
循環NK細胞是先天免疫系統的關鍵組成部分,主要功能是識別和摧毀被病毒感染的細胞以及腫瘤細胞,在臨牀中被用來診斷和檢測各種感染性疾病、自身免疫疾病、免疫缺陷和腫瘤,其水平降低往往和免疫功能障礙相關,會導致機體的炎症調控能力下降,炎症水平增加 [12]。
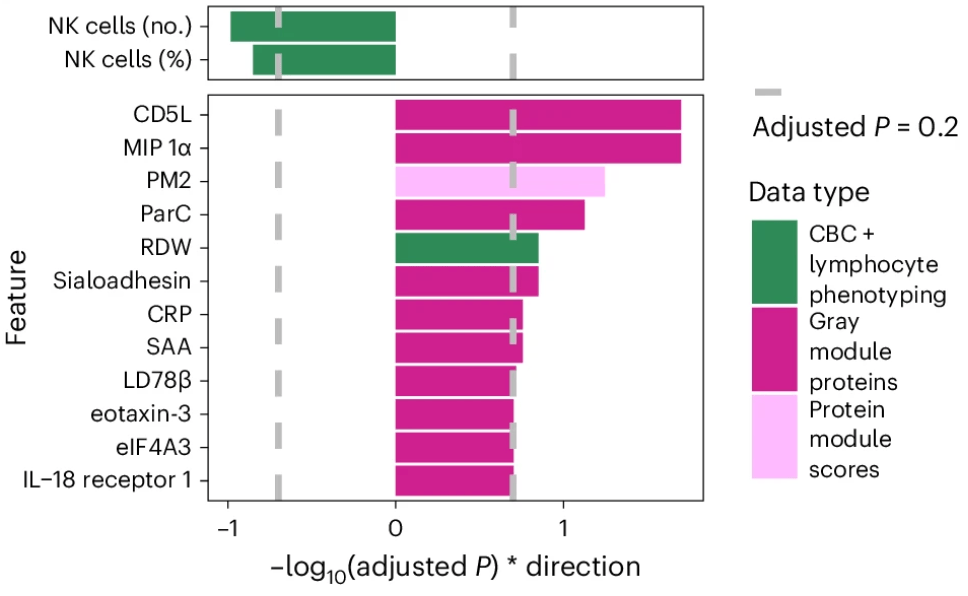
圖注:不同參數與免疫健康狀態的相關性不同,因此在模型中也被賦予了不同的佔比

進一步的分析顯示,**在健康的受試者中,IHM評分與年齡呈現負面相關,**這與老年人免疫系統功能更差這一普遍共識保持了一致 [13],這一發現在另一項獨立研究的數據(巴爾的摩衰老研究)中也得到了證實 [14]。
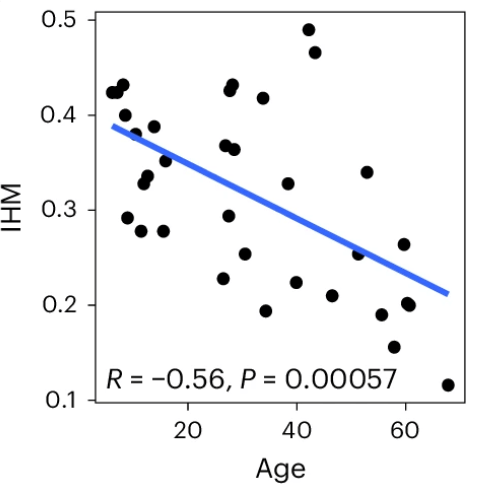
圖注:隨着年齡增長,IHM得分出現了顯著下降
而更為有趣的是,**那些老年的健康受試者的IHM評分居然和單基因免疫疾病患者的評分相似,**這是否意味着儘管他們看起來健康,實際上已經處在了免疫系統崩潰的邊緣呢?看來加強老年人對感染和炎症的防護果真是十分必要的。
當研究團隊將IHM與另一款免疫衰老評分IMM-AGE [15]進行比較時,他們又收穫了兩個喜人的發現。

圖注:IMM-AGE由斯坦福大學教授Mark M. Davis等於2019年提出,同樣發表於nature medicine雜誌 [15]
一方面,IHM和IMM-AGE在健康參與者和患者中的評分表現出了高度的相關性,對此作者猜測,這可能是因為兩者的評分機制利用了共同的免疫與衰老信號通路。而IMM-AGE自2019年被提出後,已經被應用於創傷患者、COVID-19患者、健康老年人等多個人羣的免疫衰老檢測 [16-18],其升級版本iAGE炎症衰老時鐘更是能提前7年預測老年衰弱 [19]。
推薦閲讀:前沿|比常人年輕40歲,只因控制炎症?免疫系統衰老,可能決定你的壽命!全新炎症衰老時鐘問世!
如今IHM的評分機制向它“看齊”,倒是有一種“英雄所見略同”的感覺。
不過,當用於區分健康人羣和單基因免疫疾病患者時,IHM的表現卻要比IMM-AGE更好,甚至在去除年齡因素之後,其表現依舊不凡,這一結果在多達10個與自身免疫/炎症性疾病相關的獨立人類數據集均得到了驗證 [20, 21],如此看來,IHM的這種強大區分能力似乎捕捉到了超乎衰老影響之外的、與免疫功能更加直接相關的因素。
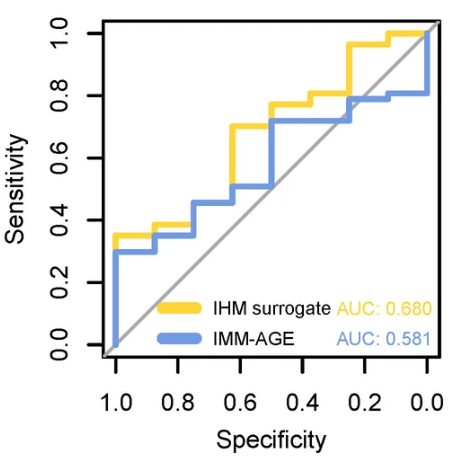
圖注:如圖,對於健康人羣和疾病患者,IHM和IMM-AGE的評分曲線幾乎一致,但總體來看IHM的AUC值更高,表明其分類性能更優
除此之外,研究團隊還發現了IHM的“預言能力”:對於同一類型疾病的患者,**IHM評分越低,疾病進展越快,**反之亦然,即使是號稱最為變幻莫測的系統性紅斑狼瘡也不例外。而對於那些正在接受治療的患者,較高的IHM評分也往往是更好治療效果的“預言”。

進一步的研究則發現,IHM在健康人羣中也具備一定的預測能力。那些**IHM評分更高的老年人在接種疫苗後免疫系統的應答也會更加積極,免疫功能被有效激活,**這倒是和IHM的本質:免疫功能評估相符。
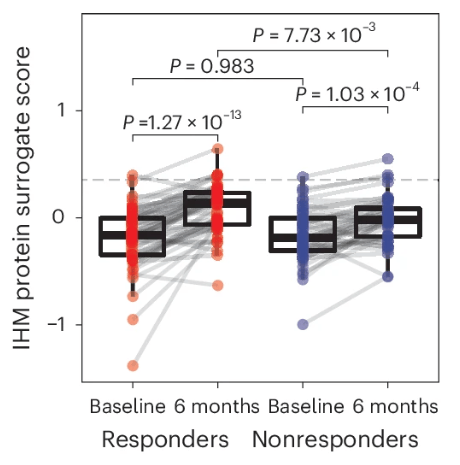
圖注:接種疫苗後免疫系統積極應答的人羣不管是在初始水平還是6個月後,都比沒有應答的人羣的IHM得分更高
最後還有一個讓人頗感意外的發現,數據表明**IHM得分和久坐成年人的BMI也呈現負相關,**這或許也暗示了我們長期久坐對包括免疫系統在內的機體全方面損害,這不禁讓派派期待起後面科學家們的詳細解釋了。
時光派點評
長久以來,免疫功能的系統性檢測都是派派十分關注的話題,我們也很有幸在去年追蹤到了Ahuja教授有關免疫彈性的發現,並及時進行了報道。
本文的作者John S. Tsang曾是美國國立衞生研究院的終身高級研究員,目前是耶魯大學免疫生物學和生物醫學工程教授,他的研究始終圍繞着**“為什麼免疫系統狀態和對干擾(例如疫苗、病毒感染和疾病)的反應在人類羣體中存在很大差異”**這一話題展開,曾獲得包括NIH/NIAID功績獎在內的多項獎項。
John S. Tsang教授研究團隊的這篇論文對於派派來説完全是意外之喜,它從另一個角度給出了同樣滿足期待的答案:直接從基因這一根源出發,以因果關係為絲線,編織出了一條“蜘蛛網”:一切觸碰蛛網的小蟲(感染、炎症),都會被檢測到。唯一讓派派感到可惜的是,研究團隊並沒有挖掘外部因素對IHM的影響,大概是留到今後的文章中繼續報道吧。
“這是免疫健康的冰山一角。免疫系統可以通過無數種方式和維度來感知和應對健康和穩態設定點的偏差,這令人興奮,值得用新技術、新概念、AI、免疫學等進行探索”,John S. Tsang教授在社交媒體上興奮地説道。

圖注:在X上,John S. Tsang教授用了一個長達12段的置頂帖子表達了對於完成本次研究的喜悦之情
這大概也就是科學的魅力,永遠在前進,永遠不會是一個人的孤獨旅程。
關注我們
參考文獻
[1]Sparks, R., et al., A unified metric of human immune health. Nature Medicine, 2024: p. 1-12.
[2]Ahuja, S.K., et al., Immune resilience despite inflammatory stress promotes longevity and favorable health outcomes including resistance to infection. Nature communications, 2023. 14(1): p. 3286.
[3]Ferrucci, L., et al., Enabling translational geroscience by broadening the scope of geriatric care. Aging Cell, 2024. 23(1): p. e14034.
[4]Shankar-Hari, M., et al., Reframing sepsis immunobiology for translation: towards informative subtyping and targeted immunomodulatory therapies. The Lancet Respiratory Medicine, 2024. 12(4): p. 323-336.
[5]Casanova, J.-L., S.M. Holland, and L.D. Notarangelo, Inborn errors of human JAKs and STATs. Immunity, 2012. 36(4): p. 515-528.
[6]Leonard, W.J., J.-X. Lin, and J.J. O’Shea, The γc family of cytokines: basic biology to therapeutic ramifications. Immunity, 2019. 50(4): p. 832-850.
[7]Manthiram, K., et al., The monogenic autoinflammatory diseases define new pathways in human innate immunity and inflammation. Nature immunology, 2017. 18(8): p. 832-842.
[8]Vayá, A., et al., Influence of inflammatory and lipidic parameters on red blood cell distribution width in a healthy population. Clinical hemorheology and microcirculation, 2015. 59(4): p. 379-385.
[9]Lippi, G., et al., Relation between red blood cell distribution width and inflammatory biomarkers in a large cohort of unselected outpatients. Archives of pathology & laboratory medicine, 2009. 133(4): p. 628-632.
[10]Sproston, N.R. and J.J. Ashworth, Role of C-reactive protein at sites of inflammation and infection. Frontiers in immunology, 2018. 9: p. 754.
[11]Cook, D.N., et al., Requirement of MIP-1α for an inflammatory response to viral infection. Science, 1995. 269(5230): p. 1583-1585.
[12]Tosello-Trampont, A., et al., Immunoregulatory role of NK cells in tissue inflammation and regeneration. Frontiers in immunology, 2017. 8: p. 301.
[13]Nikolich-Žugich, J., The twilight of immunity: emerging concepts in aging of the immune system. Nature immunology, 2018. 19(1): p. 10-19.
[14]Tanaka, T., et al., Plasma proteomic signature of age in healthy humans. Aging cell, 2018. 17(5): p. e12799.
[15]Alpert, A., et al., A clinically meaningful metric of immune age derived from high-dimensional longitudinal monitoring. Nature medicine, 2019. 25(3): p. 487-495.
[16]Conway, J., A. Acharjee, and N.A. Duggal, Integrated analysis revealing novel associations between dietary patterns and the immune system in older adults. Integrative Biology, 2024. 16: p. zyae010.
[17]Lord, J.M., et al., Accelerated immune ageing is associated with COVID-19 disease severity. Immunity & Ageing, 2024. 21(1): p. 6.
[18]Foster, M.A., et al., Investigating the potential of a prematurely aged immune phenotype in severely injured patients as predictor of risk of sepsis. Immunity & Ageing, 2022. 19(1): p. 60.
[19]Sayed, N., et al., An inflammatory aging clock (iAge) based on deep learning tracks multimorbidity, immunosenescence, frailty and cardiovascular aging. Nature aging, 2021. 1(7): p. 598-615.
[20]Shah, N., et al., A crowdsourcing approach for reusing and meta-analyzing gene expression data. Nature Biotechnology, 2016. 34(8): p. 803-806.
[21]Lau, W.W., et al., Meta-analysis of crowdsourced data compendia suggests pan-disease transcriptional signatures of autoimmunity. F1000Research, 2016. 5.