發現40赫茲的閃光可以促進睡眠及具有緩解腦部疾病的轉化潛力_風聞
葆力医学观察-专注生物科研领域,趣味科普与行业干货齐飞1小时前
腦膠質淋巴-淋巴系統(glymphatic-lymphatic system)定義腦實質中的腦脊液流動並消除代謝廢物,因此越來越被認為是腦環境穩態的基礎。動物和人體研究已經發現了調節腦膠質淋巴系統的幾個重要生理因素,包括睡眠、水通道蛋白-4和血流動力學因素。然而,對腦膠質淋巴系統調節的理解是有限的,這阻礙了以腦膠質淋巴為基礎的治療衰老和神經退行性疾病的發展。
2024年8月6日,温州醫科大學陳江帆團隊在Cell Discovery 在線發表題為”40 Hz light flickering facilitates the glymphatic flow via adenosine signaling in mice“的研究論文,該研究從熒光示蹤、雙光子記錄和動態對比增強磁共振成像分析中得到證據,表明40 Hz閃光增強了獨立於麻醉和睡眠的腦膠質淋巴內流和外排,這種效應歸因於星形膠質細胞水通道蛋白-4極化增加和血管舒縮(vasomotion)增強。
腺苷-A2A受體(A2AR)信號作為40 Hz閃光誘導的腦膠質淋巴流動增強的神經化學基礎出現,其基礎是腦液腺苷水平的增加,通過平衡核苷酸轉運體-2或A2AR的藥理學或遺傳失活,以及通過星形膠質細胞中A2AR -水通道蛋白-4的物理和功能相互作用來消除增強的腦膠質淋巴流動。這些發現確立了40hz閃光作為一種新的非侵入性增強腦膠質淋巴流動策略,具有緩解腦部疾病的轉化潛力。
另外,2024年2月8日,温州醫科大學陳江帆、瞿佳、蔡曉紅及澳門科技大學張康共同通訊在Cell Research 在線發表題為”40 Hz light flickering promotes sleep through cortical adenosine signaling“的研究論文,該研究證明了光閃爍觸發初級視覺皮層(V1)和其他大腦區域的細胞外腺苷水平立即持續增加(閃爍後長達3小時),作為光頻率和強度的函數,在40 Hz頻率和4000 lux時觀察到最大的影響。該研究發現皮質(穀氨酸能和GABA能)神經元,而不是星形膠質細胞,是細胞來源,細胞內腺苷的產生來自AMPK相關的能量代謝途徑(但不是SAM-轉甲基化或補救性嘌呤途徑),以及由平衡核苷轉運體-2 (ENT2)介導的腺苷外排是負責細胞外腺苷產生的分子途徑。重要的是,40Hz(而不是20和80Hz)閃爍30分鐘的光增強了小鼠的非快速眼動(non-REM)和2-3小時的快速眼動睡眠。通過切除V1(但不包括上丘)神經元和基因刪除編碼ENT2(但不包括ENT1)的基因,這種致睡效應被消除,但通過化學發生抑制V1神經元和以劑量依賴的方式將腺苷局部輸注到V1中重新獲得。最後,40 Hz閃爍30分鐘也能通過減少睡眠發作潛伏期、增加總睡眠時間和減少睡眠發作後醒來時間來促進失眠症兒童的睡眠。總的來説,該研究結果確定了V1中ENT2介導的腺苷信號是40Hz閃爍誘發睡眠的神經化學基礎,並揭示了一種新的非侵入性治療失眠的方法,這種疾病影響着世界上20%的人口。

腦膠質淋巴-淋巴系統定義腦實質中的腦脊液(CSF)流動並消除代謝廢物,因此越來越被認為是腦環境穩態的基礎。腦膠質淋巴系統包括腦脊液通過搏動動脈活動沿血管周圍間隙流入腦實質,腦脊液-間質液(ISF)通過星形細胞終足的水通道aquaporin-4 (AQP4)的極化分佈交換,隨後腦脊液和細胞外廢物通過淋巴系統排出。腦膠質淋巴系統清除主要在睡眠時活躍,隨着年齡的增長,其功能紊亂或下降,導致tau β-澱粉樣蛋白、α-突觸核蛋白等致病性蛋白在大腦中積累。睡眠、衰老、腦膠質淋巴清除和致病性蛋白積累的相互交織的關係表明,腦膠質淋巴功能衰竭是多種腦損傷/疾病發病機制的關鍵步驟,可能是治療上可靶向的最終共同途徑。最近的研究發現了一些調節腦膠質淋巴系統的生理因素,包括睡眠、AQP4和血流動力學因素。然而,我們對腦膠質淋巴系統調節的理解是有限的,這阻礙了以腦膠質淋巴為基礎的治療衰老和神經退行性疾病的發展。高頻感覺刺激越來越被認為是一種有前途的非侵入性策略來調節腦功能,在各種病理條件下提供益處。美國食品藥品監督管理局(FDA)將視覺和聽覺聯合刺激(GENUS)指定為治療阿爾茨海默病(AD)的“突破性醫療設計”。事實上,GENUS在AD小鼠模型中減少β-澱粉樣蛋白沉積,逆轉認知缺陷,減少心室擴張和海馬萎縮,並改善輕度AD患者的記憶表現。此外,40 Hz閃光可減弱缺血和創傷性腦損傷的病理特徵,促進睡眠。40 Hz閃光可以在多個大腦區域中攜帶伽馬振盪,激活小膠質細胞,影響血管密度和神經免疫信號,提高神經調節劑(如乙酰膽鹼)的水平,並改變許多腦細胞類型的基因表達譜。
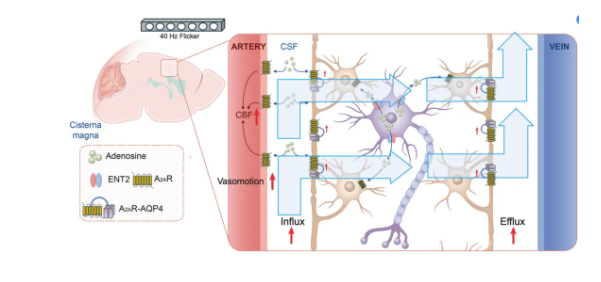
文章模式圖(圖源自Cell Discovery )對40 Hz閃光效應的兩個發現提出了令人興奮的可能性,即腦膠質淋巴系統可能代表了一種由40 Hz閃光參與的機制來控制腦損傷。首先,短暫的40 Hz閃光會使初級視覺皮層和大腦其他區域的細胞外腺苷水平強勁而持續地增加。其次,40 Hz閃光促進睡眠,此時腦膠質淋巴系統最為活躍。腺苷-A2A受體(Adenosine-A2A receptor, A2AR)信號在控制腦膠質淋巴系統中具有獨特的地位,這是基於其作為睡眠“需要”的穩態調節劑的作用,以及其調節AQP4極化和腦血流量的能力,這兩個因素都是支持腦膠質淋巴流動的關鍵因素。40 Hz閃光、增強的腺苷信號和睡眠之間的這種新關係促進了腦膠質淋巴流動,這促使研究人員提出40 Hz閃光代表了一種通過腺苷信號促進腦膠質淋巴流動的非侵入性方法。該研究發現短暫的40 Hz閃光以頻率依賴的方式增強了小鼠的腦膠質淋巴內流和外排,獨立於麻醉和睡眠,通過體外腦切片的熒光示圖,清醒小鼠的雙光子顯微鏡和體內動態對比增強磁共振成像(DCE-MRI)得出結論。這種效應歸因於星形膠質細胞終足AQP4極化表達增加和血管舒縮(vasomotion)增強。此外,該研究發現腺苷-A2AR信號是40 Hz閃光誘導的腦膠質淋巴流量增強的分子基礎,通過腦脊液中腺苷水平的增加,通過40 Hz閃光誘導的腦膠質淋巴流量增加的平衡核苷轉運體(ENTs)的藥理學和遺傳失活的消除,以及A2AR和AQP4在培養的星形膠質細胞中的物理和功能相互作用得出結論。總的來説,這些發現證實了40 Hz閃光是一種新的非侵入性策略,腺苷- A2AR信號是一種重要的調節因子,可以增強腦膠質淋巴血流,具有轉化治療神經系統疾病的潛力。參考消息:https://www.nature.com/articles/s41421-024-00701-z