做出開創性貢獻後隱入塵煙,她被2024年拉斯克獎“搶救”回來_風聞
返朴-返朴官方账号-关注返朴(ID:fanpu2019),阅读更多!41分钟前
在2024年拉斯克臨牀醫學研究獎的三位得主中,洛克菲勒大學的科學家Svetlana Mojsov無疑是存在感最低的。儘管她參與了GLP-1最初的開創性研究,破譯了真正的GLP-1活性,她能夠快速準確地大量合成實驗材料,在激烈的競爭中佔據優勢,然而在隨後的30多年裏,她隱入塵煙:GLP-1藥物大紅大紫、獲獎眾多,但獲獎者中沒有她的名字;如今70歲出頭的她,還是一名研究副教授。直到一年前,她的傳奇往事才被媒體報道出來。
編譯 | 小葉
今年6月,Svetlana Mojsov結束了假期,正與丈夫啓程返回紐約。由於飛機晚點,她抽空查看電子郵箱,結果看到 Joe Goldstein發來的一封郵件。後者是1985年的諾貝爾生理學或醫學獎得主,如今還是拉斯克醫學評選委員會主席。
Goldstein的郵件帶來了一個好消息:Mojsov成為了2024年拉斯克臨牀醫學研究獎的三位得主之一。他們的獲獎理由是發現並開發了GLP-1藥物,徹底改變了肥胖症的治療策略[1]。拉斯克獎是全球生物醫學領域最重要的獎項之一,也被譽為“諾貝爾獎風向標”。僅在過去20年時間裏,一共有32位拉斯克獎得主隨後拿到了諾獎。加之GLP-1藥物在治療糖尿病與肥胖症方面做出的巨大貢獻,人們對其可能獲得諾貝爾獎的猜測也越來越多。
其實僅僅在一年以前,Mojsov的突出學術貢獻即使在科研界也鮮為人知。直到《科學》《自然》和一些媒體報道了她之後,才將一段傳奇的科研往事公之於眾。

被遺忘的開創性貢獻
與Mojsov一同獲獎的另外兩位科學家,分別是美國麻省總醫院(Massachusetts General Hospital,以下簡稱MGH)的內分泌學家Joel Habener和跨國藥企諾和諾德的丹麥科學家Lotte Bjerre Knudsen。Habener在20世紀80年代就已是GLP-1研究領域的領軍人物,至今獲獎無數[2],聲名顯赫。Knudsen是諾和諾德的首席科學顧問,20世紀90年代開始帶領團隊在糖尿病和肥胖症藥物研發領域“開疆闢土”[3]。
與他們相比,Mojsov在GLP-1、糖尿病和肥胖相關的各種科學敍事中寂寂無名了近30年,直到2023年,她才勇敢為自己發聲,終於贏得學界的公開認可。
時間回到上世紀70年代,來自前南斯拉夫的Mojsov進入洛克菲勒大學(Rockefeller University),在著名化學家Bruce Merrifeld的實驗室攻讀研究生課程。她專攻胰高血糖素(glucagon),這是一種由胰腺釋放的激素,可用來檢測胰島素:胰島素能降低血糖,而胰高血糖素則會提高血糖。因此,科學家認為抑制胰高血糖素可能有助於治療2型糖尿病。當時,Merrifield實驗室提出了合成胰高血糖素的開創性方法,而Mojsov掌握了合成技術,她一直留在實驗室做到博士後,以改進自己的技術。
還在研究生階段,Mojsov就遇到了自己未來的丈夫——當時已有名望的免疫學家Michel Nussenzweig。他時常請Mojsov喝茶,幫助她減輕論文寫作壓力。到了80年代初,Nussenzweig獲得了MGH的住院醫師資格,Mojsov也加入了醫院內分泌科擔任教導員,她同時還負責一個新部門,為科裏的科學家合成肽。每天只要按需合成一定量的肽,對Mojsov來説,這項工作花不了太多時間。於是,她有機會開展個人研究工作,她心中早已有了明確目標:稱為胰高血糖素樣肽-1(GLP-1)的神秘肽。
同樣在70年代,Habener已經是內分泌學領域冉冉升起的科學新星。他的團隊當時一直在研究琵琶魚胰腺中的關鍵激素,也包括了胰高血糖素,他們冷凍了產生激素的胰島細胞,最終克隆出胰高血糖素原(proglucagon)。
1982年,團隊發表論文[4],報告魚的基因會編碼一種大型前體蛋白,經切割加工之後形成胰高血糖素,嵌入胰高血糖素原內的還有一段氨基酸片段,類似於胰高血糖素,這就後來大名鼎鼎的GLP-1。此外,GLP-1的氨基酸序列與腸抑胃素(GIP)共享某些特徵,後者是當時傳説中屬於腸促胰素(incretins)的唯一已知成員,科學家認為腸促胰素有潛力治療2型糖尿病,但實驗結果表明,使用它並不能有效影響糖尿病患者的胰島素水平。
於是,Habener與Mojsov都想知道GLP-1是否有所不同。首先要解決的問題是明確肽的活性產生於體內哪個部位。Mojsov在自己小小的辦公室內,仔細觀察哺乳動物GLP-1序列中的37氨基酸鏈。基於它與胰高血糖素的相似特性,她大膽假設,認為大型GLP-1肽中從位點7到位點37上的31個氨基酸組成的鏈可能是一種腸促胰島素。於是,在一張印着胰高血糖素原氨基酸序列的紙上(見下圖),她提筆記下GLP-1的功能,並決心證明自己的假設[5]。
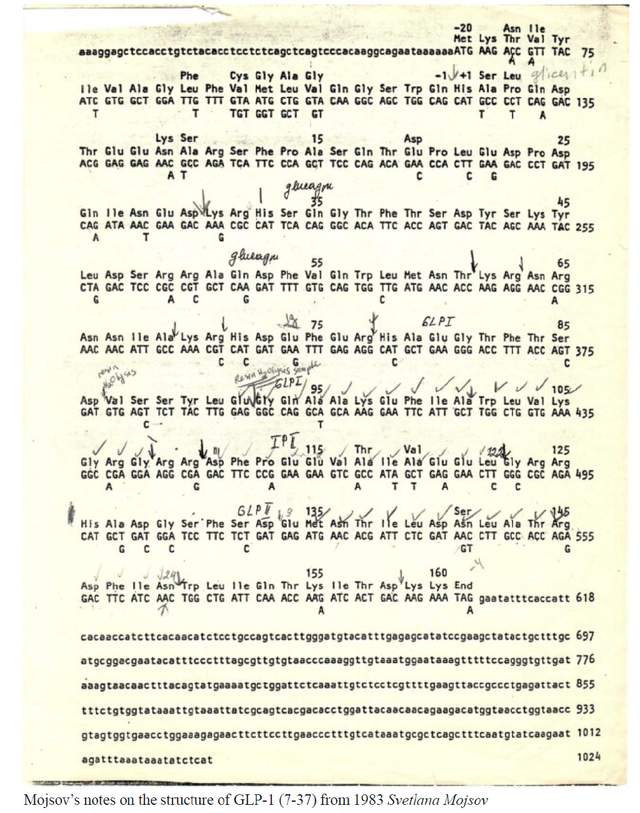
為了在腸道中尋找7-37氨基酸片段,Mojsov需要帶有抗體的魚,因為肽本身可能會以極其微小的劑量存在,難以檢測,而抗體能夠更清晰地標出肽存在的位置。她首先大批量製造出GLP-1,將其儲存在玻璃瓶中;隨後向實驗用兔子體內注射了肽的不同片段,靜待兩個月,讓抗體在兔子血液內儘可能多地增殖;最後她從兔子頸部動脈採集血液樣本,並分離出抗體。這一切全部由Mojsov獨立完成,多年實驗室的工作經驗讓她操作起來遊刃有餘。
而在Mojsov辦公室的樓下,Habener團隊則開始探索GLP-1的生物學特性。1984年,實驗室招募了博士後研究員Daniel Drucker,他的工作任務是確定哪些細胞類型能夠生成這樣的肽。作為一名從未有過實驗室經驗的新手內分泌學家,Drucker很快就陷入困境,因為沒人能協助或指導他工作。
雖然Habener與Mojsov各自開展獨立研究,但Habener明顯知道Mojsov在做什麼。於是,在Habener的建議下,Drucker找到了Mojsov,談起了合作。此時,Mojsov表示自己已經制造出針對不同GLP-1片段的抗體,並有一套方法檢測GLP-1片段的存在。接下來,Mojsov與Habener實驗室的一些研究人員聯合起來,使用Mojsov的方法在小鼠各個組織內追蹤不同的GLP-1肽片段。儘管如此,Mojsov在大部分時間裏仍然是獨自研究。最終,她發現了小鼠腸道中活躍的GLP-1(7-37)氨基酸鏈。
1986年,Mojsov與Habener作為合作者,發表論文[6],詳細描述了腸道中GLP-1(7-37)氨基酸鏈的存在。如今,這篇論文已被公認為是該領域發展的重要里程碑,Mojsov的姓名排在第一位,而Habener則作為通訊作者,排在最後。
隨後,第二個問題接踵而來:腸道中GLP-1的7-37氨基酸鏈是否具有生物活性。具體來説,它能否觸發胰腺釋放胰島素。使用Mojsov合成的GLP-1,Drucker所領導的一項研究證明[7]GLP-1確實能促進大鼠胰島細胞譜系中的胰島素分泌。緊接着,Habener想要進一步測試GLP-1對整個器官的作用,他聯繫到了自己的朋友——內分泌學家Gordon Weir。後者開發了一種大鼠胰腺模型,存活在亞克力暖箱中,裏面充滿氧氣,在室温條件下研究人員每分鐘測量模型動物的胰島素水平。當Weir注射Mojsov合成的GLP-1後,發現胰島素輸出的量隨之增加。隨後,即便減少肽的注射量,哪怕注射極其微小的劑量,研究人員都意外地觀察到同樣的效果。
Mojsov測了GLP-1的攝入量,確認肽與胰島素的應答保持一致。兩種激素“並駕齊驅,同時增加。”她形容道,“這是一場美妙無比的實驗。”終於,這篇論文於1987年發表在《臨牀調查雜誌》(The Journal of Clinical Investigation)上[8],只有三名作者,Mojsov的姓名仍然排在第一,Habener也還在最後。而Weir評價説這篇論文是自己協助的最重要研究。
在系列模型動物研究之後,Habener團隊繼續向着人體測試階段邁進,他們與Mojsov以及MGH的糖尿病專家David Nathan合作[9],Nathan將肽注射入健康受試者與糖尿病患者體內,發現GLP-1會在血糖水平升高時促進胰島素的釋放。這篇研究於1992年發表在《糖尿病護理》(Diabetes Care)期刊上,也可以説是Mojsov最後一次參與的GLP-1合作研究。
GLP-1藥物逐步“封神”
從90年代開始,Mojsov的研究生涯出現轉折。她的丈夫Nussenzweig接到了來自洛克菲勒大學的工作邀請,報酬相當誘人,他欣然答應。於是,Mojsov也隨着丈夫一起返回了紐約,滿懷希望地開啓自己的人生新篇章。
她與GLP-1藥物研發的關聯也就此中斷。此後,GLP-1相關研究突飛猛進,最終為人類與疾病的鬥爭提供了強大的新武器。
當時除了Habener團隊,其他國家的科研小組也積極探索這種肽對人類健康的影響,越來越多的研究先後發表:丹麥哥本哈根大學(University of Copenhagen)的醫學生理學教授Jens Juul Holst和現任德國波鴻魯爾大學(Ruhr-Universität Bochum)內分泌學家 Michael Nauck 共同領導的研究[10],也發現GLP-1可以使糖尿病患者的血糖水平正常化。此外Holst團隊還針對20名健康年輕男性展開調查[11],他們在豐盛的早餐後接受GLP-1靜脈注射,到了自助午餐時間,受試者放口大吃的程度低於安慰劑對照組。而英國倫敦哈默史密斯醫院的團隊也得到了類似的結論[12],將GLP-1注射到大鼠大腦中便能強烈抑制進食衝動,導致食慾不振。這似乎也暗示了GLP-1在未來的另一個應用轉化方向。
不斷報告的基礎科研成果,讓製藥公司首先看到了研發GLP-1藥物用來治療糖尿病的全新潛力。然而,在生物醫學日新月異、發展突飛猛進的新時代,從實驗室成功發現GLP-1到最終成為患者手中放心治療的藥物,竟然花了近20多年的時間。
2005年,第一批用於2型糖尿病的GLP-1藥物艾塞那肽(Byetta)獲批,不過關鍵成分是人工合成的艾塞那肽(exendin-4),源於在希拉毒蜥毒液中發現的exendin-4,這種肽的結構與功能都和人類GLP-1相似,且注射到體內數小時後不會降解[13],產生治療效果。
5年之後,諾和諾德以人體天然GLP-1分子為模版,通過更換1個氨基酸,並增加了1個16碳棕櫚酰側鏈,製造出GLP-1類似物——利拉魯肽(Victoza)[14],隨後在美國獲批用於糖尿病治療。利拉魯肽不僅保持了天然GLP-1的各種生理特性,具有高效、持久的降糖效果,且不易被降解酶所降解。而且半壽期長達12至14個小時,對於糖尿病患者來説,每日僅需皮下注射1次即可發揮良好的降糖效果。
更多的彩蛋還在後面,GLP-1藥物的應用範圍不僅限於糖尿病治療。正如前文所述,GLP-1對各種器官系統有多種影響,其中最相關的是減少食慾和食物攝入,從而達到減輕體重的目的。這是在臨牀實驗中發現的一個非常美妙的副作用,恰好能夠充分利用來解決現代人所面臨的另一場公共健康危機:超重或肥胖症。
從20世紀60年代起,就出現過苯丁胺、苄非他明和二乙丙酮等各種短期減肥藥,但長期安全性數據卻是空白[15]。一直到20世紀90年代,減肥藥“芬芬”(Fen-Phen)引發了致命心臟瓣膜病和肺動脈高壓等嚴重健康問題[16],人們始終未能找到安全有效的減肥藥物。因此,製藥企業竭盡全力開發GLP-1藥物的這一全新治療功能。終於,在2014年,諾和諾德的利拉魯肽成為第一個獲得美國食品藥品監督管理局批准的肥胖症治療藥物。
2022年,其下一代GLP-1藥物——索馬魯肽(semaglutide)繼續獲批,用於糖尿病治療(以Ozempic的藥名在市場上銷售)和體重管理(以Wegovy為藥名)。並且很快在市場上流行起來。據統計,2023年美國有1.7%的人開過Ozempic或者Wegovy的處方藥。不同於前幾款藥物,索馬魯肽只需每週注射一次。根據一項發表在《新英格蘭醫學雜誌》[17]上的研究,服用索馬魯肽的受試者在約16個月的時間內,史無前例地減掉了15%的體重,但同時也報告了常見的不良反應:噁心和腹瀉。
截至2023年,全球共11款GLP-1藥物獲批,用於治療2型糖尿病和肥胖症,主要包括艾塞那肽、利司那肽、度拉糖肽、貝那魯肽、利拉魯肽、司美格魯肽、替爾泊肽等[18]。同年,GLP-1藥物治療也成功列入《科學》年度十大科學突破之一[13]。

不再沉默,終獲認可
與GLP-1藥物的大紅大紫不同,Mojsov離開相關研發領域後,其研究生涯趨於平淡。她隨丈夫來到洛克菲勒大學,進入免疫學家、未來的諾獎得主Ralph Steinman的實驗室,擔任研究助理教授。彼時,Mojsov身邊還多了一個蹣跚學步的幼童和一個嗷嗷待哺的嬰兒。與許多職場女性一樣,她必須付出更多努力,在養育子女與拓展職業生涯之間艱辛地維持着平衡。
在美國國家科學基金會(National Science Foundation)的資助下,她轉變課題,開始研究魚類GLP-1生物學,與研究魚類葡萄糖代謝的科學家合作。與此同時,她還為實驗室的其他研究員提供多肽生物學方面的幫助,她發現自己與初級科學家的合作帶來了別樣的成就感。她認為,科學是合作,無論是剛踏入科研界的年輕科學家、初級科學家,還是資深科學家,每個人都為科學做出有價值的貢獻。她並不認可人們所謂的資深科學家才是貢獻前沿科學知識的最大功臣,而初級科學家只是輔助。
Steinman的實驗室成為了Mojsov穩定的科研陣地,她在那裏一待就是20多年,直到2011年Steinman離世。如今Mojsov還在洛克菲勒大學工作,是研究副教授,但她本人沒有領導實驗室,而是與不同科學家展開合作。
Mojsov一直為自己在 MGH 開展的 GLP-1 基礎科研工作感到自豪,也時常關注着相關進展。1996 年,她從一家生物技術公司的員工那裏得知,GLP-1的專利早在幾年前就已經授予了。
很快,她找到了 1992 年就已註冊的兩項專利,分別涉及 GLP-1 的一個“片段 ”和 “衍生物”,它們能夠促進胰島素分泌。第三項專利也在申請中。然而,所有專利都將Habener列為唯一發明人,與Mojsov一點兒關係都沒有,她內心相當震驚。
於是,Mojsov決定聘請一家律師事務所,幫助自己爭取共同發明人的權利。在與 MGH 專利部門斗爭數年之後,最終在2004至2006年間,MGH 同意修改四項專利(包括2005年授予Habener一人的第四項專利),將Mojsov列為共同發明人,同時美國專利及商標局(United States Patent and Trademark Office )也官方確認了這一發明權變動。而第五項專利於 2006 年直接授予這兩位科學家。
Mojsov表示,MGH 同意將藥物專利使用費的三分之一分給她,Habener獲得其餘部分。她拒絕透露具體數額,但表示:“對一個學者來説,這還是不錯的,沒有什麼可抱怨的。”
儘管在利益上,Mojsov因其開創性貢獻,收穫了應有的回報;但在名譽上,她還是被長期埋沒。
GLP-1藥物的大獲成功,將幕後鞠躬盡瘁的科學家們推到了公眾視野中,並且不斷榮獲各類醫學獎項。2017年,Habener、Drucker和Holst共同贏得了哈靈頓醫學創新獎(Harrington Prize for Innovation in Medicine),以表彰三位科學家“發現腸促胰素,並將其轉化,帶來了具有變革意義的新療法”[19]。2020年,他們獲得了哈佛醫學院的沃倫·阿爾伯特基金會獎(Warren Alpert Prize)[20]。2021年,享有國際聲譽的生物醫學研究獎——加拿大蓋爾德納獎(Canada Gairdner Award)也被頒發給這三位科學家[21]。
所有的獲獎成果介紹中都提到了GLP-1的發現,然而,Mojsov的名字卻未出現在任何相關科學獎項的名單中,做出突出貢獻的她被遺忘了。
前哈佛醫學院院長Jeffrey Flier承認,科學獎項是學界認可的重要方式,通常情況下,獎項委員會重點關注科研機構和同行提名的科學家,如果在GLP-1研究過程中沒有擔任重要的職位,也沒有持久的影響力,那麼Mojsov就很可能處於劣勢。
即便Mojsov因各種原因缺席了GLP-1的轉化研發階段,但並不表示可以一併抹殺她在最初基礎研究階段的所有付出。現任多倫多大學(University of Toronto)教授的Drucker承認,Mojsov的重要貢獻不應被忽視。Habener也始終記得Mojsov是一位重要的合作者:“她參與了最初的開創性研究,破譯了真正的GLP-1活性。她能夠快速準確地合成大量肽,從而讓我們在激烈的競爭中佔據優勢。”
另外,Mojsov這30多年來的寂寂無名,也許和她的個性有關,她是一個非常注重隱私的人。直到去年之前,她幾乎沒有告訴過任何人自己當年參與GLP-1研究的往事。在獲悉一切之後,她研究生時代的同學、化學家George Barany(兩人維持了近50年的友誼),Barany的兄弟、同樣也是化學家的Francis Barany,還有洛克菲勒的一些同事都紛紛支持她公開發聲。Francis Barany説:“Mojsov的遭遇在科學界是老生常談了,這裏沒有壞人,但她確實沒有得到應有的認可。”
雖然對Mojsov來説,公開談論自己並非易事,但她終於站出來,努力為自己發聲。與此同時,Habener、Drucker和Holster都證實了Mojsov的重要貢獻,Harbener表示支持Mojsov,與她同一戰線。
2023年9月《科學》發表了一篇新聞專題,詳細講述了她參與GLP-1研發的歷史與成就;同年年底,《自然》評選出年度10大科學人物,Mojsov的名字和故事也成為其中濃墨重彩的一篇,承認其早期的開創性研究為日後Wegovy,Ozempic以及其他GLP-1藥物的成功鋪平了道路[22]。各大媒體也紛紛開始報道她曾經不為人知、卻又極為重要的科研成就。
獎項也隨之而來,2023年的VinFuture獎、今年的阿斯圖里亞斯公主獎和唐獎生物技術醫藥獎,學界終於給予Mojsov遲到了近30年的認可。而今年最為重磅的拉斯克臨牀醫學研究獎同樣授予這三位GLP-1領域元老級的科學家,對Mojsov來説,不僅實至名歸,也鼓勵着各位默默奮鬥在基礎科研領域的科學家們,每一位的貢獻和付出終將有回報。
致謝:感謝美國Aspen Neuroscience公司的徐亦迅博士對本文的審核和修訂。
原文:
https://www.science.org/content/article/her-work-paved-way-blockbuster-obesity-drugs-now-she-s-fighting-recognition
相關資料
[1] https://laskerfoundationorg/winners/glp-1-based-therapy-for-obesity/
[2] https://en.wikipedia.org/wiki/Joel_Habener
[3] https://en.wikipedia.org/wiki/Lotte_Bjerre_Knudsen
[4] https://www.pnas.org/doi/abs/10.1073/pnas.79.2.345
[5] https://onlinelibrary.wiley.com/doi/10.1111/j.1399-3011.1992.tb00309.x
[6] https://www.sciencedirect.com/science/article/pii/S0021925818673247
[7] https://www.pnas.org/doi/abs/10.1073/pnas.84.10.3434
[8] https://www.jci.org/articles/view/112855
[9] https://diabetesjournals.org/care/article/15/2/270/17386/Insulinotropic-Action-of-Glucagonlike-Peptide-I-7
[10] https://www.jci.org/articles/view/116186
[11] https://www.jci.org/articles/view/990
[12] https://www.nature.com/articles/379069a0
[13] https://www.nia.nih.gov/news/exendin-4-lizard-laboratory-and-beyond
[14] https://rs.yiigle.com/CN311282200901/205195.htm
[15] https://www.mdpi.com/1422-0067/24/13/10449
[16] https://www.163.com/dy/article/I2U88IGO0511CTRH.html
[17] https://www.nejm.org/doi/full/10.1056/NEJMoa2032183
[18] https://36kr.com/p/2508251857092868
[19] https://www.harringtondiscovery.org/news-media/2017/03/14/harrington-discovery-institute-announces-2017-harrington-prize-winners
[20] https://www.eurekalert.org/news-releases/475888?adobe_mc=MCMID%3D50617636419233758663203032174279153502%7CMCORGID%3D242B6472541199F70A4C98A6%2540AdobeOrg%7CTS%3D1727132441
[21] https://www.science.org/content/article/her-work-paved-way-blockbuster-obesity-drugs-now-she-s-fighting-recognition
[22] https://www.nature.com/articles/d41586-023-03927-1

1. 進入『返樸』微信公眾號底部菜單“精品專欄“,可查閲不同主題系列科普文章。
2. 『返樸』提供按月檢索文章功能。關注公眾號,回覆四位數組成的年份+月份,如“1903”,可獲取2019年3月的文章索引,以此類推。
版權説明:歡迎個人轉發,任何形式的媒體或機構未經授權,不得轉載和摘編。轉載授權請在「返樸」微信公眾號內聯繫後台。