還在靠補蛋白留住肌肉?錯!補硒+運動才是肌肉抗衰的最強組合!_風聞
时光派-时光派官方账号-聚集全球前沿、全面、专业抗衰资讯1小时前

隨着年齡的增長,你是否感覺“走路越來越不利索了”,“樓梯爬起來好累。”這其實並非病態,而是正常的肌肉退化。根據數據顯示,在我國,65歲以上老年人因跌倒導致的傷亡率居高不下,肌肉減少已經成為老年人健康衰老的“隱形殺手”。
要説有什麼能抵抗這自然的規律?你別説還真有,近期華中農業科技大學發表在Science子刊上的研究,揭示了硒元素與肌肉萎縮之間的聯繫,並特別指出了一種名為SELENOW的含硒蛋白在肌肉衰老中扮演的關鍵角色,這可能就是我們能保持肌肉活力的關鍵!


在科學界,科學家們主要用肌肉減少症(Sarcopenia)來描述肌肉萎縮[2]。但在早期,大家往往會因為症狀並不明顯而忽視,直到出現無法挽回的嚴重後果(殘疾)。
而萎縮的核心原因,還是我們體內的運動單元(包括運動神經元、神經肌肉接頭以及肌纖維)在衰老過程中發生了結構變化,其中,運動神經元開始喪失功能,導致神經肌肉接頭傳遞失敗,肌肉纖維得不到指揮,引發肌肉功能的下降[3-4]。

圖注:隨着衰老,人們的肌肉功能下降
目前,想要逆轉肌肉萎縮,**學術界一致認可的方法是:運動!**但對於老年人來説,並不是總是可行(還有身體健康狀況、心理因素等等原因)。不過沒關係,既想逆轉(預防)肌肉萎縮,還不想運動,那你真得來看看這個“芝麻粉”(bushi)!

這看起來像是芝麻粉的東西,其實就是硒啦!作為地殼中儲量極低、分佈相當稀散的罕見元素,它竟能神奇地在我們身體裏安了家,成了我們體內不可或缺的微量元素小分隊的一員。
雖説微量,但它在人體中的作用可一點也不“微”。不僅是身體中多種抗氧化酶的組成部分,保護細胞免受氧化應激傷害[5],還能****增強免疫力[6]、預防疾病[7]以及支持營養恢復[8]。在我們體內,它主要以硒代半胱氨酸的形式,存在於25種硒蛋白裏,包括我們今天要介紹的主角也是其中一種:SELENOW蛋白。

SELENOW,全稱Selenoprotein W。能調控細胞的氧化還原與細胞週期不説,還會直接參與肌肉的生長發育。科學家們發現,患有肌少症的小鼠,體內的SELENOW蛋白表達量顯著升高,這也不禁讓他們猜想,SELENOW會不會是為了拯救小鼠的肌肉,自願多表達來緩解肌肉降解?

圖注:患有肌少症的小鼠SELENOW蛋白的表達量要高於對照組
為了驗證猜想,科學家們過表達了小鼠的SELENOW基因,發現患有肌肉萎縮症的小鼠,肌肉也不掉了,肌纖維橫截面積也不縮小了,並且體內與肌肉生長、萎縮相關的蛋白表達也相互平衡了起來。

圖注:過表達小鼠的SELENOW基因能改善肌肉質量
如果説過表達實驗僅僅證明了SELENOW蛋白“至關重要”,而敲除實驗,則進一步説明了“沒你不行”。研究人員發現,SELENOW基因缺失的小鼠,除了伴有明顯的肌肉重量和肌纖維橫截面積減少外,還引起了抗氧化能力下降和氧化應激的增加,加劇了肌肉退化。

圖注:敲除小鼠的SELENOW基因會加速肌肉的退化
既然是“沒你不行”,還得揪一下是小鼠體內的哪個基因(蛋白),沒SELENOW不行?研究人員隨即對敲除SELENOW基因小鼠的肌肉細胞進行RNA測序,結果發現與正常肌肉細胞相比,存在大量差異表達基因(DEGs),而這些基因與肌肉系統過程、蛋白質合成與降解等過程息息相關。

圖注:SELENOW在肌肉減少症中的作用可能通過Rho信號傳導
不過最重要的,其中當屬SELENOW與RAC1蛋白之間的關係,它們之間存在直接的相互作用。作為鳥苷三磷酸(GTP)酶的一種,RAC1蛋白在細胞內參與調控多種細胞功能和生理過程,包括細胞形態改變、細胞遷移、細胞增殖和細胞黏附等,不過最重要的還是它對mTORC1信號通路的重要影響。
作為細胞中重要的信號傳導中心,mTORC1參與調節細胞的生長、代謝、蛋白質合成以及細胞自噬等過程。而mTORC1的異常活化則會引發衰老。

圖注:SELENOW通過RAC1-mTORC1信號通路調節肌肉蛋白質合成與降解
研究mTORC1信號通路上的基因後,研究人員發現,原來這SELENOW基因的缺失,會導致RAC1蛋白表達下降,進而抑制mTORC1信號通路活性,導致身體蛋白質合成減少,最終加劇了肌肉萎縮。
看來,兜兜轉轉,最後還是回到了mTORC1通路上……不是之前説的抑制通路延壽,反而抑制通路導致蛋白質合成(肌肉相關)和降解失衡,導致細胞功能紊亂,加速衰老過程。

看完人家的研究後,你是不是也和派派感覺一樣,想現在立刻馬上就補一點硒,給自己一點心理安慰?不過先彆着急,為了嚴謹,派派也翻閲了《中國居民膳食營養素參考攝入量(2023版)》,其中,對硒的攝入量推薦為60 微克/天,可耐受的最高攝入量為400微克/天。
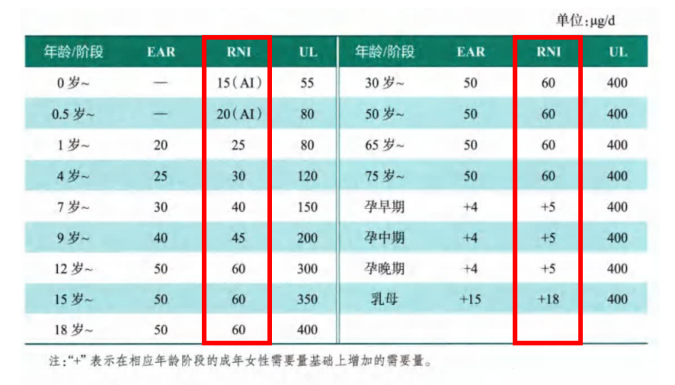
圖注:中國居民膳食硒參考攝入量(RNI為日推薦攝入量,UL為可耐受最高攝入量)
60微克每天?什麼概念?來來來,這張食物硒含量圖來解答你的疑惑[9]。

圖注:部分食物的硒含量
讓派派給你算筆賬哈,以牛肉平均硒含量140ng/g來算,一天約一斤牛肉就能滿足當日的硒需求量,更何況還有其他食物中的硒攝入,所以對於正常人羣來説,只要你不偏食、挑食,注意營養均衡,通過日常飲食就能輕鬆get到足夠的硒,壓根兒不需要額外補貨。
若是確診為缺硒的亞健康人羣,而且飲食無法自己每日的硒需要量時,就可以考慮挑點硒產品來給自己補補:推薦每天50微克即可。話又説回來了,要補哪種硒?本着送佛送到“硒”的想法,派派也看了看相關硒補充劑信息,發現這水還不是一般的深……

市場上的硒補充劑五花八門,主要分為無機、半有機和有機三大流派。其中,無機流派,以硒酸鈉和亞硒酸鈉為例,它們的生物有效性偏低,不僅吸收利用效果不好,而且安全攝入範圍太窄,一不小心就容易引起過量中毒 [10],所以一般就補硒來説,無機硒是下策。
不同於無機硒,半有機形式的硒以硒酵母和植物硒蛋白為主要代表,以硒酵母為例,在酵母生長的過程中加入硒元素,使硒與酵母體內的蛋白質和多糖有機結合,轉化為生物硒(硒代蛋氨酸、硒代半胱氨酸等),避免了化學硒對人體的毒副反應和腸胃刺激,讓硒能更高效、更安全地被人體吸收利用[11]。

圖注:補充硒酵母后,人血液中的硒含量也直線上升!
所以,半有機形式的硒其實是在酵母、植物小時候給它們喂硒,到時候成熟了再收割一波,為我們所用。你可能會想,為啥這麼複雜,直接補充硒不是更好?這就到了我們的第三代硒:有機硒。
不同於半有機硒,有機硒則是完完全全拋棄了上面的載體(酵母、植物等),完全憑藉“自己”來進行體內硒的補充,其中就以我國批准的L-硒-甲基硒代半胱氨酸(L-SeMC)為例,通過給硒代半胱氨酸左旋化(提高吸收效率),加甲基(保護),來讓它在外部環境中穩定存在,發揮功效。

圖注:L-硒-甲基硒代半胱氨酸已於2009年被衞生部批准為新型營養強化劑
説了這麼多補硒事項,還是別忘記了最能對抗肌肉衰老的方法,運動。就像之前説的,學術界普遍認為運動,特別是高強度的肌肉力量訓練,才是防止衰老引發肌肉萎縮症的頭等要事(想光靠補硒就一勞永逸的派派悄悄碎了……)。

肌肉力量訓練對於對抗老年人肌肉弱化和身體虛弱是可行且有效的[12]。有研究表明,經過高強度的肌肉力量訓練可以促進肌肉體積和質量的增長[13-14],而且,參與者的動態肌肉力量顯著增加,平均增幅高達65%[15] 。

圖注:高強度抗阻訓練能增加動態肌肉力量
所以,肌肉流失,並非衰老的必然宿命。正如文中所言,運動和合理的硒元素攝入都能幫助我們應對這一自然過程。可別等到肌肉減少,腿站不穩摔一跤才開始重視健康,趁現在抓緊行動,多做點高強度的肌肉力量訓練,保持肌肉活力,才能健康的衰老呀~
參考文獻
[1] Yang, J.C,Liu, M.,Huang, R.H,Zhao, L.,Niu, Q.J,Xu, Z.J,Wei, J.T,Lei, X.G, & Sun, L.H (2024). Loss of SELENOW aggravates muscle loss with regulation of protein synthesis and the ubiquitin-proteasome system. Science advances, 10 (38), eadj4122. https://doi.org/10.1126/sciadv.adj4122
[2] Larsson, L.,Degens, H.,Li, M.,Salviati, L.,Lee, Y.I,Thompson, W.,Kirkland, J.L, & Sandri, M. (2019). Sarcopenia: Aging-Related Loss of Muscle Mass and Function. Physiological reviews, 99 (1), 427-511. https://doi.org/10.1152/physrev.00061.2017
[3] Aagaard, P.,Suetta, C.,Caserotti, P.,Magnusson, S.P, & Kjaer, M. (2010). Role of the nervous system in sarcopenia and muscle atrophy with aging: strength training as a countermeasure. Scandinavian journal of medicine & science in sports, 20 (1), 49-64. https://doi.org/10.1111/j.1600-0838.2009.01084.x
[4] Prior, S.J,Ryan, A.S,Blumenthal, J.B,Watson, J.M,Katzel, L.I, & Goldberg, A.P (2016). Sarcopenia Is Associated With Lower Skeletal Muscle Capillarization and Exercise Capacity in Older Adults. The journals of gerontology. Series A, Biological sciences and medical sciences, 71 (8), 1096-101. https://doi.org/10.1093/gerona/glw017
[5] Huan, Q. (1999). The role of selenium in nutritional support and research progress. Parenteral & Enteral Nutrition.
[6] Xiaojing Xia,Xiulin Zhang,Mingcheng Liu,Mingyuan Duan,Shanshan Zhang,Xiaobing Wei, & Xingyou Liu (2021). Toward improved human health: efficacy of dietary selenium on immunity at the cellular level. Food & Function, 12 (3), 976-989. https://doi.org/10.1039/d0fo03067
[7] Clark LC, Combs GF, Turnbull BW, et al. Effects of Selenium Supplementation for Cancer Prevention in Patients With Carcinoma of the Skin: A Randomized Controlled Trial. JAMA. 1996;276(24):1957–1963. doi:10.1001/jama.1996.03540240035027
[8] Silvia Maggini,E. S. Wintergerst,S. Beveridge, & D. Hornig (2008). Contribution of selected vitamins and trace elements to immune function. Proceedings of the Nutrition Society, 67 (OCE1), 0-0. https://doi.org/10.1017/s0029665108006939
[9] Navarro-Alarcon, M., & Cabrera-Vique, C. (2008). Selenium in food and the human body: a review. The Science of the total environment, 400(1-3), 115–141. https://doi.org/10.1016/j.scitotenv.2008.06.024
[10] Vinceti, M., Wei, E., Malagoli, C., Bergomi, M. & Vivoli, G. (2001). Adverse Health Effects of Selenium in Humans. Reviews on Environmental Health, 16(4), 233-252. https://doi.org/10.1515/REVEH.2001.16.4.233
[11] Erik Huusfeldt Larsen,Marianne Hansen,Helge Paulin,Sven Moesgaard,Mary E. Reid, & Margaret P. Rayman (2004). Speciation and Bioavailability of Selenium in Yeast-Based Intervention Agents Used in Cancer Chemoprevention Studies. Journal of AOAC INTERNATIONAL, 87 (1), 225-232. https://doi.org/10.1093/jaoac/87.1.225
[12] Maria A. Fiatarone,Evelyn F. O’Neill,Nancy Ryan,Karen M. Clements,Guido R. Solares,Miriam E. Nelson,Susan B. Roberts,Joseph J. Kehayias,Lewis A. Lipsitz, & William J. Evans (1994). Exercise Training and Nutritional Supplementation for Physical Frailty in Very Elderly People. The New England Journal of Medicine, 330 (25), 1769-1775. https://doi.org/10.1056/nejm199406233302501
[13] Robert Csapo, & Luis M. Alegre (2015). Effects of resistance training with moderate vs heavy loads on muscle mass and strength in the elderly: A meta-analysis. Scandinavian Journal of Medicine & Science in Sports, 26 (9), 995-1006. https://doi.org/10.1111/sms.12536
[14] Charlotte Suetta,Jesper L. Andersen,Ulrik Dalgas,Jakob Berget,S. Koskinen,Per Aagaard,S. Peter Magnusson, & Michael Kjær (2008). Resistance training induces qualitative changes in muscle morphology, muscle architecture, and muscle function in elderly postoperative patients. Journal of Applied Physiology, 105 (1), 180-186. https://doi.org/10.1152/japplphysiol.01354.2007
[15] Neil, M. C. , Hicks, A. L. , Joan, M. , & Webber, C. E. . Long-term resistance training in the elderly: effects on dynamic strength, exercise capacity, muscle, and bone. Journals of Gerontology(2), B97.