減壽22%?“抗衰名流”二甲雙胍驚變“老年殺手”!這個“胍”可得謹慎點吃!_風聞
时光派-时光派官方账号-聚集全球前沿、全面、专业抗衰资讯58分钟前

咱就是説,物質抗衰這條路還真是走得跌跌撞撞。前有老牌抗衰神藥煙酸落寞退場,後又有抗衰明星NMN禁售風波,老牌抗衰藥雷帕黴素和二甲雙胍總行了吧,什麼?好評收藏家二甲雙胍居然也要“塌房”了?

最近,復旦大學和廣西醫科大學聯合發表一項研究表明,二甲雙胍抗衰具有雙相性,是**“吃出長壽”還是“偷走壽命”**,還得看胍胍背後“不為人知的一面”[1]。

在開始探索胍胍的雙相性之前,想和大家分享一個好消息!本文的通訊作者盧國棟教授受時光派邀請,將在11.1-3日來到上海,參加時光派第五屆衰老幹預論壇,如果你對他的研究感興趣,點擊下方卡片回覆fudan246,一鍵解鎖時光派第五屆衰老幹預論壇!千人“長壽盛會”,期待有你同行!

論時下最炙手可熱的抗衰候選藥,胍胍必有一席之地,沒錯,就是那個因成本低、風險小和療效強而蟬聯“降糖一哥”寶座至今的藥物,二甲雙胍。
胍胍能得抗衰界青睞,與其能降低糖尿病患者7%的全因死亡率[2]、緩解肌肉萎縮[3]、逆轉表觀年齡[4]和防止皮膚老化[5]等抗衰潛力息息相關。
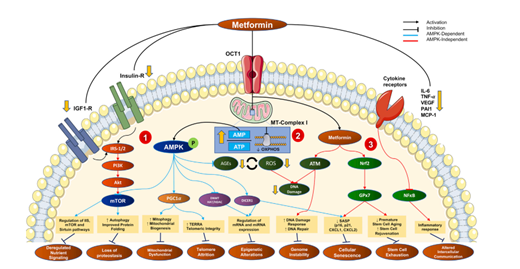
圖注:二甲雙胍減緩生物衰老特徵的作用機制
然而,胍胍降糖、抗衰再厲害,也難逃潛在毒性這一拖油瓶。除了高劑量可能因引起腎衰竭或乳酸酸中毒而使小鼠減壽14%[6]外,長期服用胍胍,還有加劇認知障礙和阿爾茲海默的風險[7]。

對於之前研究中已經展示出來的胍胍的兩面性,研究者指出,不管是抗衰還是潛在的毒性,實驗對象的遺傳和代謝都會影響胍胍的發揮。
即使不考慮遺傳因素,代謝也會隨年齡而變化。因此他們推測,年齡相關基因表達的變化可能也是胍胍效應背後的推手。一場基於此點的探究就此展開。

傳聞胍胍抗衰有“年齡歧視”?探究就從這裏出發!
在幼年(生命週期的5.56%)線蟲身上,胍胍一如既往地發揮出了抗衰效果。
胍胍治療後,幼蟲的健康壽命獲得了明顯改善,不僅食慾增加,還愛上了運動;氧化應激指標DCF的熒光強度和衰老指標脂褐素的水平均顯著下調。整體作用下,幼蟲的平均壽命足足延長了11.1%!
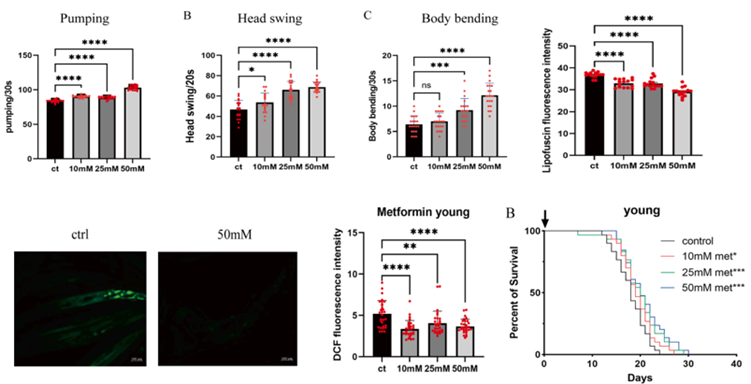
圖注:胍胍促進幼蟲攝食、運動和降低脂褐素(上),降低DCF和延長壽命(下)
但別高興太早,在成年晚期(生命週期的44.44%)的線蟲身上,胍胍畫風突變!
胍胍治療後,老年線蟲不僅不愛吃了,動也懶得動了。DCF熒光積累和脂褐素水平均明顯增加,平均壽命更是可怕地縮短了22%!
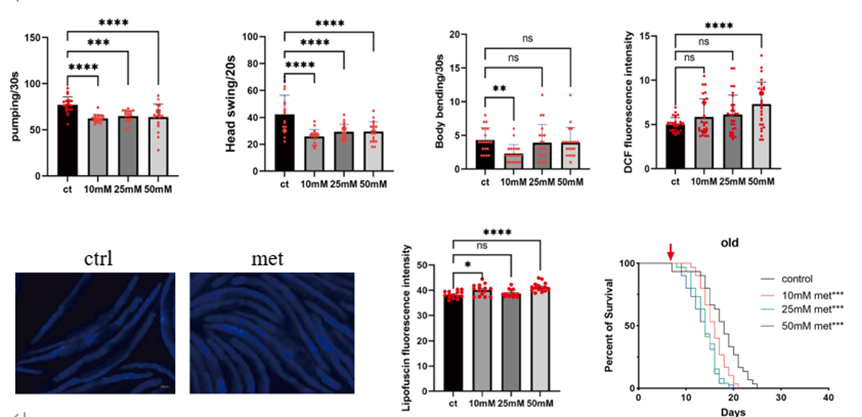
圖注:胍胍降低老年線蟲攝食、運動行為和升高DCF水平(上),升高脂褐素水平和縮短壽命(下)
這一結果和此前報道的一項研究結果其實存在一致性:都表明胍胍能使幼年秀麗隱杆線蟲延壽同時使老年線蟲減壽,具有年齡特異性雙相效應[8]。
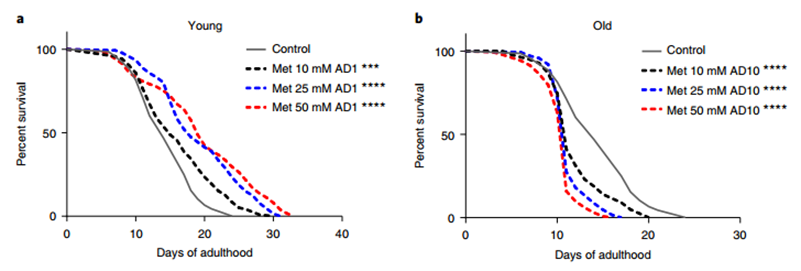
圖注:此前實驗中類似的結果:胍胍使幼年線蟲延壽,使老年線蟲減壽

所以,胍胍對年齡的“歧視”現象還真存在!儘管前面提到,代謝可能會影響胍胍的發揮,但若真要在生物自身方面找原因,還是得從基因這個掌管一切生命活動的根源處下手。

研究顯示,胍胍處理後,幼年和老年線蟲體內的生物途徑出現了不同的富集情況:在幼年線蟲體內,主要是像鈣信號和溶酶體等有助於提高健康和壽命的生物途徑加強;而在老年線蟲體內,主要是與老化加劇相關的如軸突再生和嘌呤代謝等途徑的增強。
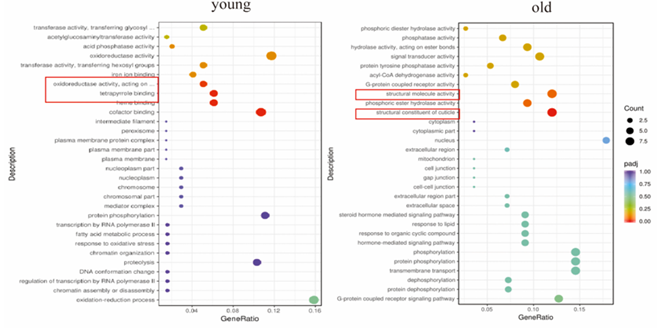
圖注:幼年和老年線蟲體內生物途徑的富集情況(基因本體富集分析)
**生物途徑的不同富集表現暗示着其背後基因表達的變化。**通過分析不同年齡的差異基因,研究者們發現了14個在幼蟲中上調而在老蟲中下調的基因,以及7個相反趨勢的基因。
進一步篩選之後,兩個最關鍵的基因nhr-57(核激素受體基因,參與低氧應答、轉錄調控和代謝等生物途徑)和C46G7.1(人類RNASEK的同源基因,影響RNA的內切核酸酶活性)被找到,胍胍處理後,它們在幼年線蟲中上調,而在老年線蟲中下調。
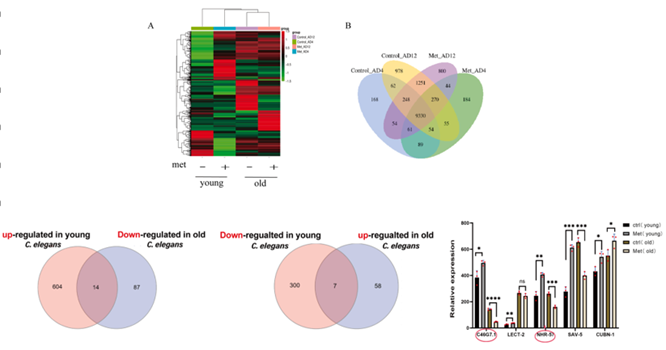
圖注:幼蟲和老蟲之間的差異表達基因和nhr-57和C46G7.1的確定
在上百個差異基因中能鎖定到nhr-57和C46G7.1,它們自然與胍胍的雙相效應最密切相關。那麼,最簡單的驗證辦法還是老樣子:敲掉它們!

研究顯示,敲除nhr-57或C46G7.1後,幼年和老年線蟲壽命均縮短,幼蟲壽命縮短33%,老年線蟲壽命縮短39%,且兩種基因縮短壽命的百分比相似。壽命之外具體而言,敲除nhr-57或C46G7.1還導致所有線蟲的食慾、活動和健康指標下降。
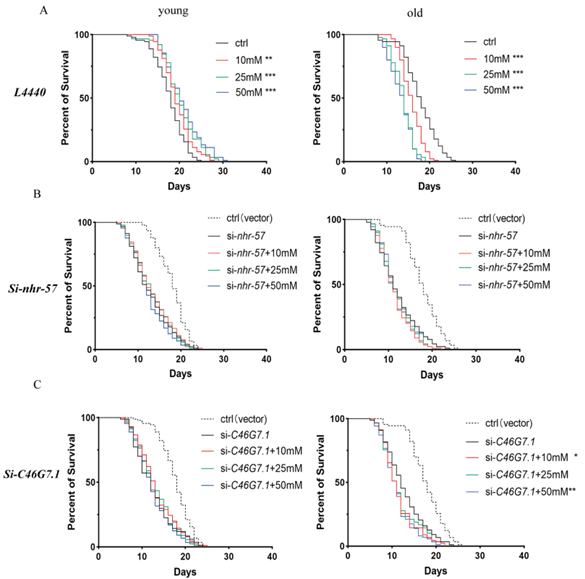
圖注:基因敲除使幼蟲和老蟲的壽命顯著減少
有意思的是,對於老年線蟲來説,雖然咋樣都不能延壽,但敲除基因這種方式卻能在一定程度上減輕胍胍帶來的不利影響,如食慾雖然也下降,但不再那麼明顯。這也算是一種因禍得福?
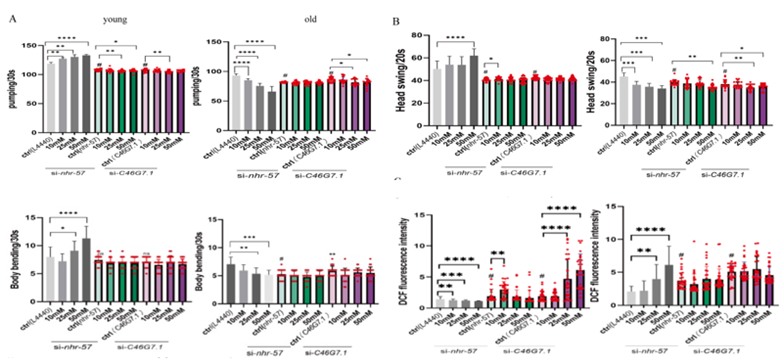
圖注:基因敲除使所有線蟲食慾、活動和DCF水平均下降並減輕了胍胍對老年線蟲的負面影響
最後,細心的研究者還注意到,關鍵基因之一的nhr-57還有一個神秘身份:缺氧誘導因子1(hif-1)的靶標。
hif-1是缺氧時通過調節基因表達來幫助細胞適應低氧環境以延長壽命的關鍵因子。敲除hif-1後所有線蟲的表現與敲除nhr-57出奇地一致。所以,nhr-57很有可能是通過hif-1因子來調控壽命的。
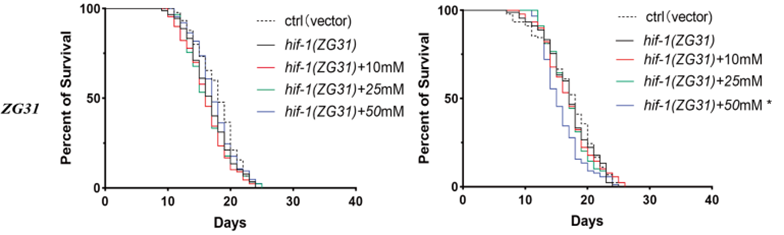
圖注:敲除hif-1基因後所有線蟲的壽命縮短
總的來説,胍胍對線蟲的壽命具有年齡依賴性的雙相效應,基因nhr-57和C46G7.1在調節壽命和介導胍胍雙相效應中發揮着不可或缺的作用。
優秀如胍胍,想不到有天也會成為“老年人的催命藥”。仔細想來,抗衰藥物好像沒幾個能火的一帆風順的,在質疑中成長或許才是每個藥物必經的旅程。
藥物抗衰是個與藥物、個體本身和環境等都能相互作用的複雜過程。就像深海潛水,越下潛,遇到的挑戰和未知情況也會越多。但不可否認,胍胍年齡特異性作用的發現,將促使抗衰實踐的目光更多地投向年齡、劑量和個體差異方面,而我們,對胍胍也有了更全面的認識。
[本文的名稱是《A mechanistic analysis of metformin’s biphasic effects on lifespan and healthspan in C. elegans: Elixir in youth, poison in elder》,發表於《Mechanisms of Ageing and Development》期刊,通訊作者是復旦大學公共衞生學院盧國棟教授、廣西醫科大學基礎醫學院生理教研室周靜教授。第一作者是Yu Zhen-Zhen。本研究由上海市三年行動計劃(GWVI-11.1-41)和復旦大學教授啓動基金資助。]
參考文獻
[1] Yu, Z. Z., Tu, J. J., Ou, M. L., Cen, J. X., Xue, K., Li, S. J., … & Lu, G. D. (2024). A Mechanistic Analysis of Metformin’s Biphasic Effects on Lifespan and Healthspan in C. elegans: Elixir in Youth, Poison in Elder. Mechanisms of Ageing and Development, 111963.
[2] Metformin reduces all-cause mortality and diseases of ageing independent of its effect on diabetes control: A systematic review and meta-analysis - ScienceDirect
[3] Petrocelli, J. J., McKenzie, A. I., de Hart, N. M., Reidy, P. T., Mahmassani, Z. S., Keeble, A. R., … & Drummond, M. J. (2023). Disuse‐induced muscle fibrosis, cellular senescence, and senescence‐associated secretory phenotype in older adults are alleviated during re‐ambulation with metformin pre‐treatment. Aging Cell, 22(11), e13936.
[4] Luo, S., Wong, I. C. K., Chui, C. S. L., Zheng, J., Huang, Y., Schooling, C. M., & Yeung, S. L. A. (2023). Effects of putative metformin targets on phenotypic age and leukocyte telomere length: a mendelian randomisation study using data from the UK Biobank. The Lancet Healthy Longevity, 4(7), e337-e344.
[5] Gouveri, E., & Papanas, N. (2023). Τhe Endless Beauty of Metformin: Does It Also Protect from Skin Aging? A Narrative Review. Advances in Therapy, 40(4), 1347-1356.
[6] Martin-Montalvo, A., Mercken, E. M., Mitchell, S. J., Palacios, H. H., Mote, P. L., Scheibye-Knudsen, M., … & de Cabo, R. Metformin improves healthspan and lifespan in mice. Nat Commun. 2013; 4: 2192.
[7] Cho, S. Y., Kim, E. W., Park, S. J., Phillips, B. U., Jeong, J., Kim, H., … & Kim, E. (2024). Reconsidering repurposing: long-term metformin treatment impairs cognition in Alzheimer’s model mice. Translational psychiatry, 14(1), 34.
[8] Espada, L., Dakhovnik, A., Chaudhari, P., Martirosyan, A., Miek, L., Poliezhaieva, T., … & Ermolaeva, M. A. (2020). Loss of metabolic plasticity underlies metformin toxicity in aged Caenorhabditis elegans. Nature Metabolism, 2(11), 1316-1331.