Adv Mater丨發現調控肺部纖維化機械微環境治療特發性肺纖維化_風聞
葆力医学观察-专注生物科研领域,趣味科普与行业干货齐飞48分钟前
不良機械力會加劇特發性肺纖維化(IPF)的惡化,破壞肺機械微環境穩態,導致肺泡功能障礙。纖維化肺固有的機械敏感性使II型肺泡上皮細胞(AECII)受到持續拉伸,過度活化的肌成纖維細胞在機械轉導過程中經歷惡性相互作用,必須開發有效的策略來調節肺機械微環境。
2024年11月12日,中國藥科大學/延邊大學/韓國成均館大學姜虎林唯一通訊在Advanced Materials 在線發表題為“Modulating Fibrotic Mechanical Microenvironment for Idiopathic Pulmonary Fibrosis Therapy”的研究論文。該研究構建了環(RGDfC)肽修飾的沸石咪唑酸鹽框架-8納米顆粒(ZDFPR NPs),靶向和修復病理肺中異常的機械力水平。
具體來説,pH響應性ZDFPR NPs通過釋放鋅離子和7,8-二羥基黃酮降低了的AECIIs中的機械張力,促進肺泡修復和分化。同時,fasudil抑制ROCK信號通路,破壞機械轉導過程中肌成纖維細胞收縮力和細胞外基質剛度之間的惡性相互作用被破壞。結果表明,ZDFPR NPs恢復了博來黴素誘導的纖維化小鼠的肺機械穩態並終止了纖維化過程。該研究不僅為調節肺機械微環境提供了一種有效策略,而且為IPF治療開闢了新方向。

特發性肺纖維化(IPF)是一種進行性且致命的肺部疾病,其特徵是肺組織的結構、組成和剛度發生變化,導致肺功能永久性惡化。在新冠肺炎疫情之後,IPF的發病率和患病率逐漸增加,影響了全球約50萬人,並造成了沉重的健康負擔。雖然尚不清楚IPF的發病機制,但各種因素引起的機械力對其造成的有害影響持續存在。纖維化微環境中,來源於上皮-內皮屏障的破壞、細胞產生的力、外部拉伸的增加和間質壓的變化等組織機械損傷,破壞了機械穩態,加劇了疾病的惡性進展,最終增加發病和死亡的風險。特別是,作為一個天生的機械敏感器官,肺受到巨大的機械力,在IPF過程中其結構和功能逐漸惡化。對肺泡的重複性機械損傷會重塑細胞骨架,激活成纖維細胞並引發細胞外基質(ECM)應力過度增加,從而破壞肺部機械微環境,損害肺泡功能,並加劇疾病的嚴重性。此外,機械刺激不僅影響細胞和器官功能,對發育和機械感知也必不可少。因此,有效解決機械刺激對IPF機械微環境的影響可以減緩甚至逆轉纖維化進程。
在纖維化肺組織中,機械微環境會造成重大損傷,加速組織降解。一方面,II型肺泡上皮細胞(AECIIs)作為肺泡幹細胞的再生能力受損,受到的機械張力逐漸增加,阻礙其分化為I型肺泡上皮細胞(AECIs)。進一步的研究表明,AECIIs的早期微損傷也會增加局部血管通透性並誘導細胞骨架重塑,從而改變細胞機械力。另一方面,雖然ECM蛋白創建了為細胞提供關鍵結構和生物力學信息的網絡,但在機械轉導過程中收縮肌成纖維細胞和緻密的ECM之間惡性相互作用的生物力學調控仍有待解決。該過程中,外力刺激可以觸發成纖維細胞周圍整合素受體的聚集,從而改變其骨骼結構,並通過將α平滑肌肌動蛋白(α-SMA)納入應力纖維中來產生高收縮力,從而激活肌成纖維細胞。肌成纖維細胞是纖維化發生的主要效應細胞,產生過量的ECM,導致基質變硬。隨後,ECM機械應力增加觸發正常成纖維細胞的再激活以進行機械轉導,建立了一個由“肌成纖維細胞收縮力-ECM剛度-再激活成纖維細胞”構成的惡性循環。這種惡性循環導致肺組織內機械硬度累積,加速了IPF的惡性發展,導致呼吸衰竭風險增加。可以説,纖維化微環境的機械化既是纖維化進展的結果,也是誘因。值得注意的是,雖然目前IPF的治療策略主要集中在調節生化信號上,但解決機械力改變對肺機械微環境造成的實質性破壞問題更為關鍵。
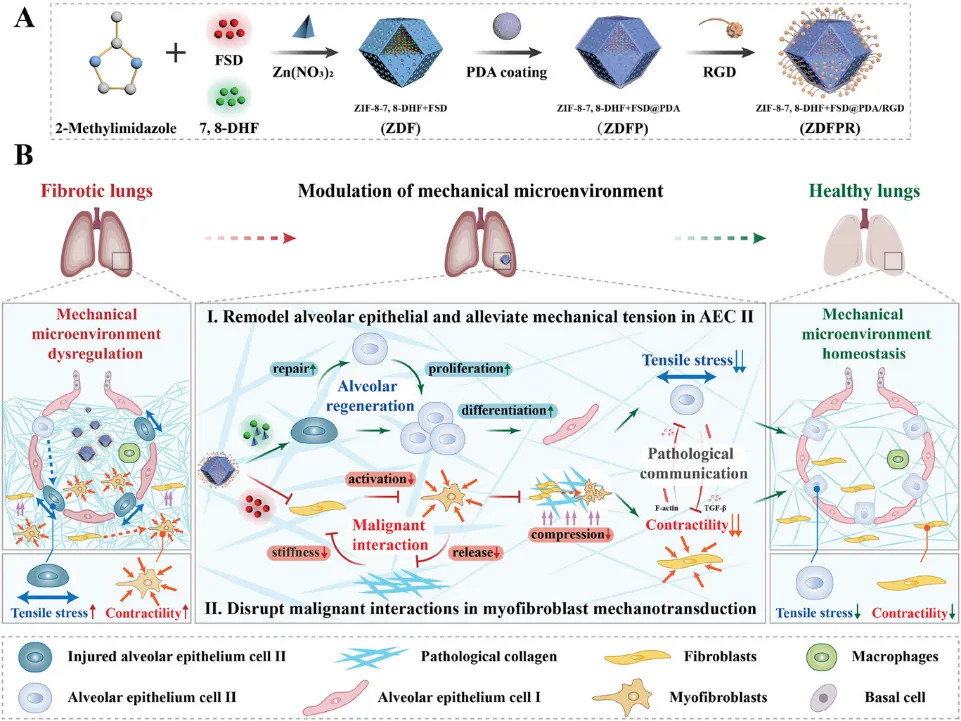
圖1 ZDFPR NPs製備及IPF治療示意圖(摘自Advanced Materials)
該研究使用沸石咪唑酸鹽框架8(ZIF-8)構建了一種納米顆粒ZDFPR NPs,以解決IPF中肺機械微環境失調的問題,促進肺泡上皮重塑並減輕AECIIs中的機械壓力,改善肌成纖維細胞機械轉導中的惡性相互作用。生物相容性ZIF-8負載了治療藥物7,8-二羥基黃酮(7,8-DHF)和fasudil(FSD),外層包裹聚多巴胺(PDA)並用環(RGDfC)肽(RGD)修飾,靶向富含整合素-αvβ6的受損AECIIs和肌成纖維細胞。對博來黴素(BLM)誘導的纖維化小鼠進行霧化給藥後,ZDFPR NPs響應pH變化釋放鋅離子並激活鋅轉運蛋白8/沉默信息調節因子1(ZIP8/SIRT1)通路以修復AECII。此外,7,8-DHF促使 AECIIs修復並分化為AECIs,並恢復正常肺泡間隙的機械微環境。Rho相關蛋白激酶(ROCK)抑制劑FSD破壞肌動蛋白細胞骨架,其對肌成纖維細胞的收縮性至關重要,同時抑制肌成纖維細胞內的機械敏感信號傳導並破壞ECM和肌成纖維細胞之間的惡性相互作用。機械微環境中,ZDFPR NPs同樣中斷了AECIIs和成纖維細胞之間的病理通訊。因此,ZDFPR NPs可以調控受干擾的機械微環境,使其恢復正常的機械穩態,並提高IPF的治療效果。
參考消息:
https://onlinelibrary.wiley.com/doi/full/10.1002/adma.202407661