工作裏做對1件事延壽12.4%!_風聞
时光派-时光派官方账号-聚集全球前沿、全面、专业抗衰资讯56分钟前

你是一隻平凡的小鼠。基因平凡,生活平凡,在研究所的“工作”平凡。
每天你在工位,都有一隻似乎不那麼平凡、但會給你帶來壓迫感的小鼠來與你溝通10分鐘的工作,然後接下來它都會坐在離你不遠、你能感受到的地方。除了偶爾會羨慕隔壁工位狹小但不用social的“同事”,日子就這麼平平淡淡一天天過去了,但在這樣花費了生命1/30-1/15時間後你猛然發現,你老了,剩餘的日子也不多了……
等會兒,這竟然不是擬人故事,而是最新發表在衰老生物學經典專刊《Nature Aging》上的科學研究?不必懷疑,你正在看的就是派派報導的**《衰老誘因研究之社會壓力折壽12.4%·“打工鼠”的故事》**[1],更多精彩,請繼續看。


誠如開頭所描述的,本文研究就是這樣展開的:採用的是最普通的3月齡年輕C57BL/6J小鼠,其中一組小鼠和更具侵略性、占主導地位[2]的CD1小鼠兩兩共養,每天有10分鐘交互接觸時間,其他時間用多孔隔板隔開;另一組則每天有3小時在僅能定點卧趴的狹小空間裏。
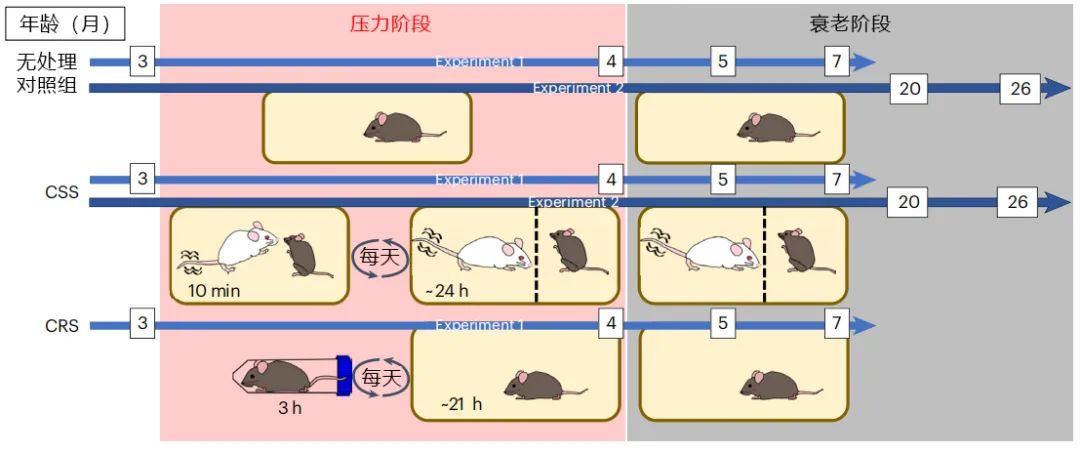
圖注:白色為CD1強勢鼠,棕色為C57BL/6J普通實驗鼠,圖示為具體實驗流程
實驗鼠們平均能活約30月,而實驗只連續開展1-1.75月,實驗結束後就檢測不同組小鼠的衰老指標……那,在這個實驗中,真正要討論的“變量”,或者説,研究者們想發現的那個能影響衰老的因素是什麼?
對第一段科學性描述進行擬人化想象可能會給大家帶來不太美妙的回憶,但本文的中心主題能隨之浮現:**慢性社會從屬壓力(CSS),**與之相對比的對照組則是慢性約束壓力(CRS)。

壓力是什麼?從生理層面上,壓力被定義為“環境需求超過生物體自然調節能力的、不可預測、不可控的情況”,有打破包括人類在內的各種生物的體內平衡的能力[2]。
既然能打破生理平衡,就可能促進衰老。確實,早就有研究嘗試討論壓力對衰老的促進作用,比如2023年6月的一項發表研究表示,童年壓力會導致中年加速衰老[3]。但壓力也分很多種,那到底哪種壓力才是衰老“罪魁禍首”?

本文抱着這樣的疑問展開了研究,並從心理層面和物理層面分別挑選了1種人生在世最可能遇到的“壓力源”展開討論——因為社交產生的社會從屬壓力和因為生存環境產生的約束壓力。
事實證明,“人為”壓力可比“環境”壓力可怕多了。
No.1
都想着換別人年輕血液,只有我把自己血液“催熟”了?
p16Ink4a是細胞衰老的重要標誌之一,所以研究者們抽取了經歷了2種壓力7周後小鼠的血液進行對比。血細胞類型都沒有發生改變,但經歷從屬壓力(CSS)小鼠外周血單核細胞(PBMC)的p16Ink4a的表達量升高了,而經歷約束壓力(CRS)的小鼠沒有。
而且研究者發現,實驗在進行7周後(此時實驗鼠不到5月齡,約為人類不到成年)就停止了,但衰老沒有。等到20月齡和26月齡的時候,它們外周血p16Ink4a水平就會從實驗剛結束時的對照組6倍慢慢增長到7倍,然後是12倍。
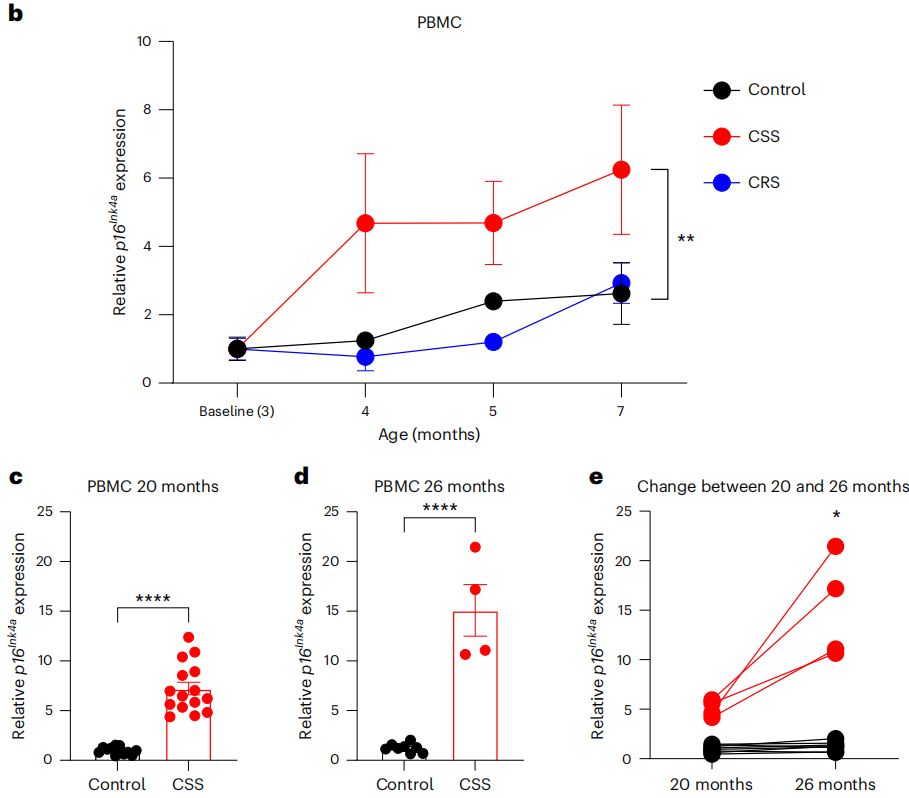
圖注:CSS促進血液PBMC表達衰老標誌物p16Ink4a,而CRS不會
No.2
別壓了別壓了,再壓就痴呆給你看
PBMC是已被公認為能代表全身變化的血細胞類型[4],其衰老指標的突然增長值得警惕,但不夠有震懾力——只是血液細胞的衰老,可能短時間內並不能顯現出對其他器官機能的影響,於是研究者們又去實驗鼠全身展開了大範圍調查。
他們還真成功找到了對CSS最敏感的功能區域:大腦。
在經歷了一個月從屬壓力的小鼠大腦裏,研究者們從海馬體和皮層中檢測到了顯著升高的衰老標誌物,除了有代表細胞衰老的p16Ink4a、還有與衰老傳播相關的炎性因子如IL-1β和IL-6;而CRS組小鼠沒有。
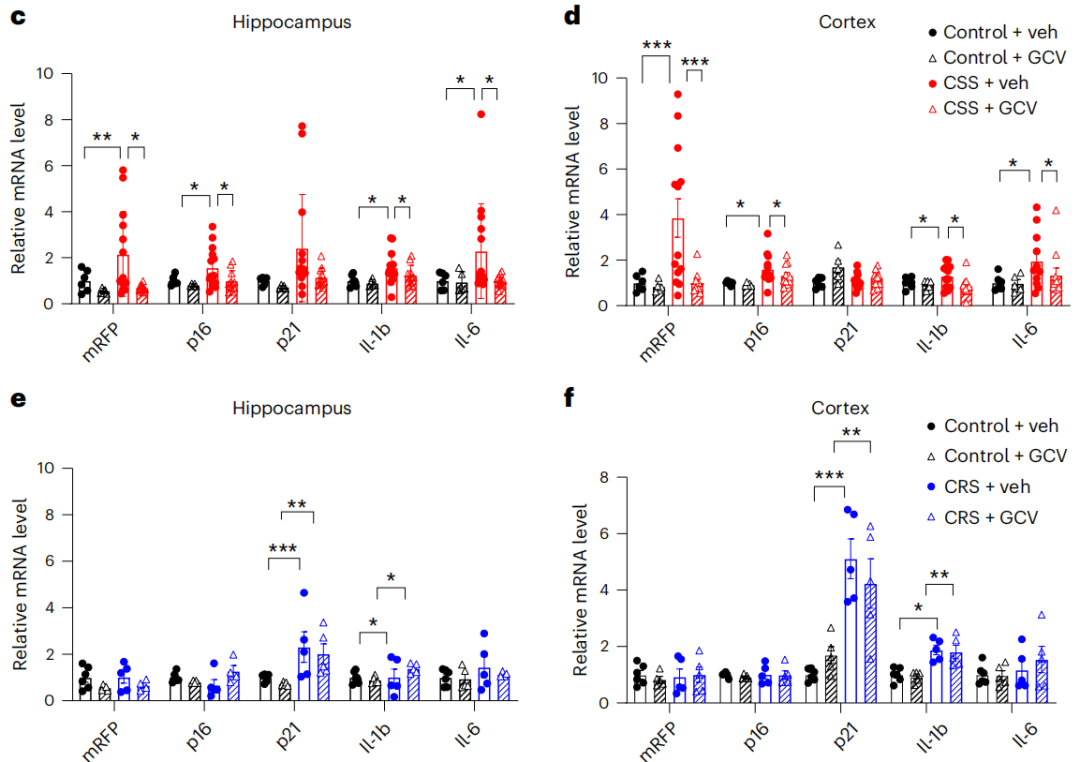
圖注:CSS能促進小鼠大腦中衰老標誌p16和炎性因子的表達,而CRS不行
為具體到細胞類型,研究者還通過腦切片探針標記技術檢測了四類主要腦細胞:神經元、星形膠質細胞、少突膠質細胞和小膠質細胞,其中神經元是負責認知的主體,其他三者都是神經元賴以生存的支持細胞。
很遺憾,受CSS影響的只有神經元。也就是説,社會從屬壓力作用於小鼠並促衰時,甚至並不打算迂迴、更傾向於直接打擊;
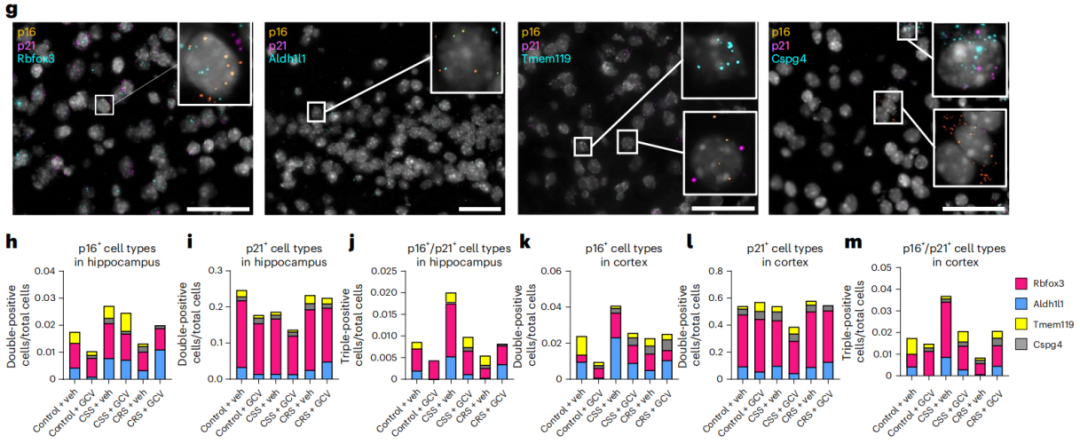
圖注:Rbfox3指代神經元,Aldh1l1指代星形膠質細胞,Cspg4指代少突膠質細胞,Tmem119指代小膠質細胞,但只有Rbfox3能和衰老標誌p16共表達
至於神經元衰老衰老了會發生什麼?無外乎就是認知功能的下降、反應能力的降低,尤其是發生在海馬和皮層這樣與記憶力、注意力、方向感知、決策和行為等息息相關的區域。
No.3
折壽12.4%?弱小、可憐、但能吃
不過,只是血液和大腦還不夠,血液的變化外表看不出來,大腦衰退了也只有自己知道,CSS一頓操作猛如虎,結果就這麼點本事?派派在本文研究的基礎上廣泛檢索了類似文章,發現關注社會從屬壓力促衰的還真有幾個“其他”課題組。
本項研究中用的是抗壓能力普普通通的C57BL/6J鼠,而有的研究用上了鼠中“軟柿子”Sv129Ev鼠,於是又發現了更多:

在長期的社會從屬壓力下,小鼠的身體成分發生改變,脂肪量不斷升高,而非脂肪體重下降[2];還會出現伴隨終生的食慾亢進和體重增加;它們糞便中的皮質酮(壓力激素)含量也會升高;其他還有身體虛弱、皮毛失色……
在上述改變的共同促使下,受試小鼠患心血管、神經退行、神經免疫、消化和代謝疾病的風險升高,如高血糖、自發性早期動脈粥樣硬化病變、抑鬱等;現象的下一步是疾病,而疾病的下一步就是死亡,而壓力鼠壽命還真比優勢鼠少12.4%,最大壽命也明顯更短[5]!
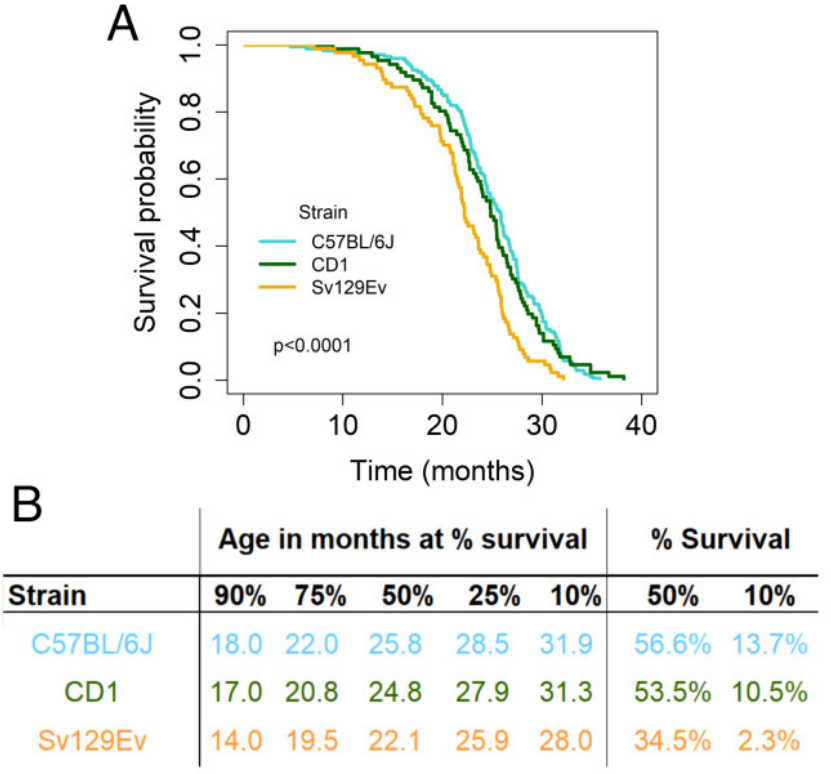
圖注:抗壓能力越差的小鼠種類壽命越短

造成衰老的原因看上去平平無奇,頻發的衰老現象聳人聽聞,想要避免在不知不覺中被“偷走”壽命,還得先從找到連接二者之間的紐帶才行。研究者們檢測了最敏感的海馬和皮層裏的p16Ink4a高表達區域,看都有哪些基因在跟着“偷偷搞事”。
在海馬中,他們發現了11個上調的基因和20個下調的基因;在皮層中,他們找到了17個上調的基因和14個下調的基因;而對比這兩組基因就會發現,它們中都有編碼DNA損傷和SASP(衰老相關分泌表型)信號傳導等的途徑,如p53非依賴性DNA損傷反應、IL-1家族信號轉導、NF-κB經典炎症信號傳導……
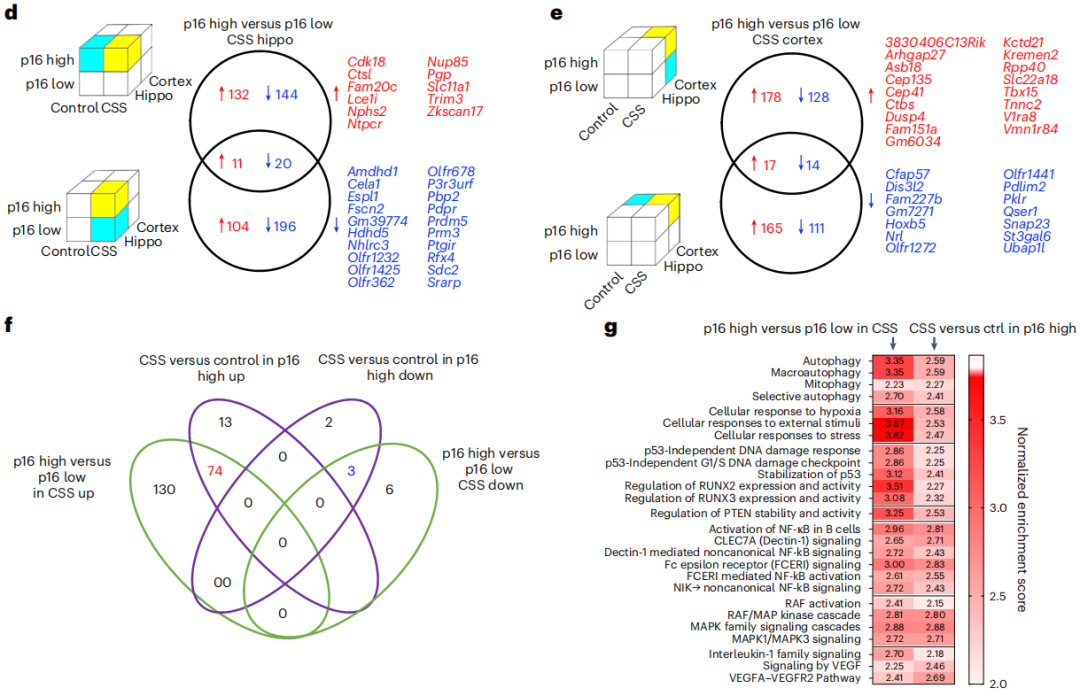
圖注:p16高表達區域的其他基因表達變化情況
之後,研究者們還將這倆組織的基因組和前人研究中總結出的各種“衰老基因組”進行比對,最終一款名為Core Senescence Signature的衰老特徵基因組成功對上了,而這組基因的源頭正是DDR——DNA損傷反應。
所以關鍵是DNA損傷?為了驗證這一點,研究者們用DNA損傷經典標誌物γH2AX來檢測CSS鼠的大腦,果然,**海馬和皮層都被標記上了!**而且和前文檢測到的衰老類型一樣,只有神經元裏檢測到DNA損傷,而支持組的膠質細胞們安然無恙。
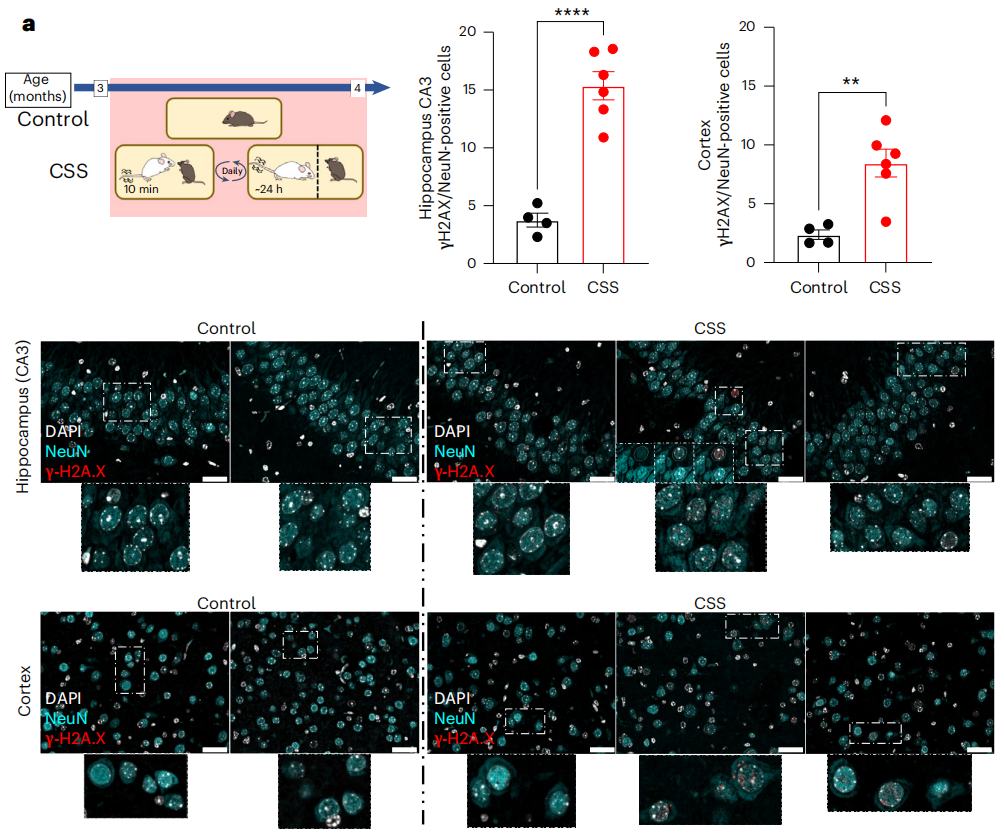
圖注:CSS後,小鼠大腦中代表DNA損傷的γH2AX水平增加
至於為什麼會產生DNA損傷,可能得歸咎於大腦裏的“警報”或“緊急”反應機制——下丘腦-垂體-腎上腺(HPA)軸。
正常情況下,HPA軸負責精心策劃大腦和身體的反應,以預測和應對環境對體內生理平衡的挑戰,比如,通過刺激皮質醇的分泌來促進肝糖原分解,以做好能量準備等。
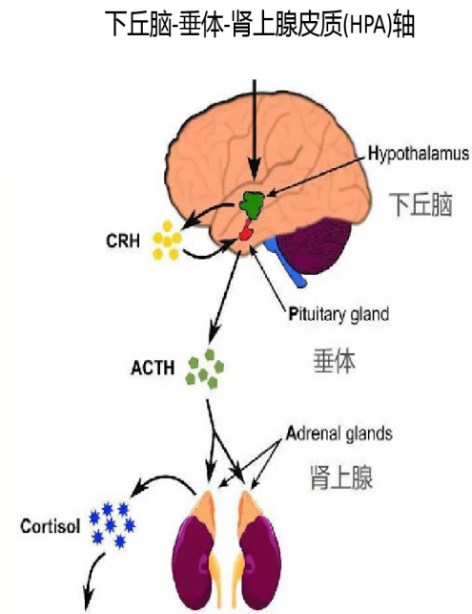
圖注:HPA軸圖示
但長期、慢性的壓力會反覆激活HPA,長此以往,HPA軸的反應就會出現異常,不足或過度或無效,大腦和身體也就會在反反覆覆甚至異常的HPA反應中產生“磨損”,其中密切參與HPA活動的前額葉皮層、海馬等自然也就首當其衝[6]。

瞭解清楚了CSS是怎麼“折磨”小鼠的,研究者只覺得後背發涼,不能再這樣下去了!必須得找到解決CSS的方法!它CSS不是通過在血液和大腦中製造大量衰老細胞來搞事情的嗎?那我們就用衰老細胞清除劑!
一針專門針對p16Ink4a陽性衰老細胞的藥物更昔洛韋(GCV)下去,CSS小鼠大腦裏的衰老細胞的確被控制住了,其數量和分泌的炎性細胞因子都被減少到對照組水平。
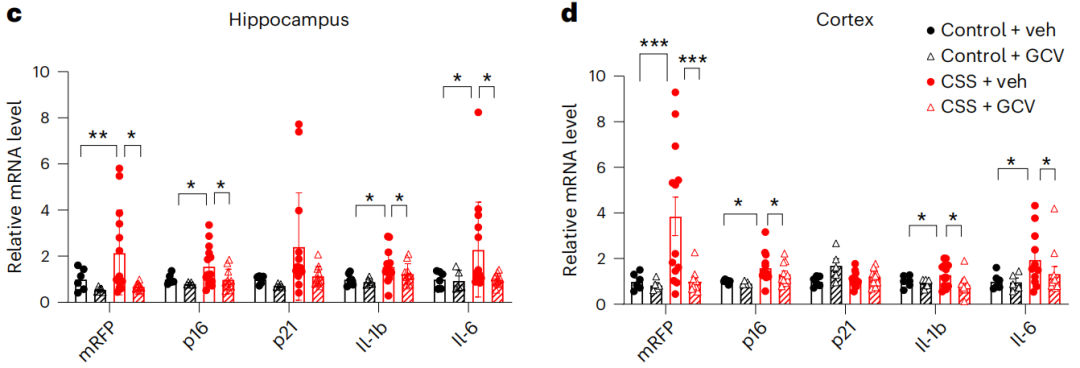
圖注:GCV作用下,經歷CSS小鼠大腦裏的細胞衰老和炎性因子水平恢復至正常水平
但研究者們還沒高興多久,就發現這……治標不治本啊!食慾亢進、體重增加、虛弱和皮毛失色都沒能得到改善,HPA激活的分子標誌物表達情況也絲毫不為所動,這衰老細胞堪稱是清除了個寂寞,似乎除了不讓CSS造成的衰老繼續惡化外,啥也挽回不了。
那怎麼辦?
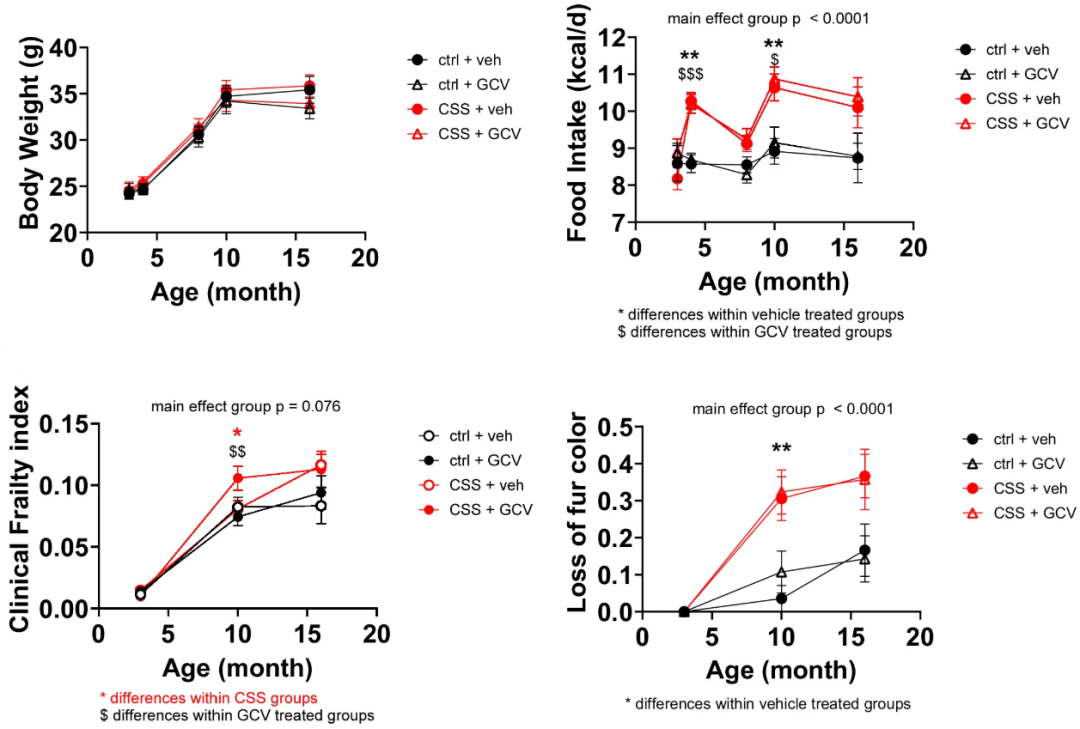
圖注:GCV雖能消除衰老細胞,但並不能改善已經出現的衰老損傷
對於這樣“慘痛”的實驗結果,本文的研究者表示要繼續探索其他Senolytics(衰老細胞清除)手段的效果,有機會還要從抗炎和抗氧化的角度試試;其他做了類似研究的文章更是兩手一攤,表示束手無策;而要派派説,與其在發生了衰老、損傷甚至折壽後求醫問藥煩惱解決方法,不如從源頭解決問題。
CSS是慢性、長期的社會從屬壓力,歸根結底還是來自於小鼠之間不恰當的社交關係,那給小鼠以選擇,讓它們早早逃離不就好了?壓力促衰的實驗進展並非一蹴而就,到4周時衰老跡象初顯,滿7周則已經“全老”且無法挽回,那也就是説,在4周內終止,都能及時止損!
研究介紹到這裏也差不多了,那在最後,派派祝研究者們能早日找到解決CSS相關衰老的方案,也祝每一隻實驗小鼠都能有光明的未來!