狂吃不胖還延壽?既想吃得美,又想活得久,抑制這一個基因就夠了!_風聞
时光派-时光派官方账号-聚集全球前沿、全面、专业抗衰资讯43分钟前

人間煙火,唯美食不可辜負!這眼瞅着馬上又要過年了,到底是選擇大飽口福呢還是陷入**“每逢佳節胖3斤”**的魔咒裏呢?關鍵是,胖了還不利於抗衰延壽啊……啊啊啊啊好糾結!要是能有啥狂吃不胖的法子就好了,已虔誠許願10086次。

要是派派説,還真有這法子,不僅能對抗狂吃變胖,還能有效抗衰….不賣關子了,今天要介紹的這篇發佈在國際期刊《Experimental&Molecular Medicine》上的研究中就藏着答案:只需對體內的特定基因動點小手腳,修煉成**“吃不胖不易老”**星人也不是不可能[1]!


那…動誰的手腳好呢?不慌,研究者根據對歷史文獻的深刻調研已鎖定了目標,即在之前的研究中因過表達而引起小鼠對胰島素的反應變得遲鈍,並導致2型糖尿病的Trib3基因[2]。
Trib3是Tribbles基因家族的成員之一,在代謝調節和胰島素信號傳導方面扮演着重要的角色。既然其過表達會導致胰島素抵抗和糖尿病,那麼給它敲掉是不是會收穫不一樣的結局呢?這次,先行探路的依舊是我們的老演員——小鼠。

首先,研究者給Trib3基因敲除小鼠和普通小鼠都吃正常食物,結果發現兩組小鼠無論在體重、代謝有關的組織重量還是對胰島素的反應能力方面都差不多,説明在正常飲食條件下,Trib3基因的存在與否對於小鼠的基本代謝功能和體重控制沒有顯著影響。
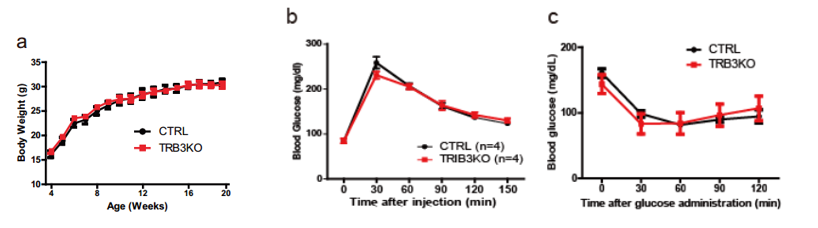
圖注:正常飲食下敲除小鼠和普通小鼠體重變化以及葡萄糖和胰島素耐量試驗
但是在給它們改善伙食後(吃脂肪含量高達60%的高脂食物)區別就來了:同樣的伙食,沒見Trib3基因敲除小鼠吃得更少,但結果普通小鼠吃成了球,而Trib3基因敲除小鼠比普通小鼠少增重了33%!
具體來説,它們體內脂肪組織的總重量和脂肪以外的身體重量都要比普通小鼠輕。也就是説,在高脂飲食條件下,敲除Trib3基因可以讓小鼠對飲食誘導的肥胖產生抵抗力。
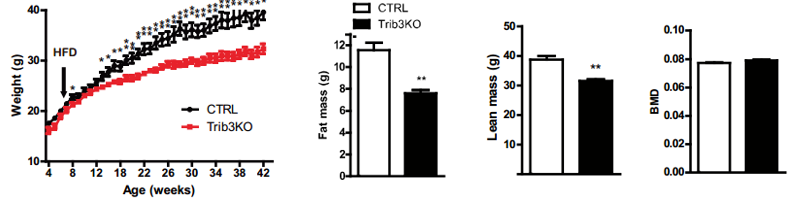
圖注:高脂肪飲食下敲除小鼠和普通小鼠體重、脂肪、瘦肉質量和骨密度變化
除了少長胖,Trib3基因敲除小鼠的代謝情況也更好一些:高脂飲食會造成普通小鼠肝臟脂肪堆積、脂肪細胞肥大以及脂肪組織炎症,但在敲除小鼠中,這些情況都要好得多;它們體內與控制血糖和能量平衡相關的細胞信號通路活性以及對胰島素的敏感性也都得到了改善。
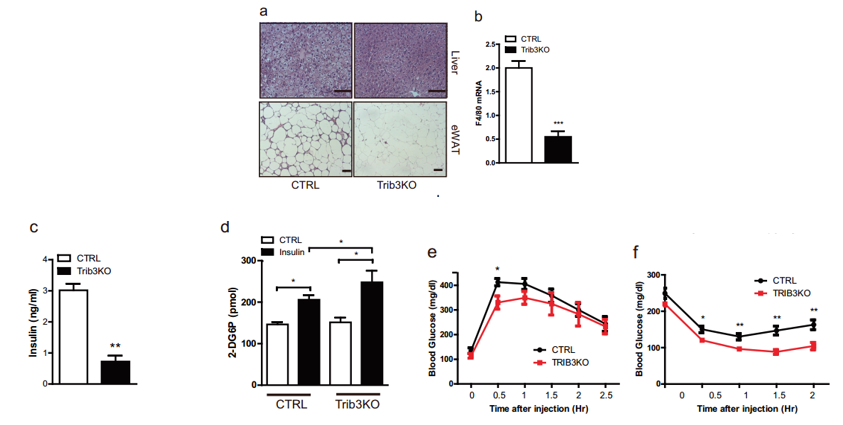
圖注:飲食誘導肥胖條件下敲除小鼠葡萄糖穩態的改善
減重、控糖和調節代謝,無私的Trib3基因表示:犧牲我,助你減輕美食的代價——變胖和促老,也不是不行。

在吃得一樣多的情況下,靠敲除一個基因就能減少33%的肉肉困擾,如果猜得沒錯,這些小鼠體重更輕的原因應該是它們消耗了更多的能量!

的確如此,Trib3基因敲除小鼠的氧氣消耗率(衡量能量代謝活動的重要指標)比普通小鼠更高,意味着它們的確消耗了更多的能量。
但這卻不是因為活動量更多引起的,而是這些小鼠體內負責機體產熱和消耗能量的棕色脂肪組織(BAT)的活性增加導致的,具體表現為:
BAT對葡萄糖的攝取率更高、表觀更紅潤(線粒體內鐵元素是BAT的顏色來源,在此表明線粒體數量在增加以支持BAT執行功能)以及脂滴更小(BAT分解脂滴釋放脂肪酸,產生能量和熱量,脂滴更小表明BAT正在活躍地分解脂肪)。
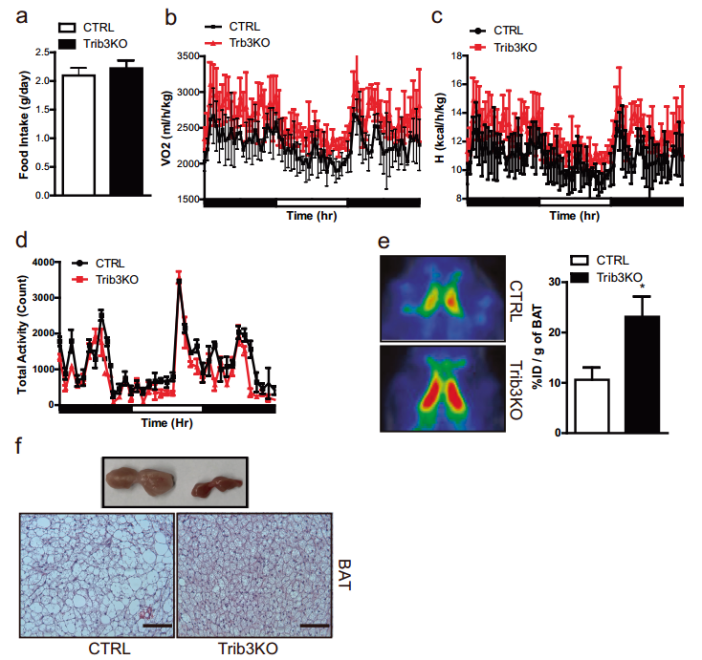
圖注:Trib3基因敲除小鼠的能量消耗和BAT活性
當進一步細查這一過程的分子機制就會發現,BAT活性增強與該組織內調節能量平衡的AMPK-ACC信號通路活性增強、脂肪前體細胞(能分化成棕色脂肪細胞,後者消耗能量產熱和維持體温)增殖和分化能力增強以及線粒體功能提高(通過非顫抖性熱產生來消耗能量)均有關。
也就是説,這些因素共同作用,使得Trib3基因敲除小鼠體內的BAT能更有效地工作,從而消耗更多的能量。
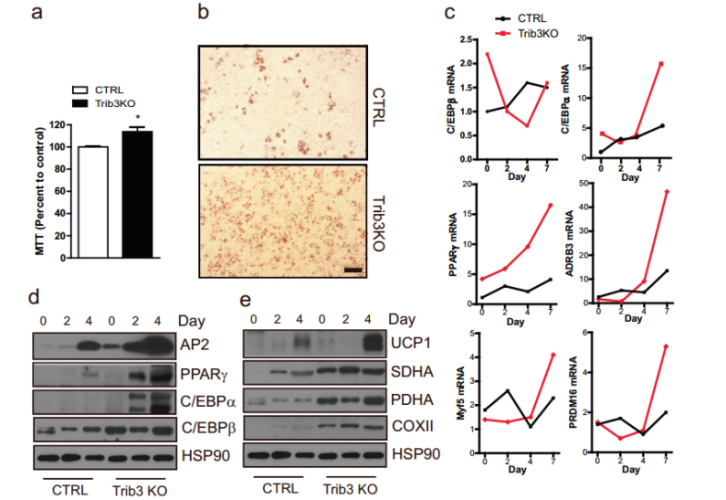
圖注:Trib3基因敲除小鼠體內的脂肪前體細胞增殖和分化能力增強以及線粒體功能提高
考慮到BAT是耗能產熱一把手,BAT活性增強使能量消耗增加,其產熱能力一定也增加了。為了進行驗證,研究人員使用了一種藥物(CL316,243)來進行測試,這種藥物可以激活BAT,使其消耗更多的氧氣,從而產生更多的熱量。
結果顯示,藥物作用下兩種小鼠的能量消耗都增加了,但Trib3基因敲除小鼠對藥物表現得更敏感,能量消耗增加更多,BAT產熱能力也更強,這可能由於,敲除Trib3基因會使BAT受體與藥物的信號傳導途徑變得更加高效或使BAT對能量底物(如脂肪和糖)的利用效率更高,從而在藥物刺激下能更有效地消耗能量併產生熱量。
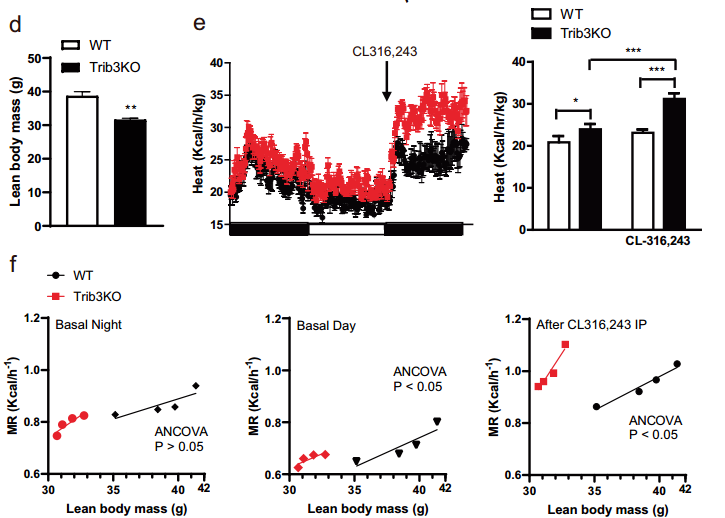
圖注:藥物(CL316,243)對Trib3基因敲除小鼠和普通小鼠的不同效果
總的來説,敲除Trib3基因會使小鼠體內的棕色脂肪組織變得更加活躍,導致能量消耗增加和產熱能力提升,表現得比普通小鼠能更高效地燃燒和利用能量!

但話説回來,這一切好處都得益於敲除了Trib3基因。那麼,沒動手腳的時候,是誰在影響Trib3的表達呢?尤其想知道,是誰推動了可能對體重和血糖調節不利的Trib3過表達情況呢?
研究顯示,高脂肪飲食是其中的一個重要因素:
在高脂飲食下,Trib3的表達水平會增加,且與遊離脂肪酸FFA(通過多種機制影響細胞內代謝和信號傳導,可能導致細胞功能障礙)和二酰基甘油DAG(能激活PKC酶,PKC通過影響脂質代謝等降低胰島素敏感性)這兩種物質有關。
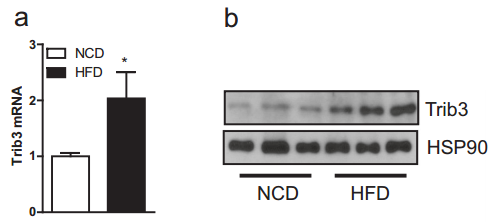
圖注:正常飲食小鼠和60%高脂飲食小鼠BAT中Trib3 mRNA和蛋白表達水平
具體來説,FFA能增加前棕色脂肪細胞(能分化成棕色脂肪細胞)中Trib3的mRNA和蛋白水平;DAG模擬物質TPA能通過直接激活PKC酶的方式增加Trib3蛋白數量,且能同時抑制Trib3降解蛋白COP1的降解作用。促表達的同時抑制降解,高脂飲食下Trib3的表達想不被增加都難!
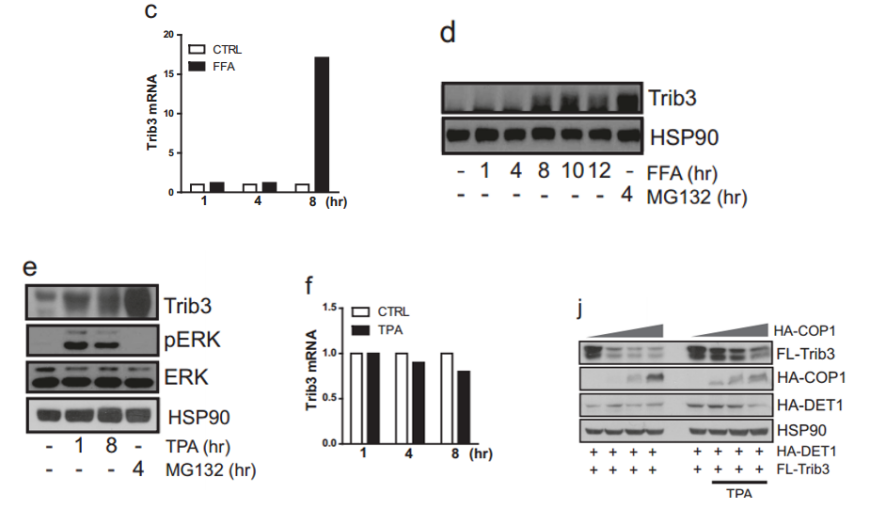
圖注:高脂飲食下FFA和DAG增加Trib3的表達
除了高脂肪飲食,年齡,也是讓Trib3表達增加的幕後Boss。

研究發現,對於年輕的Trib3敲除小鼠和普通小鼠,在正常飲食下,它們的體重和血糖控制看起來都差不多。
但大約到了1歲(小鼠中年)的時候Trib3基因敲除小鼠開始展現出更好的體重和血糖控制情況,説明隨着年齡增長,Trib3基因的表達逐漸上升,其對機體體重和血糖方面的不良影響也會越來越明顯。
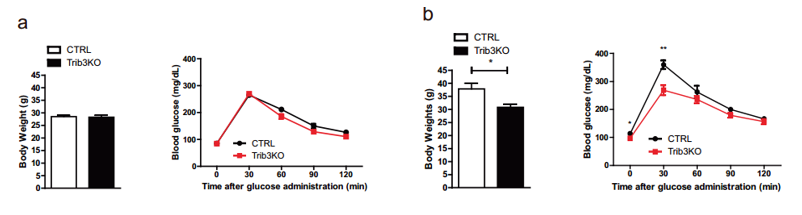
圖注:18周齡(左)和56周齡(右)時對照和Trib3基因敲除小鼠的體重和葡萄糖耐量測試
進一步檢查Trib3與衰老之間的具體聯繫發現,隨着年齡增長,棕色脂肪組織中Trib3基因的表達水平和PKC酶的活性會增加,而UCP1蛋白(負責產熱和調節能量消耗)的表達會減少,最終證實年齡增長在促Trib3表達和破壞能量代謝平衡中扮演着重要角色。
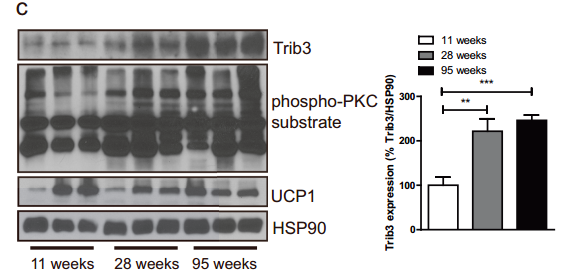
圖注:隨着年齡增長,Trib3表達水平和PKC酶活性增加,UCP1蛋白表達減少
難怪老年肥(年齡相關的體重增加)和糖尿病這些會隨着年紀找上門,看來與Trib3表達增加引發的能量代謝變化和胰島素抵抗關係匪淺!而通過敲除Trib3,不止能減輕美食帶來的肥胖煩惱,對減輕衰老相關的體重增加和葡萄糖穩態受損的影響,也是極有用的。
果然,不管是高脂肪飲食的誘惑還是衰老的不請自來,都在時時刻刻要人“老命”!所幸,抑制Trib3基因表達的剋制之法已初顯端倪,而且比起減重,通過減輕衰老相關的能量代謝變化而延長健康壽命的效果似乎更加讓人興奮哎!
目前,科學界正在考慮研發新的藥物,打算通過控制Trib3基因的活躍度來預防和治療飲食和衰老相關的肥胖和2型糖尿病。不難想象,未來一旦實現了對Trib3基因的控制,這將又會是一把對抗肥胖與衰老的得力武器!