困於繁文縟節,歐洲臨牀試驗落後中國
【文/觀察者網 張菁娟】歐洲製藥工業協會聯合會(EFPIA)21日發佈聲明稱,儘管全球臨牀試驗數量在過去十年增長了38%,但歐洲經濟區(EEA)在全球試驗中所佔的份額卻在同期減少了一半。研究表明,歐洲對臨牀研究的吸引力下降可歸因於較不利的監管和資金環境。
根據艾昆緯(IQVIA)為EFPIA和歐洲疫苗(Vaccines Europe)撰寫的最新報告顯示,歐洲經濟區開展的商業試驗(由製藥公司贊助的試驗)佔全球研究的比例已從2013年的22%降至2018年的18%,後又降至2023年的12%。
聲明稱,這意味着參與歐洲經濟區國家臨牀試驗的患者數量減少了6萬人,僅在歐洲經濟區進行的試驗名額減少了2萬個,也就是説生活在歐洲的人們將失去獲得最新藥物的機會。
然而,報告顯示,自2018年以來,中國開展的商業試驗數量翻了一番,目前佔全球商業臨牀試驗份額的18%。
報告分析認為,歐洲經濟區複雜的監管框架往往導致在審查合規性、建立試驗場地和招募患者方面比其他地區花費的時間多很多,這使得製藥商對歐洲經濟區冗長的時間表望而卻步。報告舉例稱,與美國相比,歐洲經濟區在所研究的所有治療領域(腫瘤、傳染病和罕見病)的試驗設立和獲得方面都較慢。進行多國試驗的需求對歐洲來説也具有挑戰性,而美國和中國尤其受益於龐大的患者羣體。

報告封面截圖
臨牀試驗為患者提供了獲得新藥治療的機會,一般從I期臨牀試驗到新藥被批准上市需要5-10年。
報告強調,I期臨牀試驗的意義重大,為一個地區進一步的臨牀開發、投資和融資奠定了基礎。在過去十年,全球臨牀I期試驗的佔比從32%上升至41%,而歐洲經濟區的這一比例卻從19%逐步降至14%。“其不利影響可能會在未來幾年顯現出來。”
英國《金融時報》(FT)援引歐洲製藥工業協會聯合會總幹事莫爾(Nathalie Moll)的話稱,歐洲臨牀試驗受阻於緩慢而分散的研究生態系統,目前的舉措不足以阻止和扭轉十年來的衰退。
報道指出,西班牙是一個例外,它超越德國成為歐洲開展臨牀試驗最多的國家,在截至2022年的十年間,行業投資從4.79億歐元攀升至8.34億歐元。在此期間,西班牙投資了新的研究基地並簡化了程序。此外,西班牙還在2022年註冊了900多項臨牀試驗,高於疫情前的水平。
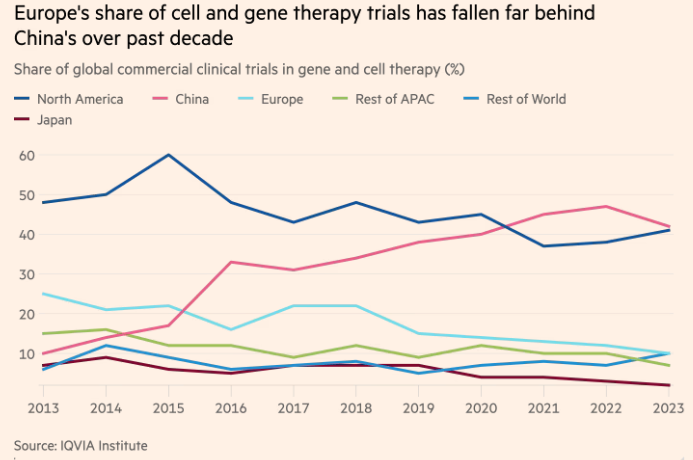
歐洲在全球CGT商業臨牀試驗中所佔的份額遠遠落後於中國 FT
據報道,世界衞生組織的一份數據顯示,2021年,包括中國在內的西太平洋地區的臨牀試驗數量已增至約2.5萬項,而十年前這一數字僅為7400項。同年,歐洲進行了約1.78萬項臨牀試驗,而2011年為1.03萬項。
今年9月,前歐洲央行行長、前意大利總理德拉吉(Mario Draghi)發佈了題為《歐洲競爭力的未來》的報告。這份報告的核心主題是簡化與革新競爭政策,以增強歐洲與全球競爭對手競爭的能力。
在德拉吉的報告中,他提議歐盟應簡化臨牀試驗的監管框架,以吸引更多的臨牀研究。
莫爾則表示,“歐洲要想具有競爭力,就需要作為一個統一的區域而不是單個成員國來運作,並通過政策支持來吸引全球研究投資”。
在歐盟,醫療保健屬於國家當局的管轄範圍,這意味着27個成員國的醫療監管往往各不相同。
《臨牀試驗條例》(CTR)於2022年1月31日起開始實施,以協調歐盟(EU)臨牀試驗的提交、評估和監督流程。伴隨着CTR的實施,全新的臨牀使用信息系統(CTIS)也隨之上線。若要開展臨牀試驗,申辦方只需在CTIS上審批通過即可,而不需要像之前那樣分別向各個國家的主管部門和倫理委員會提交臨牀試驗申請等。
歐盟委員會的一位發言人表示,研究 “如何進一步改善歐盟臨牀試驗規則的運作,從而為臨牀研究重新注入活力”將是下屆委員會的“重中之重”。歐盟委員會主席馮德萊恩此前表示,希望在今年11月之前完成新團隊的組建,但外界預計新一屆歐委會可能在12月上任。
本文系觀察者網獨家稿件,未經授權,不得轉載。