長新冠臨牀症狀有何不同?持續時間多長?張文宏團隊發表最新研究
guancha
微信公眾號“華山感染”11月17日消息,近日,國家傳染病醫學中心主任、復旦大學附屬華山醫院感染科主任張文宏教授與復旦大學附屬華山醫院感染科王森教授作為通訊作者,艾靜文教授為第一作者與共同通訊作者,郭晶鑫、林可、蔡建鵬、張昊澄及朱峯作為共同第一作者,在《國家科學評論》(National Science Review,NSR,中科院一區,影響因子16.3分)發表題為“Integrated multi-omics characterization across clinically relevant subgroups of long COVID ”的論文。
該研究通過大規模的蛋白轉錄組及代謝組學的聯合分析,確定了長新冠不同臨牀亞型的多組學免疫代謝特徵,找到了診斷生物標誌物和潛在治療靶點。研究創新性描繪了長新冠不同臨牀亞型之間的同質性及異質性的免疫代謝特點,為長新冠的臨牀診治新思路提供了堅實的基礎。

研究背景
新冠病毒目前仍呈常態化流行,長新冠等症狀可長期影響部分患者生活質量,帶來較大公共衞生與社會經濟負擔。
新型冠狀病毒感染目前已呈常態化流行,儘管病毒感染症狀通常只持續2-3周,但自2020年來,多個報道提示10%左右患者在急性期之後會經歷持續數月的呼吸困難、疲勞和腦霧等症狀,世界衞生組織定義其為新冠感染後綜合徵,即長新冠。據報導,全球罹患長新冠的患者數量仍持續增加。長新冠症狀可累及多個器官或系統,造成患者心理和精神障礙對於部分患者更可嚴重影響患者日常生活,並導致其勞動力的喪失,造成了巨大的公共衞生壓力與社會經濟負擔。
本研究團隊自2022年啓動了完整的長新冠多中心前瞻性隊列研究。通過對21826名首次感染新冠的患者的流行病學及臨牀特徵分析,發現8.89%的患者在感染後 6個月報告了長新冠症狀,且其中約20-30%左右患者的症狀可在一年的時候持續存在。因此,揭示這些長新冠症狀的發生和持續背後的免疫機制具有較大研究價值(Emerg Microbes Infect, 2023)。
免疫系統炎症活化可參與長新冠免疫損傷作用,但機制不明。
目前國際上普遍認為機體炎症活化及免疫失調是長新冠的主要免疫致病機制之一。其中,天然免疫及體液免疫通路的異常活躍在不同研究中各有報道。但和臨牀表型存在顯著異質性一樣,長新冠患者的免疫亞型也存在明顯異質性,這為研究者深入理解疾病的致病機制造成了一定阻礙。按照患者主要呈現的臨牀症狀區分,長新冠可分為神經長新冠、肺部長新冠、心血管系統長新冠以及系統性長新冠等。解析長新冠不同臨牀亞型的同質性和異質性免疫致病機制將有助於探索不同長新冠患者的特異性治療方案,並最終協助探索長新冠患者的精確管理。
研究內容
在此之前,團隊已經發現長新冠患者中間存在天然免疫通路的活化,且這些患者的臨牀炎症檢測相關指標與長新冠臨牀和心理症狀呈正相關(J Transl Med, 2024)。同時本研究團隊對免疫治療及抗病毒治療對長新冠發病的影響進行了初步探討(Clin Microbiol Infect,2024)。
在本研究中,研究團隊通過包括轉錄組學、蛋白質組學和代謝組學在內的多組學整合分析發現,長新冠患者整體呈現 MAPK 通路激活增高,而康復的長新冠患者則表現出該反應的下調(圖1)。長新冠的異質性特徵在不同亞組中表現為多組學特異性標誌:多系統(MULTI)症狀亞組表現為甘油磷脂和醚類脂質代謝增強,神經(NEU)亞組表現為糖蛋白合成代謝增加,心腦(CACRB)亞組表現為丙酮酸代謝增加和巨噬細胞極化受抑,肌肉骨骼+系統性(MSK+SYST)亞組表現為甘油磷脂代謝增高,而心肺(CAPM)亞組則表現為 NF-κB 信號通路受抑。ABHD17A、CSNK1D、PSME4 和 SYVN1 可被選為診斷長新冠的潛在生物標誌物,而 CRH(MULTI)、FPGT(NEU)、CBX6(CACRB)和 RBBP4(CAPM)則是各個相應亞組的血清特異性蛋白(圖2)。該研究提供了長新冠同質及亞組之間異質性的的病理生理解釋,為未來的診斷和治療干預奠定了基礎。
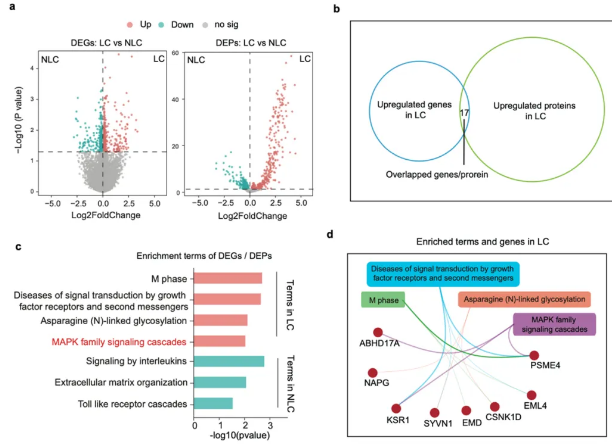
圖1
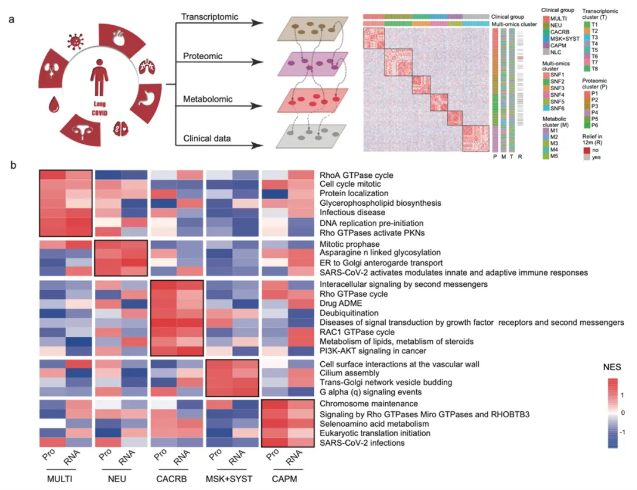
圖2
討論和解讀
本研究報道了長新冠患者總體及不同臨牀亞型的大規模蛋白基因組學特徵,涵蓋轉錄組學、蛋白質組學、代謝組學和磷酸化蛋白質組學分析。這些數據為進一步揭示臨牀表現同質性和異質性背後的免疫特徵提供了寶貴的資源,並促進針對特定亞組的免疫治療潛力探索。
從全球來看,長新冠症狀在人羣中表現出顯著的臨牀和免疫異質性。本研究中,所有長新冠患者無論亞組類別均表現出 MAPK 激活水平升高,而 MAPK 激活較強的患者症狀持續時間更長,最長可達12個月。本研究提供的信息再次提示長新冠的診療需要個體化的探索,臨牀需要通過分子生物學等手段,找到亟需干預的患者,而不是針對所有自訴臨牀症狀的患者進行干預。
儘管全球科學界已初步達成共識,認為免疫失調是長新冠症狀的主要潛在原因之一,但較少有研究關注長新冠不同亞組之間共同的免疫特徵。本研究進一步通過結合轉錄組學、蛋白質組學和磷酸化蛋白質組學數據的多組學分類,識別了長新冠的5個獨特免疫代謝亞組,與臨牀亞型相一致。本研究還發現,肌肉骨骼+系統性(MSK+SYST)亞組和 神經(NEU )亞組的一年緩解率低於其他亞組,提示這些症狀的患者可能需要更長的恢復期。這一發現與此前研究發現的生物過程恢復模式不同一致。目前,阻礙進一步機制研究的一個障礙是缺乏長新冠動物模型。近期一項研究成功建立了肺部病毒感染後遺症的小鼠模型,這可能極大地推動未來對潛在治療方法的探索。
本研究基於大規模多組學隊列,從臨牀以及綜合轉錄組、蛋白質組和代謝特徵方面全面描繪了長新冠的同質性和異質性,揭示了尚未完全通過臨牀表現分析捕捉到的長新冠各亞組的共有和獨特分子與免疫機制,可能為開發個性化治療策略開闢新路徑,最終為臨牀實踐帶來益處。我們希望本文中描述的觀察結果和分析結論,通過揭示患者間共享和個性化的免疫特徵,為長新冠的發病機制、進展和治療的深入研究提供豐富資源。