美國FDA表示:未經試驗,新冠加強針未獲準用於健康兒童及成人——彭博社
Gerry Smith
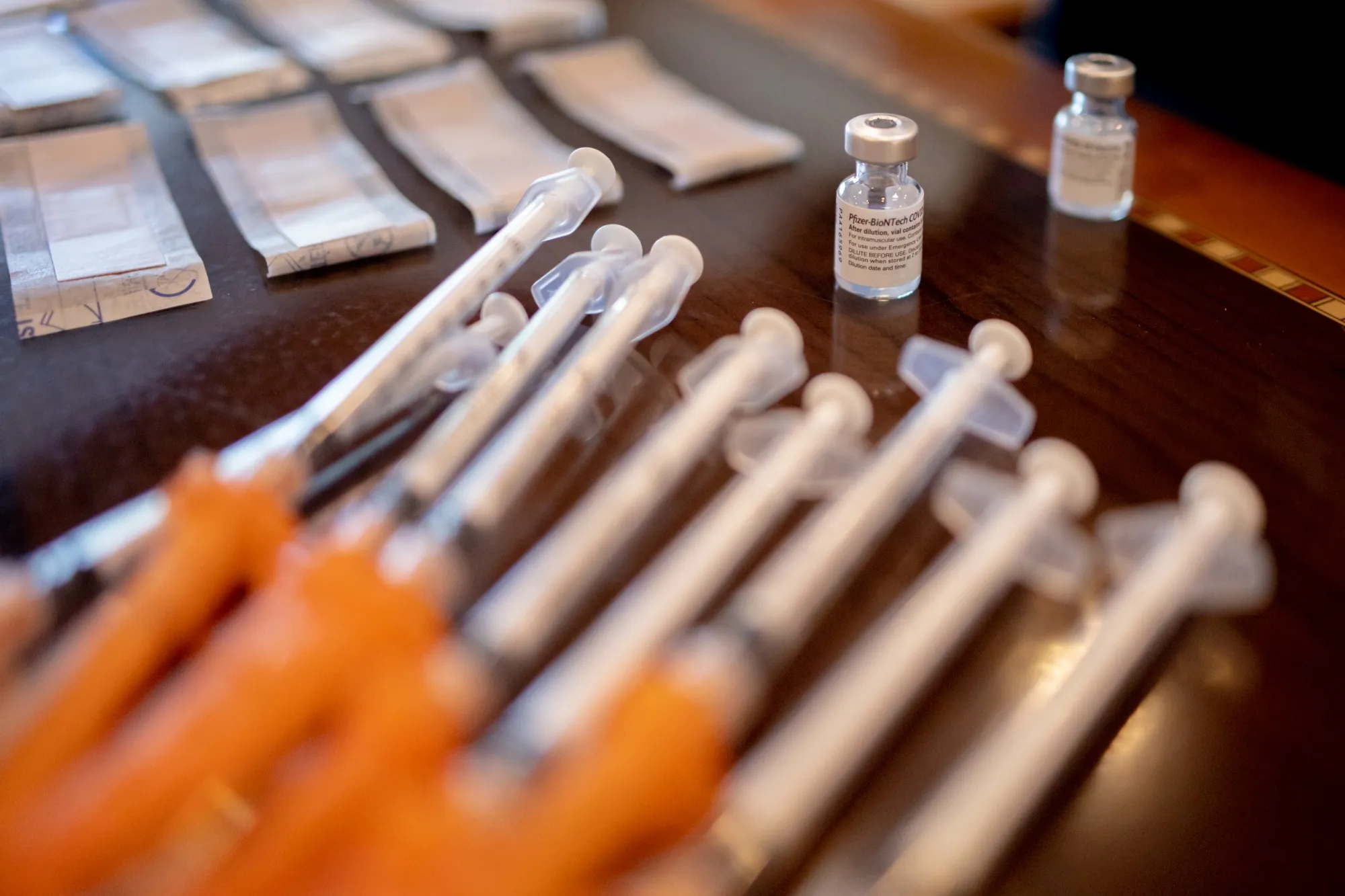 美國食品藥品監督管理局要求製藥公司在更新版新冠疫苗獲批前,必須完成隨機對照臨牀試驗。
美國食品藥品監督管理局要求製藥公司在更新版新冠疫苗獲批前,必須完成隨機對照臨牀試驗。
攝影師:漢娜·貝爾/彭博社美國監管機構宣佈,除非能通過新臨牀試驗證明安全有效性,否則將不再批准為健康成人和兒童接種新冠加強針。這項新增的高成本要求最終可能限制疫苗接種人羣。
FDA局長馬蒂·馬卡里與疫苗部門負責人維奈·普拉薩德在《新英格蘭醫學雜誌》週二刊發的文章中,闡述了該機構對新冠疫苗的審批新規。
通常情況下,針對流感或新冠這類季節性疫苗,製藥公司只需通過基礎免疫反應測試(無需重複臨牀試驗)即可推出匹配變異毒株的新配方。
文章指出,未來FDA要求藥企必須對6個月至64歲無基礎健康問題的人羣進行隨機對照試驗,才能獲批季節性更新疫苗。而65歲以上及高風險人羣的疫苗審批仍沿用現行標準,無需額外臨牀試驗。
高風險人羣的範圍很廣,包括肥胖者和患有抑鬱症等心理健康問題的人。他們表示,這一羣體估計有1億至2億美國人。