晚期癌症被治癒!CAR-T讓患者活了18年_風聞
医学界-医学界官方账号-为你提供可靠、有价值的内容是我们的存在方式。51分钟前
治療後,5名晚期神經母細胞瘤患者存活超過13年。研究人員指出,他們可能已經被徹底治癒了。
**撰文 |**凌 駿
責編丨汪 航
19年前,一位年僅4歲的美國女孩患上了神經母細胞瘤,在接受標準治療後腫瘤仍在持續進展,“走投無路”的父母帶她參與了一項CAR-T療法的早期臨牀試驗。
如今,這位女孩創造了一個醫學奇蹟。18.2年,這是迄今為止CAR-T療法創造的世界最長存活紀錄。她已經結婚生子,多年來沒再接受過任何抗癌治療,醫生也檢測不到任何腫瘤跡象。
2025年2月17日,美國貝勒醫學院等機構的學者在《自然·醫學》發佈了這一創舉,參與試驗的19名患者中,7人存活了8年以上,其中3人實現完全緩解。
浙江大學醫學院附屬兒童醫院莫干山院區副院長、國家兒童健康與疾病臨牀醫學研究中心癌症研究中心主任王金湖教授對“醫學界”分析,儘管論文存在部分“細節數據缺失”,“但它釋放了積極的信號,未來手術聯合細胞治療等多種前沿手段,將對神經母細胞瘤的治療產生變革性影響。”
研究發佈後,《自然》在頭版跟進評論
無病生存18.2年
此次研究啓動於2004年,是一項CAR-T療法的I期臨牀試驗。
當時,距離全球第一款CAR-T細胞產品獲批還有13年。作為先行者,研究團隊希望探索出其在實體瘤治療中的長期潛力。
為此,他們招募了19名復發/難治性神經母細胞瘤患者。這是一種多發於兒童的實體瘤,惡性程度高、治療難度大且易發生骨轉移。相關統計數據顯示,其在兒童中的發病率約為1/7000,90%發生在5歲以下兒童,15%的患癌兒童是死於神經母細胞瘤。
“依靠手術和放、化療,過去高危或復發骨髓轉移的神經母細胞瘤患兒,總體5年生存率僅在30%左右。現在結合幹細胞移植、免疫治療等多種手段,大概也只提升到了約50%。”王金湖向“醫學界”介紹。
入組時,這19名患兒已經處於Ⅳ期,意味着腫瘤發生了遠處轉移。而根據最新發布的數據,有7名患者最後一次隨訪時尚存於世,其中2人在生存分別超過8年和10年後失訪,失訪前腫瘤處於完全緩解(CR)和無疾病證據狀態(NED)。
另外5名持續接受隨訪的患者,存活超過13年,目前均處於CR/NED。研究人員指出,“他們可能已經被徹底治癒了。”
其中,最久的一名患兒無病生存長達18.2年。當時她才4歲,已經出現難治性骨病變,但如今她的腫瘤完全緩解,還成為了兩個孩子的母親。相對遺憾的是,這名患者得了神經性失聰,研究人員認為這是此前接受化療導致的後遺症。
也有12名患兒在治療後2個月到7年間不幸離世,他們大多當時已處於較嚴重的疾病狀態,出現大面積腫瘤復發、骨髓復發或骨損傷。研究人員表示,這説明初始狀態相對較好的患者,更容易從CAR-T療法中獲益。
值得一提的是,根據2004年研究團隊登記的臨牀試驗註冊信息,他們一開始的計劃是,所有患者至少要隨訪15年以上,這不僅是為了驗證療效,還能加深對CAR-T療法的生物學理解,並驗證長期的安全性風險。
由於CAR-T療法使用了經過基因工程改造的T細胞,是否會導致繼發性T細胞惡性腫瘤,始終是業內關心的話題。
通過最長達18年的隨訪,研究團隊指出,“(這項研究)沒有證據表明CAR-T細胞治療會導致腫瘤,或其他長期後果。”
河南省腫瘤醫院免疫治療科主任高全立教授對“醫學界”表示,“這是非常令人驚喜的結果,而且還是20年前的研究,用的還是第一代CAR-T細胞”。
一個“瘋狂的想法”
“2004年我們啓動這項研究時,CAR-T還是一個‘瘋狂的想法’。它基於一種‘奇怪’的合成生物學,真的能起作用嗎?”研究團隊成員,貝勒醫學院免疫療法研究員Helen Heslop博士在接受《自然》採訪時回憶道。
由於當時使用的是第一代CAR-T細胞,隨着技術迭代早已被棄用,在2009年的I期臨牀試驗結束後,研究也停止了患者招募。“那時也是腫瘤細胞免疫治療的‘黑暗時代’,業內並不看好免疫療法,因此很難找到投資持續推進研發。”高全立對“醫學界”分析。
但十多年來,團隊並未停止對試驗患者的後續跟進。他們還在CAR-T細胞相關的結構設計、生物學理解,以及針對淋巴瘤、胰腺癌、乳腺癌等惡性腫瘤的治療上,發表了數十篇研究論文。
期間,CAR-T療法也迎來飛躍式發展。自2017年首個CAR-T療法獲批以來,CAR-T細胞已經更新到第五代,目前全球共有12款CAR-T細胞產品上市,涉及多類血液瘤適應證。
雖然CAR-T療法改變了血液瘤患者的命運,但醫生們始終難以在實體瘤治療上成功複製。
高全立告訴“醫學界”,相對於血液瘤治療中相關靶點的特異性較高,早期針對實體瘤的靶點多為腫瘤相關抗原(TAA),在正常組織中有所表達,導致CAR-T療法有較高的“腫瘤脱靶”風險。
而此次研究團隊率先使用的CAR-T細胞,針對的是GD2靶點,“GD2在神經母細胞瘤中特異性較強,最終取得這樣的成績,為學界後續開發針對實體瘤的CAR-T療法,提供了信心和啓示。”高全立説。
“這應該是未來神經母細胞瘤治療的重點方向之一。”王金湖稱。據悉,自貝勒醫學院團隊進行首次試驗以來,學界已經開發出針對神經母細胞瘤的新型CAR-T細胞,並不斷調整治療方案,以尋求更好更全面的治療效果。
今年1月25日,意大利研究人員在《自然·醫學》發文指出,通過靶向GD2的新一代CAR-T療法,在5名復發/難治性高危神經母細胞瘤患兒中,2人達到完全緩解,1人持續部分緩解。
王金湖表示,隨着現代外科技術發展,很多曾經被認為是不可能切除的腫瘤,已經可以實現CME(肉眼可見病灶完全切除),配合放化療等,神經母細胞瘤患者的局部複發率可以控制在非常低的水平。“目前高危組患者的5年生存率還是隻有50%左右,主要是因為它的骨髓和骨轉移病灶。”
實體腫瘤特殊的免疫抑制微環境,和瘤體內部複雜的異質性是限制CAR-T細胞療效的關鍵因素。“但骨髓和骨骼轉移灶處於一個有豐富血供的環境,CAR-T療法因此能有機會發揮更好的效力。”
“同時,GD2還不僅只在神經母細胞瘤中高表達,在其他一些癌種,比如部分腦膠質瘤中也展現出了潛力。”王金湖説。
CAR-T有望治癒癌症嗎?
研究發佈後,《自然》迅速跟進評論:我們有理由保持樂觀。但與此同時,也還有很長的路要走。
王金湖對“醫學界”分析,“雖然取得了不錯的結果,但可能由於是20年前的試驗,這篇論文缺失了不少細節。比如入組患者雖然都是Ⅳ期,但未説明具體的病理類型,沒給出危險度分組。”
事實上,試驗中有一部分孩子經過前期治療,使用CAR-T細胞時已經處於癌症緩解狀態。“對於這部分患兒,很難評估CAR-T療法對長期生存到底發揮了多少作用。論文也表明,治療時病情危重的患兒,後續生存情況並不理想。”王金湖説。
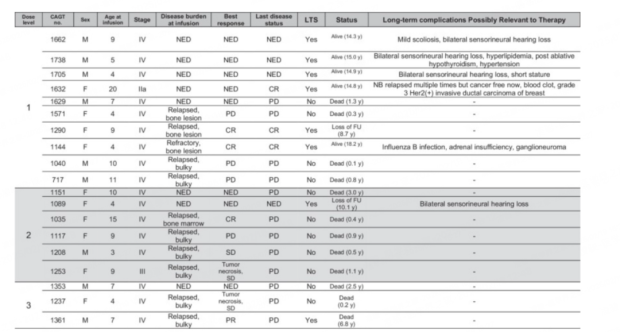
患者的基線狀態和隨訪進展,部分在治療時已處於NED/CR狀態 圖源:《自然·醫學》
“CAR-T療法存在一些天然缺陷,如製備複雜、治療過程繁瑣,需要清淋預處理等。同時,神經母細胞瘤的成分也非常複雜,很多壞死區域處於缺血缺氧的環境,幾乎沒有血供,CAR-T細胞很難進入腫瘤內部起到殺傷作用。”
因此王金湖認為,未來需要運用精準醫學手段,針對不同癌種,對不同類型的患者進行分組,並配合多種治療方式,找到CAR-T療法的最佳治療人羣和時機。
“在神經母細胞瘤的治療中,通過手術和放化療等手段清除軟組織病灶,後續應用高效的CAR-T療法清除骨髓和骨骼等的轉移病灶,將是高危組患者實現長期生存極有前景的方向。”
“基於不同的技術平台、設計方法等,CAR-T細胞有很多種類,給治癒癌症帶來了無限可能。雖然目前在實體瘤領域進展還比較慢,但所有改變人類醫學的革命性療法,都是這樣一步步發展起來的。”王金湖説。
據王金湖介紹,目前他的團隊和合作夥伴,也啓動了針對復發/難治性神經母細胞瘤的通用型CAR-T治療技術的研發,“在前期的幾例‘同情用藥’患者中,我們看到了可喜的療效,近期將會進一步推進研發和臨牀應用。”
全球範圍內,在CAR構建體的優化、確定創新治療組合策略等方面,諸多研究機構均展開了多維度嘗試。比如進行“雙特異性”設計,即針對同時表達有兩種腫瘤抗原的癌細胞,既提高了抗腫瘤活性,也避免了誤傷只表達單一抗原的健康細胞。
美國研究人員則對CAR-T細胞進行了雙重改造,既能靶向抗腫瘤靶點,又表達了有利於T細胞在腫瘤微環境中活化的白介素-15(IL-15),I期臨牀試驗中12位實體瘤患者8人疾病得到控制。相關成果於2024年10月發佈於《自然》。
高全立表示,就癌症治療技術的前景而言,目前不少前沿療法的試驗數據,短期療效並不比CAR-T療法差,甚至有些還要更優,“但CAR-T療法展現出的‘癌症治癒’潛力,是學界不斷推動其研發的根本動力。”